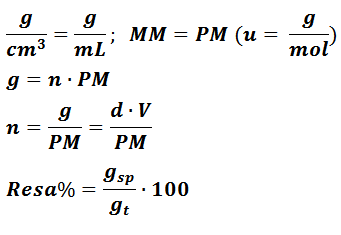ESERCITAZIONE: Sintesi dell’Acetanilide
OGGETTO: Preparazione di Acetanilide tramite reazione di acilazione tra anilina e anidride acetica.
FORMULE
LEGENDA:
gsp= grammi sperimentali netti
gt= grammi teorici
gl= massa lorda
MM o PM = Massa Molecolare (o Peso Molecolare)
d= densità
p.f.= punto di fusione
V = Volume (mL)
n= moli
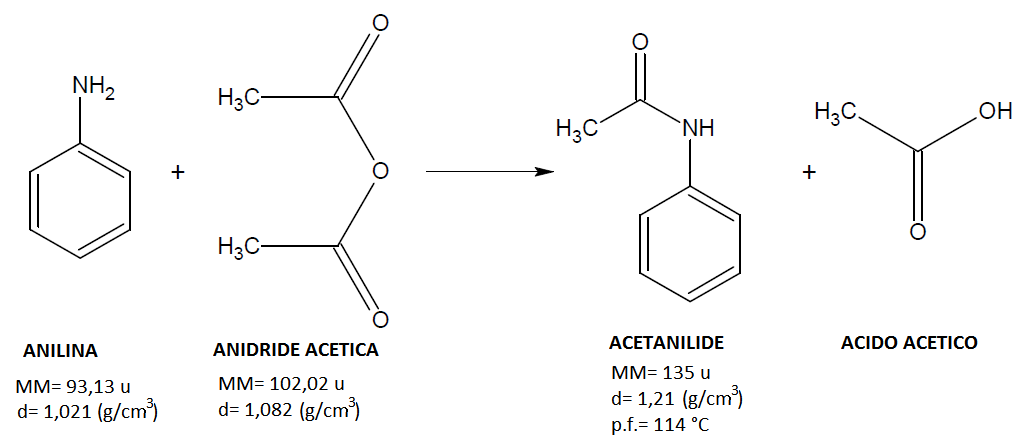
REAZIONI
CALCOLI e RISULTATI
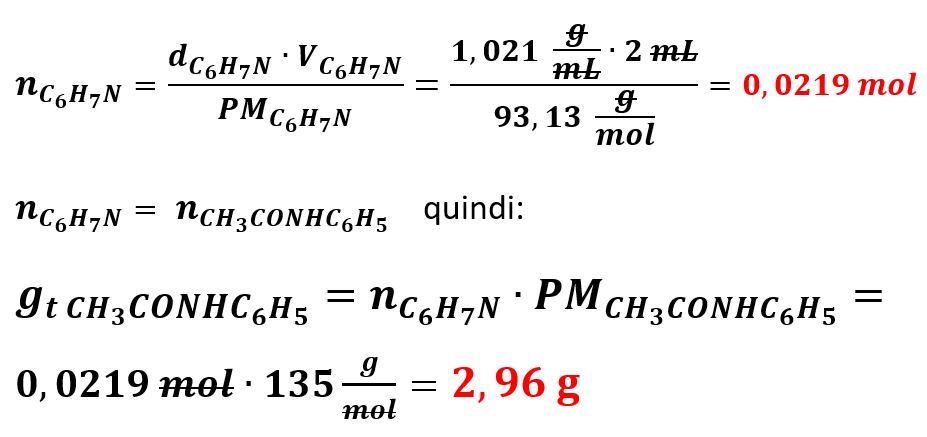

TABELLA
| GRUPPO | MASSA LORDA [g] | TARA [g] | MASSA NETTA Sperimentale [g] | MASSA MEDIA [g] | MASSA Teorica [g] | RESA [%] |
| 1 | 2,30 | 0,23 | 2,07 | 1,98 | 2,96 | 66,9 |
| 2 | 2,16 | 1,93 | ||||
| 3 | 2,23 | 2,00 | ||||
| 4 | 2,15 | 1,92 |
STRUMENTI, APPARECCHI E SOSTANZE
- Bilancia Tecnica;
- Cappa d’aspirazione chimica;
- Bunsen;
- Becherone con acqua;
- Becher;
- Spruzzetta con acqua distillata;
- Provettoni lunghi 15 cm;
- Guanti;
- Stufa;
- Anidride acetica (CH3CO)2O;
- Anilina (C6H7N);
- Pompa per il sotto vuoto;
- Carta da Filtro;
- Imbuto Büchner;
- Vetrino d’orologio;
- Cubetti di ghiaccio;
- Metanolo.
RELAZIONE
CONOSCENZE TEORICHE
L’acetanilide è un sale poco solubile in acqua a temperature basse che è stato il precursore degli antipiretici ed appartiene alla stessa famiglia del paracetamolo e dell’acido acetilsalicilico (aspirina). Al giorno d’oggi esso è stato abbandonato per questi usi a causa dei suoi effetti collaterali.
La metodica utilizzata per la preparazione dell’acetanilide è una reazione di acilazione che usa come mezzo acilante l’anidride acetica al posto dell’acido acetico perché è più energica.
L’anidride acetica deriva dall’acido acetico ed è un liquido corrosivo, infiammabile e dannosissimo per l’uomo e l’ambiente.
L’anilina è un liquido avente massa molecolare 93,13 u e densità 1,021 g/cm3. Essendo un’ammina aromatica essa è altamente tossica, corrosiva, pericolosa per l’ambiente e può essere cancerogena, per questo motivo va lavorata sempre sotto cappa e con l’utilizzo di guanti.
DESCRIZIONE DELLA PROVA
Lo scopo della prova è quello di preparare l’acetanilide. Per farlo si utilizza la metodica dell’acilazione dell’anilina con l’anidride acetica.
Le seguenti procedure vanno effettuate tramite l’utilizzo di guanti e sotto cappa accesa.
In una provetta lunga si aggiungono 2 mL di anidride acetica e 2 ml di anilina e si porta all’ebollizione in un bagno maria per circa 10 minuti per accelerare la reazione. L’avvenimento della reazione è facilmente riconoscibile grazie all’odore dell’acido acetico liberato.
Al termine dei dieci minuti si lascia raffreddare la soluzione e la si versa velocemente in un becher con 10 mL di acqua distillata e 1 cubetto di ghiaccio per facilitare la cristallizzazione dato che l’acetanilide è poco solubile in acqua ed abbassando la temperatura la solubilità diminuisce ancora di più.
Dopo aver inserito la soluzione nel becher, l’acetanilide cristallizza immediatamente e va effettuata una filtrazione sotto vuoto tramite imbuto Büchner con carta da filtro. La carta da filtro prima di essere inserita va pesata sulla bilancia tecnica in modo da conoscere la tara da eliminare tramite i calcoli. Il sotto vuoto facilita la filtrazione tra parte liquida e parte solida. Vanno effettuati 2 o 3 lavaggi con acqua fredda in modo da raccogliere tutti i cristalli.
Al termine della filtrazione, la carta da filtro va posizionata su un vetrino d’orologio e va posta in stufa ad essiccare a 100 °C perché una temperatura al di sopra dei 114 °C porterebbe alla fusione dell’acetanilide.
Al termine dell’essiccazione si dovrebbe procedere ad un ulteriore purificazione tramite cristallizzazione sciogliendo l’acetanilide grezza in acqua e metanolo che viene prima riscaldata in modo che l’acetanilide si disciolga e poi si lascia raffreddare lentamente in modo da ricristallizzare l’acetanilide che questa volta diventa più pura. Per mancanza di tempo, andiamo ad analizzare e pesare l’acetanilide grezza sulla bilancia tecnica. Si fa una media di tutti i valori e si calcola la resa in percentuale. (Calcoli)
Un’altra prova che andrebbe fatta è la determinazione del punto di fusione della sostanza che consente di verificare la sua purezza, infatti se coincide con il punto di fusione teorico dell’acetanilide (114 °C) vuol dire che è pura.
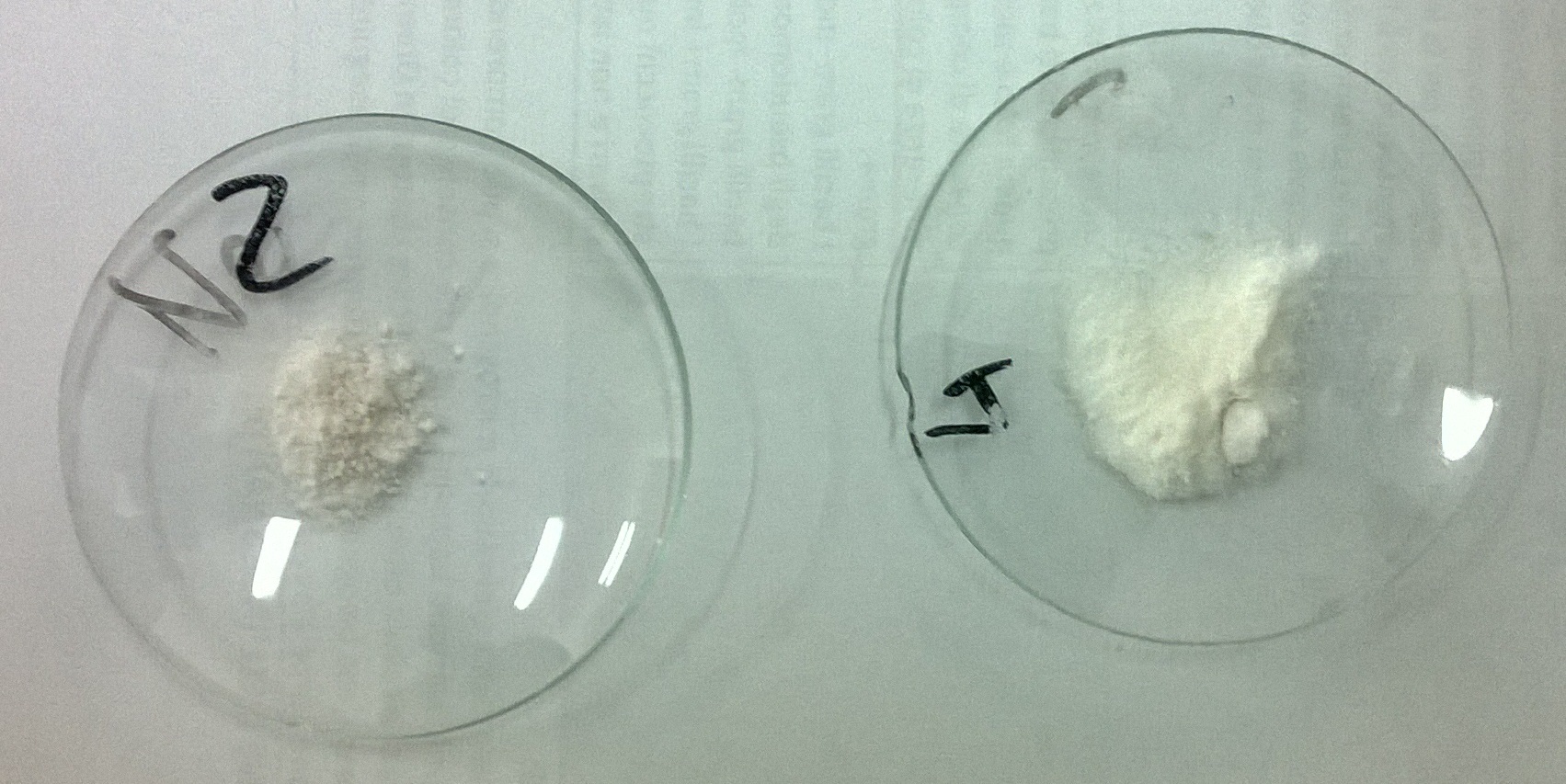
OSSERVAZIONI
Come già si può osservare dall’immagine, l’acetanilide grezza (a sinistra) è più grossolana ed ha un colore più grigiastro rispetto all’acetanilide pura (a destra) che è bianca, inoltre essa ha un odore di aceto a causa della presenza dell’altro prodotto della reazione (l’acido acetico), per questo motivo non è stato necessario determinare il punto di fusione. Sotto questo punto di vista, la resa può risultare falsata perché non abbiamo un composto puro.
Inoltre la resa è risultata più bassa anche a causa del fatto che l’anidride acetica usata da noi era abbastanza vecchia: un reattivo vecchio è meno efficace di uno nuovo.
CONCLUSIONE
Grazie a questa prova si può comprendere la tecnica di preparazione dell’acetanilide tramite acilazione. Questa tecnica può raggiungere rese anche alte, ma le tempistiche di lavorazione sono molto lunghe e richiedono molta manualità, attenzione e ripetizioni di passaggi.