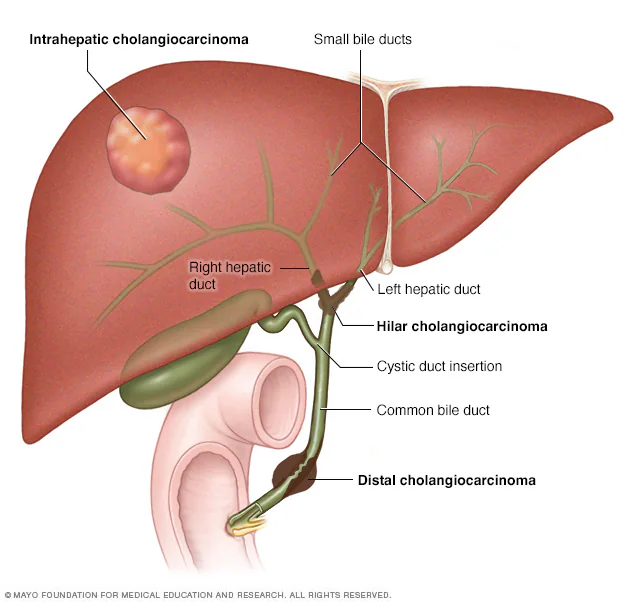
Il colangiocarcinoma ilare (HC), noto anche come tumore di Klatskin, è una neoplasia rara e aggressiva che origina alla confluenza dei dotti epatici destro e sinistro. Data la sua localizzazione anatomica critica e la sua tendenza all’infiltrazione locale, la gestione di questa patologia è eccezionalmente complessa e la prognosi rimane spesso infausta. La complessità della diagnosi, della stadiazione e del trattamento richiede un approccio multidisciplinare integrato per ottimizzare i risultati per i pazienti, sottolineando l’importanza di una stretta collaborazione tra specialisti.
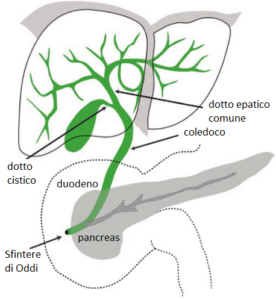
Il tumore prende il nome dal Dr. Gerald Klatskin, che per primo ne descrisse le caratteristiche cliniche e patologiche distintive in una pubblicazione del 1965. Dal punto di vista anatomico, si tratta di un tipo di cancro dei dotti biliari extraepatici che si sviluppa nel punto in cui i dotti epatici destro e sinistro si uniscono per formare il dotto epatico comune, tipicamente al di sopra dell’inserzione del dotto cistico. Questa localizzazione strategica porta a un’ostruzione biliare precoce, ma rende anche la resezione chirurgica tecnicamente impegnativa.
Caricamento….
- Epidemiologia
- Fattori di rischio
- Presentazione clinica
- Valutazione diagnostica
- Esami di laboratorio
- Tecniche di Imaging
- Colangiografia diretta e biopsia
- Caratteristiche patologiche
- Sistemi di stadiazione
- Strategie di gestione e trattamento
- Ottimizzazione Pre-operatoria
- Resezione Chirurgica
- Trapianto di Fegato (OLT)
- Terapie non chirurgiche e palliative
- Prognosi e fattori prognostici
- Conclusioni
Epidemiologia
Comprendere l’epidemiologia e i fattori di rischio associati al colangiocarcinoma ilare è fondamentale per l’identificazione dei pazienti ad alto rischio, per lo sviluppo di strategie di sorveglianza e per la ricerca eziologica. Sebbene si tratti di una patologia rara nei paesi occidentali, la sua incidenza è notevolmente più elevata in alcune aree geografiche, suggerendo un forte legame con fattori ambientali e patologie predisponenti.
I dati epidemiologici chiave includono:
- rarità: il colangiocarcinoma rappresenta meno del 2% di tutte le neoplasie umane, con un’incidenza stimata di circa 1 caso su 100.000 persone.
- prevalenza: è il secondo tumore primario del fegato più comune dopo l’epatocarcinoma. Negli Stati Uniti si registrano circa 3.000 nuovi casi di colangiocarcinoma extraepatico all’anno.
- distribuzione geografica: l’incidenza è significativamente più alta in Asia (fino a 113 casi per 100.000 uomini) rispetto ai paesi occidentali, principalmente a causa della maggiore prevalenza di infezioni parassitarie epatiche;
- caratteristiche demografiche: la patologia si manifesta tipicamente nella sesta decade di vita o in pazienti di età superiore ai 50 anni, con una leggera predominanza nel sesso maschile.
Fattori di rischio
Diversi fattori di rischio sono stati chiaramente associati allo sviluppo del colangiocarcinoma ilare. Questi fattori condividono un meccanismo comune legato all’infiammazione cronica e al danno dell’epitelio biliare.
Caricamento…
Colangite Sclerosante Primitiva (CSP): è il fattore di rischio più consolidato nei paesi occidentali. La CSP è una condizione infiammatoria idiopatica che causa fibrosi e stenosi dei dotti biliari. L’incidenza di colangiocarcinoma nei pazienti con CSP varia dal 6% al 36% nel corso della vita, e la diagnosi di neoplasia avviene spesso entro 2,5 anni dalla diagnosi di CSP.
Patologie Biliari Croniche: le cisti biliari congenite, come le cisti del coledoco e la malattia di Caroli, sono associate a un rischio aumentato di trasformazione maligna. Anche la colelitiasi, in particolare l’epatolitiasi (calcoli intraepatici) e la coledocolitiasi (calcoli nel dotto biliare comune), e l’infiammazione cronica della cistifellea (colecistite) sono considerati fattori predisponenti.
Infezioni parassitarie: le infestazioni da parassiti epatici, in particolare Clonorchis sinensis e Opisthorchis viverrini, sono un fattore di rischio maggiore nel Sud-est asiatico. L’infezione, contratta attraverso il consumo di pesce crudo o poco cotto, causa un’infiammazione biliare cronica che può portare alla displasia e alla neoplasia.
Altre condizioni mediche: altre patologie che aumentano il rischio includono la cirrosi epatica, la malattia infiammatoria intestinale (spesso associata alla CSP) e la pancreatite cronica.
Esposizione a sostanze chimiche: l’esposizione industriale a sostanze come amianto e nitrosammine è stata collegata a un aumento del rischio. Anche l’uso in passato del mezzo di contrasto radiologico Thorotrast (diossido di torio) è un fattore di rischio noto.
L’identificazione di questi fattori è cruciale, ma la maggior parte dei casi di HC si verifica in modo sporadico, senza fattori di rischio noti. Questo sottolinea la necessità di una diagnosi tempestiva basata sulla manifestazione clinica.
Presentazione clinica
La presentazione clinica del colangiocarcinoma ilare è spesso tardiva e i sintomi iniziali sono aspecifici, il che rende il percorso diagnostico una fase critica per determinare la resecabilità del tumore e definire la strategia terapeutica più appropriata. La diagnosi tempestiva e accurata è la chiave per poter offrire un trattamento con intento curativo.
Il quadro sintomatologico è dominato dai segni di ostruzione biliare. Il sintomo di esordio più frequente è l’ittero (colorazione gialla della cute e delle sclere), che è tipicamente indolore. Altri sintomi comuni includono dolore addominale (localizzato nel quadrante superiore destro), perdita di peso inspiegabile, prurito intenso, affaticamento, urine scure e feci acoliche (color argilla). Meno frequentemente possono presentarsi nausea e febbre, quest’ultima spesso indicativa di colangite sovrapposta.
Valutazione diagnostica
Esami di laboratorio
La valutazione iniziale include esami ematochimici per valutare la funzionalità epatica e dosare i marcatori tumorali.
- Test di funzionalità epatica: mostrano tipicamente un pattern colestatico, con un aumento significativo della bilirubina coniugata (diretta) e degli enzimi di colestasi come la fosfatasi alcalina (ALP) e la gamma-glutamil transferasi (GGT). Le transaminasi (AST e ALT) possono essere lievemente elevate.
- Marcatori tumorali: i markers più utilizzati sono l’antigene carcino-embrionario (CEA) e l’antigene carboidratico 19-9 (CA 19-9). Sebbene non siano specifici per l’HC, possono supportare il sospetto diagnostico. Livelli molto elevati di CA 19-9 sono spesso associati a uno stadio più avanzato della malattia. La combinazione dei due marcatori ha una sensibilità dell’89% e una specificità dell’86% nel contesto di altre modalità diagnostiche. È importante notare, tuttavia, che livelli elevati possono essere riscontrati anche in condizioni benigne come l’infiammazione o l’ostruzione biliare, e pertanto non sono diagnostici in modo isolato.
Tecniche di Imaging
L’imaging gioca un ruolo centrale nella diagnosi, stadiazione e valutazione della resecabilità del colangiocarcinoma ilare.
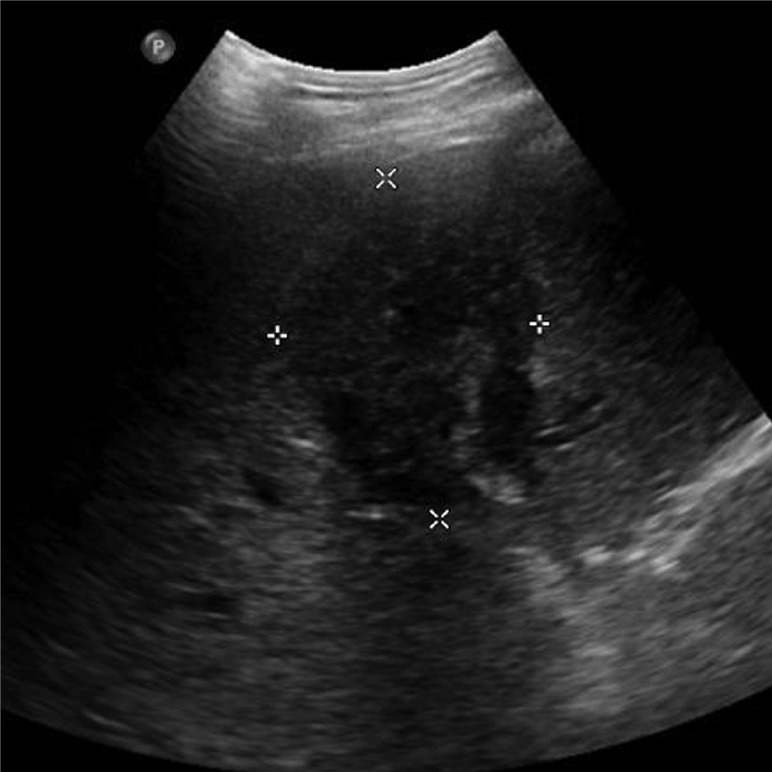
- Ecografia (US): rappresenta tipicamente la valutazione radiografica iniziale. È una tecnica non invasiva e a basso costo, molto efficace nel rilevare la dilatazione dei dotti biliari a monte dell’ostruzione. Tuttavia, la sua sensibilità nel localizzare con precisione il sito dell’ostruzione e nel definire l’estensione del tumore, in particolare l’invasione vascolare e linfonodale, è limitata.
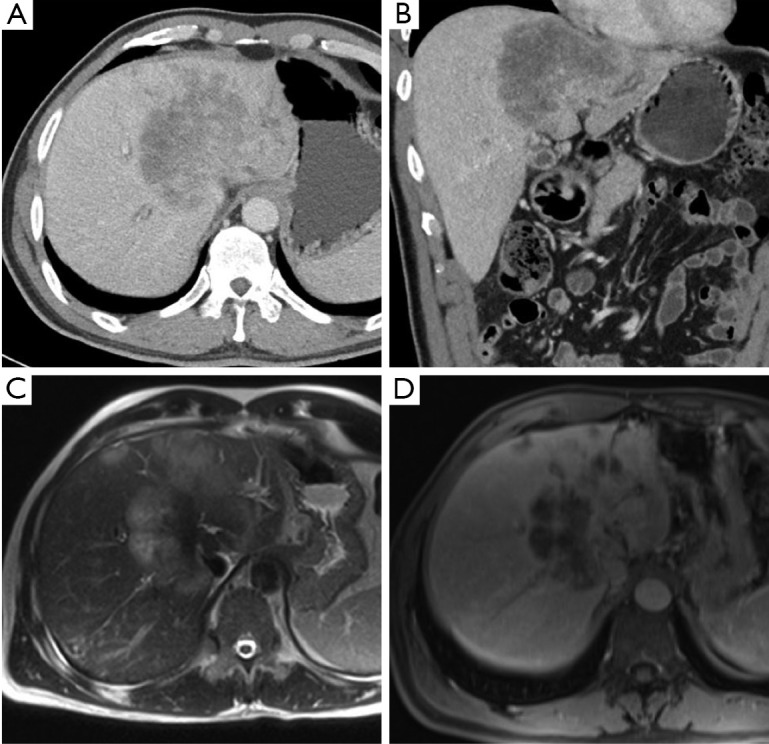
- Tomografia computerizzata (TC): la TC multidetettore con mezzo di contrasto è la modalità più utilizzata per la stadiazione e la valutazione della resecabilità, con un’accuratezza riportata tra il 60% e il 90%. Le scansioni in fase arteriosa e portale sono essenziali per delineare con precisione l’invasione dell’arteria epatica e della vena porta. I limiti della TC risiedono nella sua minore accuratezza nella valutazione del coinvolgimento linfonodale e nella rilevazione di piccole metastasi peritoneali.
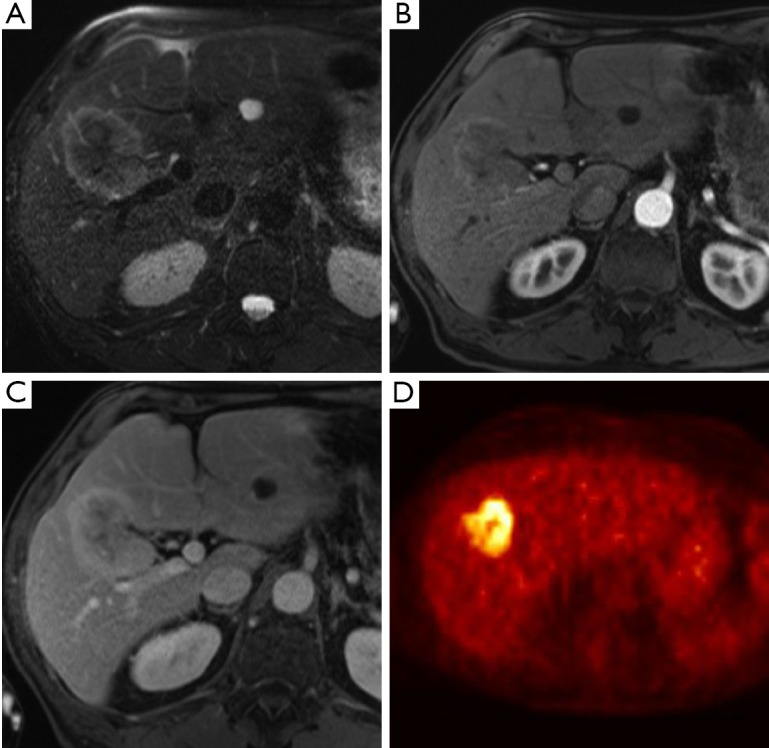
- Risonanza Magnetica (RM) e colangiopancreatografia a risonanza magnetica (CPRM): queste tecniche stanno guadagnando sempre più favore. La RM offre un’eccellente risoluzione di contrasto dei tessuti molli, mentre la CPRM fornisce una visualizzazione non invasiva e dettagliata dell’albero biliare, paragonabile alla colangiografia diretta. La combinazione di RM e CPRM ha un’accuratezza di circa l’80% nel predire la resecabilità ed è particolarmente vantaggiosa per la stadiazione biliare, definendo l’estensione del tumore lungo i dotti.
- PET/CT: il ruolo della tomografia a emissione di positroni (PET) con TC nella valutazione della resecabilità locale è limitato. Tuttavia, questa modalità è molto utile per rilevare metastasi a distanza e linfonodali non identificate da altre tecniche, con una specificità superiore all’80%. Il suo utilizzo può quindi prevenire laparotomie non necessarie in pazienti con malattia metastatica occulta.
Colangiografia diretta e biopsia
È fondamentale ottenere un’imaging cross-sezionale di alta qualità prima di qualsiasi intervento di drenaggio biliare per evitare artefatti infiammatori che possono complicare l’interpretazione e la stadiazione. La diagnosi definitiva di malignità richiede una conferma istologica o citologica.
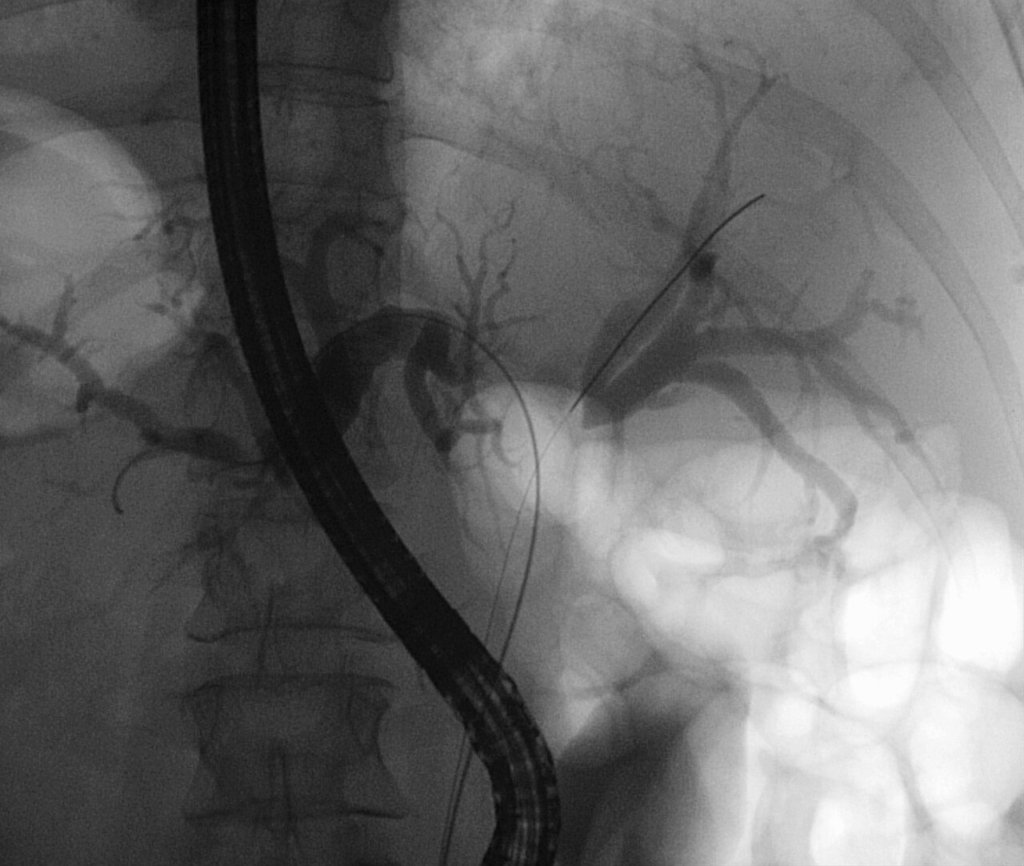
- Colangiopancreatografia Retrograda Endoscopica (ERCP) e Colangiografia Percutanea Transepatica (PTC): queste tecniche invasive hanno un duplice ruolo. Permettono una visualizzazione diretta dell’albero biliare per valutare l’estensione duttale del tumore e consentono il prelievo di campioni tissutali (brushing citologico, biopsia endobiliare). Inoltre, offrono la possibilità di un drenaggio biliare terapeutico tramite il posizionamento di stent. È importante sottolineare che una biopsia o un brushing negativo non esclude la diagnosi di colangiocarcinoma, data la natura sclerosante di molti di questi tumori.
- Biopsia con ago sottile (FNA): l’aspirazione con ago sottile per via transperitoneale sotto guida ecografica o TC è generalmente sconsigliata per le lesioni potenzialmente resecabili. Questa procedura è associata a un rischio significativo di disseminazione peritoneale delle cellule tumorali, che comprometterebbe l’intento curativo della chirurgia.
Una volta completato l’iter diagnostico, i risultati vengono integrati nei sistemi di stadiazione per classificare accuratamente la malattia e guidare il piano terapeutico.
Caratteristiche patologiche
Il colangiocarcinoma ilare viene classificato in base all’aspetto macroscopico e alle caratteristiche microscopiche.
| Tipo Macroscopico | Caratteristiche Microscopiche |
|---|---|
| Sclerosante: è il sottotipo più comune. Si presenta come un ispessimento anulare della parete duttale con infiltrazione sia longitudinale che radiale, causando una marcata reazione fibrotica (desmoplastica). Tende a invadere i tessuti neurali periduttali e le strutture vascolari maggiori dell’ilo. | Adenocarcinoma: oltre il 95% dei tumori sono adenocarcinomi, che vanno da ben a scarsamente differenziati in base alla formazione di strutture ghiandolari. |
| Nodulare: si manifesta come una massa solida e irregolare che protrude nel lume del dotto. Spesso coesistono caratteristiche del tipo sclerosante, configurando un quadro nodulare-sclerosante. | Invasione: l’invasione linfatica e perineurale è una caratteristica comune e precoce, associata a un’elevata probabilità di recidiva locale e metastasi linfonodali. |
| Papillare: è il sottotipo meno comune, caratterizzato da una crescita intraluminale soffice e friabile. Ha una minore tendenza all’invasione transmurale e una prognosi significativamente migliore rispetto agli altri tipi. | Lesioni premaligne: la neoplasia biliare intraepiteliale (BiIN) è considerata la lesione precursore dell’adenocarcinoma invasivo. La BiIN-3 rappresenta il carcinoma in situ. |
Sistemi di stadiazione
Diversi sistemi di stadiazione vengono utilizzati per classificare il colangiocarcinoma ilare, ciascuno con specifici punti di forza e limiti.
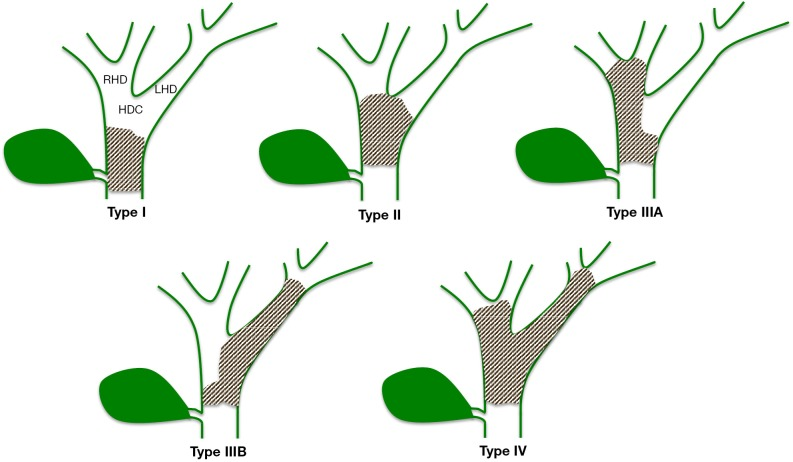
- Classificazione di Bismuth-Corlette: si basa esclusivamente sulla localizzazione anatomica del tumore per guidare la pianificazione chirurgica.
- Tipo I: tumore limitato al dotto epatico comune, distale alla confluenza.
- Tipo II: tumore che raggiunge e coinvolge la confluenza dei dotti epatici, senza estendersi ai dotti principali.
- Tipo IIIa/IIIb: tumore che coinvolge la confluenza e si estende nel dotto epatico principale destro (IIIa) o sinistro (IIIb).
- Tipo IV: tumore che coinvolge la confluenza e si estende bilateralmente ai dotti epatici secondari. Ha un valore prognostico limitato perché non tiene conto dell’invasione vascolare, del coinvolgimento linfonodale o delle metastasi a distanza.
- Classificazione del Memorial Sloan Kettering Cancer Center (MSKCC): rappresenta un’evoluzione che integra il coinvolgimento della vena porta e la presenza di atrofia lobare epatica. Questi parametri aggiuntivi forniscono una valutazione più accurata della resecabilità locale e si correlano meglio con la sopravvivenza.
- Stadiazione AJCC (American Joint Committee on Cancer): è il sistema più utilizzato, basato sul sistema TNM (Tumore, Nodi, Metastasi). Include l’invasione vascolare, il coinvolgimento linfonodale e le metastasi a distanza. Sebbene sia il più completo dal punto di vista prognostico, è principalmente un sistema di stadiazione post-operatorio.
- Stadiazione per stadi (da 0 a IVB): derivata dal sistema TNM, questa classificazione descrive la progressione della malattia in stadi clinici. Ad esempio, lo Stadio II indica una diffusione ai tessuti adiposi circostanti o al fegato; lo Stadio IIIC indica il coinvolgimento di 1-3 linfonodi; lo Stadio IVB rappresenta la presenza di metastasi a distanza.
Nella pratica clinica, questi sistemi vengono utilizzati in modo complementare. La classificazione di Bismuth-Corlette offre una mappa anatomica essenziale per la pianificazione chirurgica. Il sistema MSKCC aggiunge dettagli cruciali sull’invasione vascolare e sull’atrofia epatica, affinando la valutazione della resecabilità locale. Infine, la stadiazione AJCC/TNM fornisce la valutazione prognostica definitiva dopo l’intervento chirurgico, guidando le decisioni sulle terapie adiuvanti e sul follow-up.
Strategie di gestione e trattamento
La gestione del colangiocarcinoma ilare è complessa e richiede un approccio multimodale e multidisciplinare. La resezione chirurgica con margini negativi (R0) rimane l’unica opzione potenzialmente curativa in grado di offrire una sopravvivenza a lungo termine. Tuttavia, a causa della presentazione spesso tardiva e dell’estensione locale della malattia, solo una minoranza di pazienti risulta candidabile a un intervento chirurgico al momento della diagnosi.
Ottimizzazione Pre-operatoria
Prima di un intervento di chirurgia maggiore come l’epatectomia estesa, è fondamentale ottimizzare le condizioni del fegato per ridurre il rischio di complicanze post-operatorie.
- Drenaggio biliare pre-operatorio (PBD): l’uso del PBD rimane un argomento di dibattito clinico. Sebbene sia indicato per ridurre i livelli di bilirubina nei pazienti itterici, le procedure di drenaggio possono aumentare il rischio di complicanze infettive peri-operatorie. L’evidenza attuale suggerisce che il PBD sia vantaggioso e raccomandato per i pazienti con un futuro residuo epatico (FLR, Future Liver Remnant) di volume ridotto (<30-40%), poiché il beneficio di migliorare la funzione epatica supera i rischi. Al contrario, nei pazienti con un FLR adeguato (>40%), i rischi associati al PBD, in particolare le infezioni, superano i benefici, e pertanto il drenaggio non è raccomandato di routine.
- Embolizzazione della vena porta (PVE): quando il volume del futuro residuo epatico (FLR) previsto dopo l’epatectomia è insufficiente (generalmente inferiore al 30-40% del volume epatico totale), si ricorre alla PVE. Questa procedura occlude il ramo portale del fegato che verrà resecato, reindirizzando il flusso sanguigno verso il fegato rimanente e inducendone l’ipertrofia. Ciò permette di aumentare il volume del FLR, riducendo significativamente il rischio di insufficienza epatica post-operatoria.
Resezione Chirurgica
L’obiettivo primario dell’intervento chirurgico è ottenere una resezione R0 (assenza di tumore residuo microscopico).
- Procedura standard: l’intervento standard consiste in un’epatectomia maggiore (destra o sinistra estesa) associata alla resezione del dotto biliare extraepatico, alla resezione del lobo caudato (per la sua stretta vicinanza anatomica e il drenaggio biliare diretto) e a una linfoadenectomia regionale en bloc. L’escissione locale del solo dotto biliare deve essere evitata, poiché è associata a un’altissima incidenza di margini positivi e a una sopravvivenza inferiore.
- Resezione vascolare: il ruolo della resezione vascolare è controverso. La resezione e ricostruzione della vena porta (PVR) può essere eseguita in centri ad alto volume di esperienza per ottenere margini R0 in pazienti con invasione venosa, senza compromettere la sopravvivenza a lungo termine rispetto ai casi senza resezione. Al contrario, la resezione dell’arteria epatica non è raccomandata di routine, in quanto associata a un’elevata morbilità e mortalità senza un chiaro beneficio in termini di sopravvivenza.
Nonostante l’aggressività chirurgica, i risultati rimangono modesti. I tassi di sopravvivenza a 5 anni dopo la resezione variano dal 10% al 40%. I tassi di recidiva sono elevati, attestandosi tra il 50% e il 70%, anche dopo una resezione R0. I progressi nelle tecniche chirurgiche e nella gestione peri-operatoria, come l’uso routinario dell’epatectomia e della PVE, hanno tuttavia portato a una riduzione della morbilità e a un miglioramento della sopravvivenza nel tempo.
Trapianto di Fegato (OLT)
Il trapianto ortotopico di fegato (OLT) è un’opzione terapeutica per un gruppo altamente selezionato di pazienti con malattia localmente avanzata ma non resecabile, senza evidenza di metastasi linfonodali o a distanza.
Il protocollo più noto prevede una terapia neoadiuvante rigorosa con chemioradioterapia, seguita da una laparotomia di stadiazione per escludere metastasi. I criteri di inclusione sono stringenti e includono tumori di diametro inferiore a 3 cm, assenza di metastasi intraepatiche o extraepatiche e diagnosi istologica ottenuta senza biopsia transperitoneale.
Nei pazienti che completano il protocollo, i risultati sono incoraggianti. Studi multicentrici hanno riportato una sopravvivenza libera da recidiva a 5 anni del 65%, un risultato superiore a quello ottenibile con la sola chirurgia resettiva per tumori di stadio simile.
Terapie non chirurgiche e palliative
Per i pazienti con malattia non resecabile o metastatica, e nel contesto adiuvante, sono disponibili diverse opzioni terapeutiche.
- Chemioterapia: la combinazione di gemcitabina e cisplatino è considerata lo standard di cura per la malattia in stadio avanzato. Nel contesto adiuvante (post-chirurgico), i risultati sono stati contrastanti. Lo studio BILCAP ha mostrato un beneficio in termini di sopravvivenza con l’uso della capecitabina adiuvante nell’analisi per protocollo; tuttavia, l’analisi primaria per intenzione al trattamento (intention-to-treat) non ha raggiunto la significatività statistica (p=0.097), portando all’adozione della capecitabina come opzione standard in molti centri sulla base dell’analisi secondaria.
- Radioterapia: viene utilizzata principalmente nel contesto adiuvante, spesso in combinazione con la chemioterapia (chemioradioterapia), per migliorare il controllo locale della malattia, in particolare nei pazienti con margini di resezione positivi (R1).
- Terapie target e immunoterapia: rappresentano nuove frontiere per la malattia avanzata. Farmaci mirati come gli inibitori di FGFR e IDH hanno mostrato efficacia in sottogruppi di pazienti con specifiche alterazioni molecolari. Anche gli inibitori del checkpoint immunitario sono un’opzione in fase di studio e per casi selezionati.
- Terapia palliativa: per i pazienti non candidabili a trattamenti curativi, l’obiettivo è migliorare la qualità della vita. Il drenaggio biliare tramite il posizionamento di stent endoscopici o percutanei è fondamentale per alleviare l’ittero e il prurito. La terapia fotodinamica (PDT), in aggiunta allo stenting, può aumentare la sopravvivenza di 2-3 mesi distruggendo selettivamente il tessuto tumorale che ostruisce il dotto.
Prognosi e fattori prognostici
La prognosi del colangiocarcinoma ilare è generalmente sfavorevole, anche nei casi trattati con intento curativo. La natura aggressiva del tumore, la sua tendenza alla recidiva locale e a distanza, e la complessità del trattamento contribuiscono a tassi di sopravvivenza complessivamente bassi. È quindi fondamentale identificare i fattori prognostici che possono aiutare a stratificare il rischio e a guidare le decisioni terapeutiche.
Now loading…
Secondo i dati del National Cancer Institute (NCI) degli Stati Uniti, che raggruppano i tumori dei dotti biliari extraepatici, i tassi di sopravvivenza relativa a 5 anni sono i seguenti:
- sopravvivenza complessiva a 5 anni: 9%;
- malattia localizzata: 23% (il tumore è confinato ai dotti biliari);
- malattia regionale: 9% (il tumore si è diffuso ai linfonodi o ai tessuti vicini);
- malattia a distanza: 3% (il tumore si è diffuso a organi distanti come polmoni o ossa).
È importante sottolineare che queste cifre sono stime basate su dati storici di una vasta popolazione e non possono predire l’esito per un singolo paziente. La situazione individuale può variare in base a molteplici fattori, tra cui l’età, la salute generale del paziente e la risposta al trattamento.
I principali fattori prognostici che influenzano negativamente la sopravvivenza sono ben definiti e sono strettamente legati alle caratteristiche del tumore e all’efficacia del trattamento chirurgico:
- Stato dei margini di resezione: l’ottenimento di una resezione con margini chirurgici negativi (R0) è il fattore prognostico più importante per la sopravvivenza a lungo termine. Una resezione R1 (margini microscopicamente positivi) è associata a una prognosi significativamente peggiore.
- Metastasi linfonodali: la presenza di cellule tumorali nei linfonodi regionali è un potente indicatore prognostico negativo.
- Grado del tumore: tumori scarsamente differenziati (alto grado) hanno un comportamento più aggressivo e una prognosi peggiore rispetto a quelli ben differenziati.
- Invasione linfovascolare: l’invasione dei vasi linfatici o sanguigni da parte del tumore è associata a un rischio più elevato di recidiva e di metastasi a distanza.
Conclusioni
In sintesi, il colangiocarcinoma ilare (tumore di Klatskin) si conferma una malattia rara ma estremamente aggressiva, caratterizzata da una prognosi difficile e da sfide gestionali significative. La sua localizzazione anatomica critica, la tendenza all’infiltrazione locale precoce e la presentazione spesso tardiva contribuiscono a limitare le opzioni terapeutiche curative.
È stato ribadito che la resezione chirurgica con margini negativi (R0), spesso richiedente un’epatectomia maggiore e una complessa ricostruzione biliare, rappresenta l’unica possibilità di sopravvivenza a lungo termine. Tuttavia, anche nei pazienti che ricevono questo trattamento radicale, i tassi di recidiva rimangono elevati, evidenziando la natura sistemica e la biologia aggressiva di questa neoplasia. Le opzioni per i pazienti con malattia non resecabile, sebbene in evoluzione con l’avvento di terapie mirate e del trapianto di fegato in casi altamente selezionati, offrono ancora benefici limitati.
In conclusione, la gestione ottimale di questa complessa patologia non può prescindere da un approccio multidisciplinare, che richiede una stretta e coordinata collaborazione tra chirurghi epatobiliari, oncologi medici, radiologi, gastroenterologi interventisti e radioterapisti. Solo attraverso una valutazione integrata e la personalizzazione del piano terapeutico è possibile sperare di migliorare i risultati e la qualità della vita per i pazienti affetti da colangiocarcinoma ilare.
Fonti:
- Cholangiocarcinoma (bile duct cancer);
- Hilar cholangiocarcinoma: diagnosis, treatment options, and management – PMC;
- Klatskin Tumors (Hilar Cholangiocarcinoma);
- The Landmark Series: Hilar Cholangiocarcinoma – PMC;
- Tumore di Klatskin – Wikipedia;
- Hilar cholangiocarcinoma: pathology and tumor biology – PubMed.