Il flusso sanguigno cerebrale e il metabolismo sono processi fisiologici strettamente interconnessi. Una variazione nell’attività funzionale del cervello si traduce, infatti, in un corrispondente cambiamento nel suo apporto di sangue (perfusione). La medicina nucleare sfrutta questo principio fondamentale attraverso studi di perfusione cerebrale che utilizzano traccianti radioattivi lipofili, in grado di attraversare la barriera emato-encefalica.
Queste indagini sono estremamente preziose per identificare anomalie regionali del flusso ematico, come quelle causate da ictus ischemici, e per valutare le alterazioni dell’attività neuronale in condizioni come l’epilessia e i traumi cranici.
Un campo di applicazione in forte crescita e dalle notevoli potenzialità è quello dello studio delle patologie psichiatriche, dove queste tecniche offrono una visione funzionale unica.
Per visualizzare il sistema nervoso centrale, vengono impiegati diversi radiofarmaci. I più comuni in ambito SPECT sono i composti marcati con Tecnezio-99m, come 99mTc-HMPAO, che misurano la perfusione sanguigna. Per la tomografia a emissione di positroni (PET), il tracciante per eccellenza è il Fluorodesossiglucosio marcato con Fluoro-18 (18F-FDG), uno zucchero radioattivo che viene metabolizzato dalle cellule, fornendo una mappa dettagliata del consumo di glucosio e, quindi, dell’attività metabolica e funzionale dei neuroni. In casi più specifici, come lo studio del liquor, può essere utilizzato 111In-DTPA.
Le applicazioni della medicina nucleare in neurologia e psichiatria sono vastissime e in continua evoluzione. Le immagini funzionali ottenute con SPECT e PET integrano le informazioni morfologiche della risonanza magnetica (MRI) e della tomografia computerizzata (CT), rispondendo a quesiti clinici specifici.
Indice:
- Demenze
- Morte cerebrale
- Epilessia e localizzazione focus epilettogeni
- Tumori cerebrali
- Parkinson e parkinsonismi
- Alterazioni del liquido cefalorachidiano (CSF)
Demenze
La demenza non è una condizione unica, ma un termine ombrello che racchiude diverse patologie, ognuna con caratteristiche proprie. Dal punto di vista clinico e per immagini, è utile classificarle in tre macro-categorie:
- le demenze frontotemporali (che colpiscono i lobi frontali e temporali, come la malattia di Pick e l’afasia progressiva primaria);
- le demenze posteriori o corticali (che interessano le regioni parietali e occipitali, come il morbo di Alzheimer e la demenza a corpi di Lewy, quest’ultima spesso associata al morbo di Parkinson);
- le demenze vascolari (causate da problemi di circolazione sanguigna nel cervello).
La medicina nucleare, attraverso tecniche come la SPECT cerebrale (che misura il flusso sanguigno regionale, rCBF) e la PET con FDG (che valuta il metabolismo del glucosio, rCGM), riveste un ruolo fondamentale nel distinguere queste diverse forme. Sebbene i meccanismi misurati (flusso e metabolismo) siano diversi, le due metodiche rivelano pattern scintigrafici molto simili per ogni tipo di demenza, agendo come una “finestra” sull’attività funzionale del cervello.
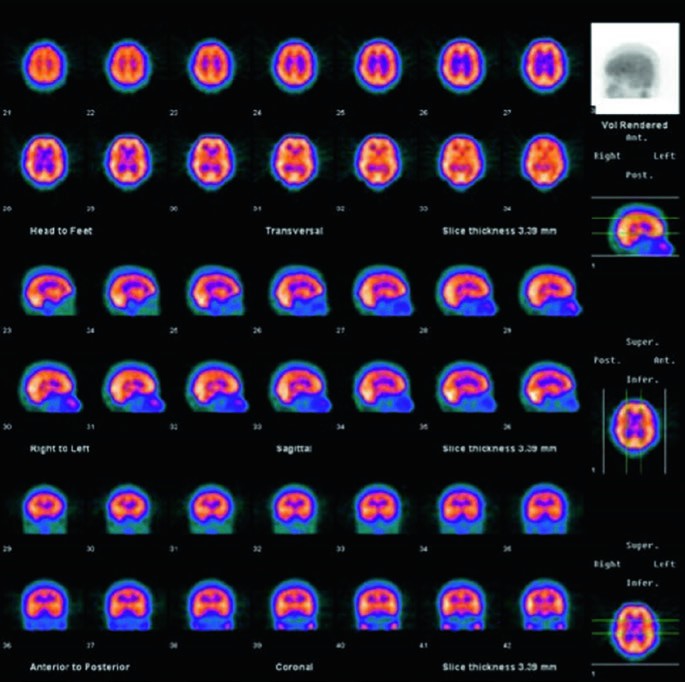
Un esame normale, sia SPECT che PET, mostrerà un’immagine uniforme e simmetrica del consumo energetico cerebrale, senza aree di ipoperfusione o ipometabolismo significative.
Caricamento....
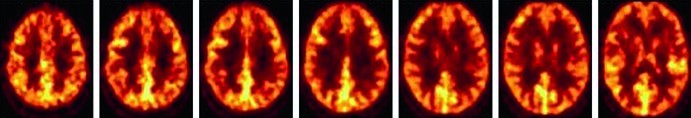
Il Morbo di Alzheimer, la forma di demenza degenerativa progressiva più comune, presenta un’impronta caratteristica che la medicina nucleare è in grado di identificare con grande precisione. Il quadro tipico mostra una riduzione generalizzata del flusso sanguigno e del metabolismo, ma con un’accentuazione marcata del deficit nelle regioni posteriori temporo-parietali bilaterali e nella corteccia cingolata posteriore.
Al contrario, aree come il talamo, i nuclei della base (striato) e la corteccia sensomotoria rimangono relativamente risparmiate nelle fasi iniziali della malattia. I lobi frontali tendono a essere coinvolti in una fase più avanzata del decorso patologico. Questo pattern distintivo permette di differenziare l’Alzheimer da altre demenze con un’accuratezza molto elevata, supportando una diagnosi precoce e un approccio terapeutico più mirato.
Le linee guida internazionali più recenti riconoscono sempre di più il valore della PET FDG e dell’Amiloide-PET (un tracciante specifico per le placche beta-amiloidi) come biomarcatori cruciali per una diagnosi precisa già nelle fasi prodromiche della malattia.
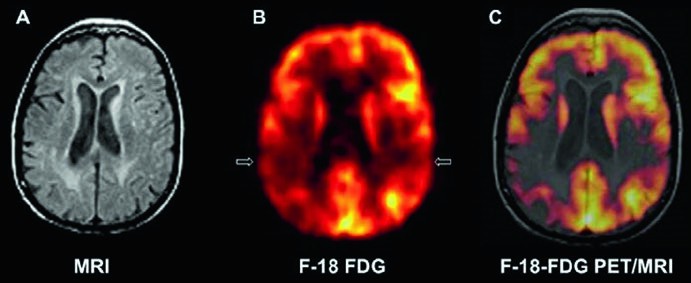
La MRI (a) mostra alterazioni ischemiche croniche dei piccoli vasi e una lieve atrofia diffusa, senza un pattern specifico che possa essere diagnostico per la malattia di Alzheimer.
La PET FDG (b) evidenzia una riduzione dell’attività nelle regioni temporali posteriori e parietali bilateralmente, con un coinvolgimento più marcato a destra rispetto a sinistra.
La PET FDG fusa con la MRI in T1 (c) mostra che, nelle aree di ridotto assorbimento di FDG, non è presente un’atrofia cerebrale sproporzionata rispetto ad altre aree del cervello tale da indicare che la riduzione dell’assorbimento sia effetto dell’atrofia. Pertanto, la riduzione dell’assorbimento di può essere attribuita a una diminuzione dell’attività metabolica neuronale, conseguente a un danno neuronale riconducibile all’amiloidopatia della malattia di Alzheimer.
Morte cerebrale
La morte rappresenta l’evento biologico irreversibile che sancisce la cessazione permanente delle funzioni critiche dell’organismo nel suo insieme. Dal punto di vista neurologico, questa condizione coincide con la morte encefalica, definita come la perdita irreversibile di tutte le funzioni dell’encefalo, inclusi il cervello e il tronco encefalico. Il concetto poggia sul principio che è il cervello l’organo indispensabile per integrare le funzioni vitali del corpo; la sua cessazione attività equivale, quindi, alla morte dell’individuo. Sebbene questo sia un principio giuridico e medico largamente accettato a livello internazionale, le specificità legislative e culturali possono variare da paese a paese.
La definizione di “morte encefalica” (o “coma irreversibile“) fu formalizzata per la prima volta nel 1959, in un’epoca antecedente alla pratica diffusa dei trapianti d’organo, sottolineando come si tratti di un concetto clinico distinto e autonomo.
La diagnosi di morte encefalica rimane, prima di tutto, un atto clinico. Essa viene posta dopo aver accertato l’assenza di tutte le funzioni cerebrali e del tronco encefalico in un paziente in coma apneico, escludendo al contempo condizioni potenzialmente reversibili come ipotermia grave, shock o intossicazione da farmaci sedativi. Tuttavia, in molti contesti, è richiesto o fortemente raccomandato un test strumentale di conferma per documentare in modo oggettivo e inequivocabile l’irreversibilità della condizione.
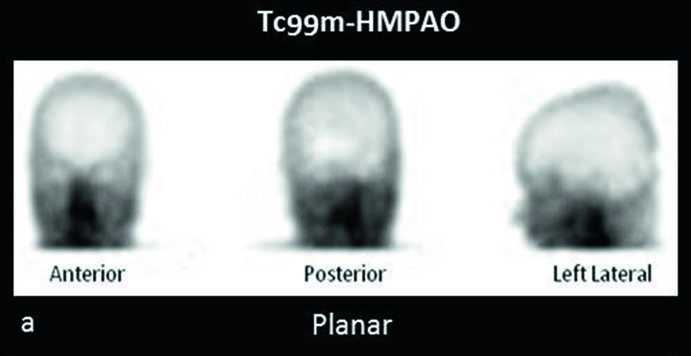
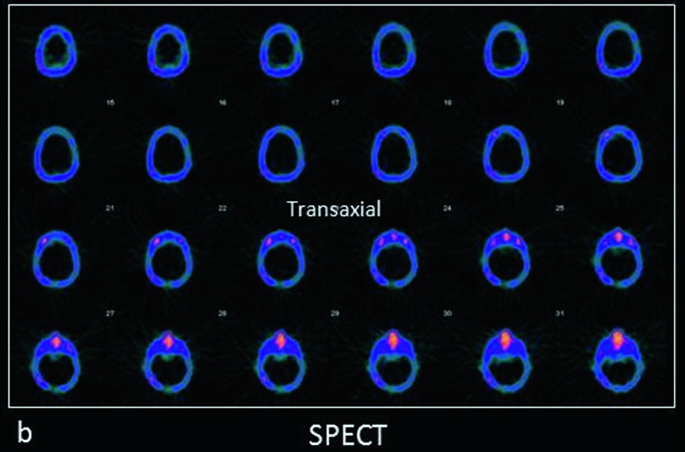
Tra queste metodiche di conferma, la scintigrafia cerebrale ha assunto un ruolo di primaria importanza, diventando in molte nazioni, inclusi gli Stati Uniti e gran parte d’Europa, il principale referto legale a supporto della diagnosi. Questo esame si basa su un principio fisiologico fondamentale: nella morte encefalica, la pressione intracranica supera quella arteriosa, causando l’arresto completo della circolazione sanguigna nel cervello.
La procedura utilizza un radiofarmaco lipofilo, come il 99mTc-HMPAO o il 99mTc-ECD, in grado di attraversare la barriera emato-encefalica solo se essa è integra e se esiste un flusso sanguigno attivo. In un paziente con morte encefalica, il tracciante non perfonde il parenchima cerebrale. L’immagine risultante mostrerà quindi il “segno del cranio vuoto” (empty skull sign): un’assenza completa di uptake del radiofarmaco all’interno della volta cranica, con la persistente visualizzazione del flusso sanguigno extracranico nei vasi della faccia e del cuoio capelluto (il “segno del cappuccio” o hot nose sign). Questo reperto è considerato prova definitiva dell’assenza di perfusione cerebrale.
Rispetto all’angiografia cerebrale con mezzo di contrasto iodato, un tempo considerata il gold standard, la scintigrafia offre il vantaggio di essere meno invasiva, più rapida da eseguire e di non richiedere l’uso di mezzi di contrasto potenzialmente nefrotossici. Per questi motivi, è diventata la tecnica di imaging di conferma preferita nella maggior parte dei protocolli internazionali.
Epilessia e localizzazione focus epilettogeni
L’epilessia è un disturbo neurologico caratterizzato dalla ricorrenza di crisi convulsive, che possono manifestarsi sia in presenza di una patologia cerebrale identificabile sia in assenza di essa. Questa condizione interessa approssimativamente lo 0.5% della popolazione globale, con un esordio che, sebbene prevalente in età pediatrica, può verificarsi in qualsiasi fase della vita.
La base fisiopatologica di una crisi epilettica risiede in un focus neuronale che, a causa di un’anomala attività elettrochimica, inizia a scaricare in modo eccessivo e sincrono. Questa scarica anomala si propaga poi in maniera incontrollata attraverso le reti cerebrali, generando le manifestazioni cliniche della crisi. L’elettroencefalogramma (EEG) rappresenta lo strumento primario per rilevare questa attività elettrica aberrante.
Tuttavia, quando le crisi sono farmacoresistenti e si valuta un approccio chirurgico, la localizzazione precisa della zona da cui originano le crisi (focolaio epilettogeno) diventa fondamentale. In questi casi complessi, la medicina nucleare offre un contributo diagnostico insostituibile, integrando le informazioni dell’EEG.
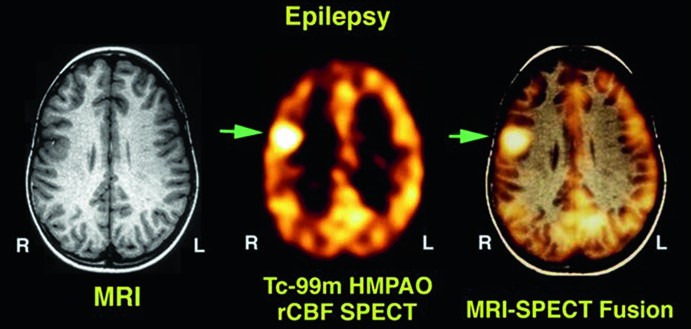
La SPECT cerebrale con radiofarmaci come il 99mTc-HMPAO gioca un ruolo cruciale se eseguita durante o immediatamente dopo una crisi epilettica (stato ittale). In questa fase, il focolaio epilettogeno presenta un metabolismo e un flusso sanguigno enormemente aumentati. Il radiofarmaco, captato avidamente dalle cellule cerebrali iperattive, “fotografa” questa iperperfusione, rendendo il focus chiaramente visibile come un’area di intensa ipercaptazione.
Al contrario, la PET con FDG viene tipicamente eseguita tra una crisi e l’altra (fase interittale). In questo periodo, il focolaio epilettogeno è spesso ipometabolico, ovvero presenta un consumo di glucosio ridotto rispetto al tessuto cerebrale sano circostante. La PET FDG è quindi eccellente nel delineare un’area di ipocaptazione, che corrisponde alla zona di cervello disfunzionale da cui originano le crisi.
L’impiego combinato di queste due tecniche: la SPECT ictale per “catturare” la crisi in atto e la PET FDG interittale per identificare il tessuto cronicamente alterato, fornisce ai neurologi e ai neurochirurghi informazioni complementari e estremamente preziose. Questo duplice approccio permette di localizzare con precisione il focus epilettogeno in quei pazienti complessi in cui la risonanza magnetica (MRI) e l’EEG da soli non forniscono una localizzazione univoca, aprendo la strada a un trattamento chirurgico potenzialmente risolutivo.
Tumori cerebrali
Il trattamento dei tumori cerebrali maligni di alto grado, come il glioblastoma, rimane una sfida clinica di notevole complessità. Una delle difficoltà principali nel management post-terapeutico di questi pazienti risiede nell’interpretazione delle immagini di follow-up. I tradizionali esami di imaging morfologico, come la Tomografia Computerizzata (TC) e la Risonanza Magnetica (MRI), mostrano infatti reperti spesso ambigui: sia una recidiva di tumore vitale che la necrosi cerebrale indotta dalla radio-chemioterapia, infatti, possono presentare un effetto massa, edema perilesionale e un enhancement dopo somministrazione di mezzo di contrasto.
È proprio in questo cruciale dilemma diagnostico che l’imaging metabolico della medicina nucleare dimostra tutto il suo valore, fornendo informazioni funzionali che integrano e superano i limiti della sola anatomia. Il principio fisiopatologico su cui si basa è chiaro: un trattamento efficace sopprime l’attività metabolica e la proliferazione cellulare tumorale, mentre un trattamento inefficace o una recidiva sono caratterizzati da una ripresa della crescita e da un’aumentata attività metabolica.
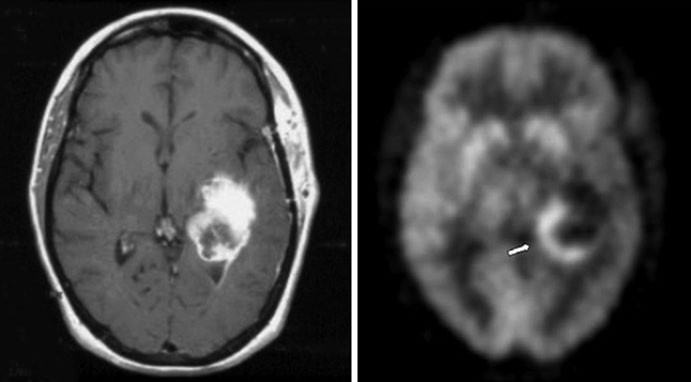
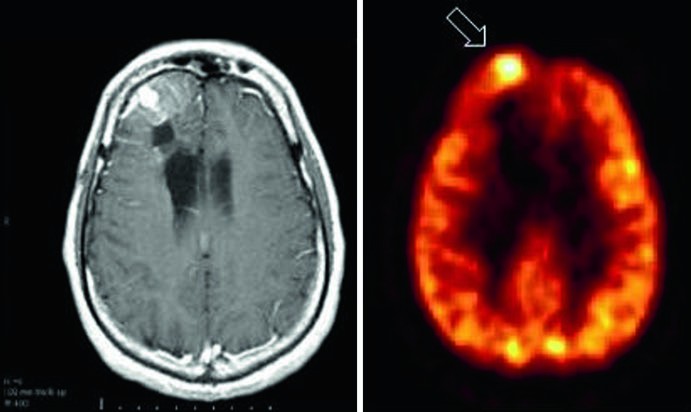
La PET con FDG è stata a lungo la metodica di riferimento per questa distinzione. Le cellule tumorali maligne, infatti, sono caratterizzate da un avido consumo di glucosio (fenomeno noto come effetto Warburg). Una lesione ipermetabolica, che quindi capta intensamente il FDG, è altamente suggestiva per una recidiva tumorale vitale. Al contrario, la necrosi tissutale o la pseudoprogressione (una reazione infiammatoria post-radioterapia che mima una progressione) sono tipicamente ipometaboliche, mostrando un’assenza di uptake significativo del tracciante.
Oltre a questa cruciale discriminazione, il grado di captazione del FDG (SUVmax) fornisce anche preziose informazioni prognostiche e sulla gradazione tumorale. Un elevato metabolismo glucidico si correla infatti con un grado istologico più alto e un’aggressività biologica maggiore, spesso permettendo di prevedere l’outcome del paziente in modo più accurato rispetto alle sole caratteristiche morfologiche della TC o della MRI.
Negli ultimi anni, l’armamentario diagnostico si è ulteriormente arricchito con l’avvento di traccianti PET più specifici, come gli analoghi degli aminoacidi (es. MET-DOPA, FET). Questi radiofarmaci offrono un elevato contrasto tra il tessuto tumorale e il parenchima cerebrale sano, che normalmente ha un basso uptake aminoacidico, migliorando ulteriormente l’accuratezza nella pianificazione dei trattamenti e nel monitoraggio della risposta terapeutica.
Parkinson e parkinsonismi
Le sindromi parkinsoniane costituiscono un gruppo eterogeneo di disturbi del movimento, accomunati dalla presenza di bradicinesia (lentezza dei movimenti) associata ad almeno uno dei seguenti sintomi cardinali: tremore a riposo, rigidità muscolare e instabilità posturale. La corretta classificazione di queste sindromi è fondamentale per una prognosi e un trattamento appropriati.
Dal punto di vista eziologico, è possibile distinguere tre grandi categorie:
Caricamento….
- le forme neurodegenerative, come il Morbo di Parkinson idiopatico (PD), la Paralisi Sopranucleare Progressiva (PSP), l’Atrofia Multi-Sistemica (MSA), la Demenza a Corpi di Lewy (DLB) e la Degenerazione Corticobasale (CBD);
- le forme non neurodegenerative, come il parkinsonismo psicogeno, quello indotto da farmaci (un effetto collaterale comune di alcuni neurolettici), il tremore distonico e la distonia DOPA-responsiva;
- forme secondarie a cause vascolari, traumatiche o tossiche.
Il Morbo di Parkinson idiopatico, la forma più comune, è una patologia neurodegenerativa cronica e progressiva. La sua base fisiopatologica risiede nella progressiva riduzione e degenerazione dei neuroni pigmentati della substantia nigra nel mesencefalo, che secernono dopamina. Un marcatore patologico distintivo è la formazione di inclusioni proteiche intracellulari, chiamate Corpi di Lewy.
Proprio il sistema dopaminergico nigro-striatale è il bersaglio della medicina nucleare per la diagnosi differenziale. Il radiofarmaco I-123 Ioflupane (commercialmente noto come DaTSCAN™) è un analogo della cocaina che si lega selettivamente ai trasportatori della dopamina (DaT) presenti a livello presinaptico nei neuroni dello striato. Queste proteine transmembrana hanno la funzione di recuperare la dopamina rilasciata nello spazio sinaptico per riciclarla.
Nelle sindrome parkinsoniane neurodegenerative, la perdita di questi neuroni dopaminergici comporta una riduzione del numero di trasportatori disponibili a legare il radiofarmaco.
La scintigrafia DaTSCAN è, ad oggi, l’unico esame di medicina nucleare in vivo approvato per la conferma diagnostica nei sospetti casi di sindrome parkinsoniana. L’esame permette di visualizzare l’integrità del sistema nigro-striatale: un pattern normale mostra due simmetriche e ben definite aree di captazione a forma di “virgola” nei nuclei della base; in caso di PD o di altro parkinsonismo neurodegenerativo, si osserva invece una riduzione o un’assenza asimmetrica della captazione, con un tipico pattern a “punto e virgola” o a “farfalla“.
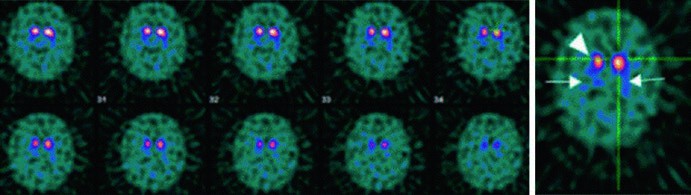
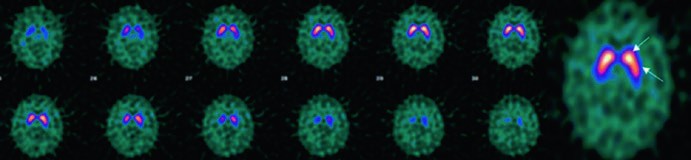
L’interpretazione visiva delle immagini da parte di un medico nucleare esperto è generalmente sufficiente per una diagnosi accurata. Tuttavia, un’analisi semiquantitativa computerizzata, che calcola il rapporto di binding striatale, può aumentare ulteriormente l’accuratezza diagnostica, soprattutto nei casi borderline o atipici. Questo esame è diventato uno strumento indispensabile per distinguere il tremore essenziale (che mostra un DaTSCAN normale) dal parkinsonismo e per supportare la diagnosi precoce, spesso prima che il quadro clinico sia completamente conclamato.
Caricamento….
Alterazioni del liquido cefalorachidiano (CSF)
Il liquido cefalorachidiano (CSF) è un componente essenziale del sistema nervoso centrale, agendo principalmente come cuscino meccanico per proteggere encefalo e midollo spinale. Con un volume totale di circa 150 ml, questo fluido viene prodotto in modo continuativo dai plessi corioidei al ritmo notevole di 500 ml al giorno, il che implica che viene completamente rinnovato più volte nelle 24 ore.
Il suo riassorbimento avviene a livello dei villi aracnoidei e delle granulazioni del Pacchioni, strutture specializzate che drenano il CSF nel seno sagittale superiore, un grande vaso venoso intracranico. Quando questo delicato equilibrio tra produzione e riassorbimento viene alterato, si possono verificare condizioni patologiche. Un’ostruzione meccanica all’interno del sistema ventricolare o un’insufficienza dei meccanismi di assorbimento, infatti, portano a un accumulo di liquido e a una conseguente dilatazione anomala dei ventricoli cerebrali, condizione nota come idrocefalo, associata a disturbi neurologici spesso severi.
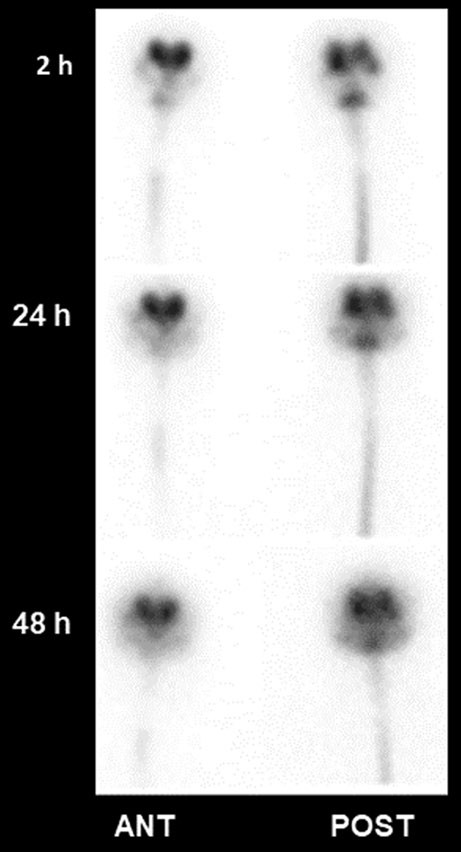
La medicina nucleare offre una metodica unica per valutare dinamicamente la circolazione del CSF: la cisternografia radioisotopica.
Questo esame prevede la somministrazione intratecale di un radiofarmaco, solitamente tramite una puntura lombare, e il successivo monitoraggio del suo percorso attraverso immagini scintigrafiche acquisite in diverse ore, o addirittura giorni.
Le principali applicazioni cliniche di questo studio sono:
- diagnosi dell’idrocefalo a pressione normale (un disturbo caratteristico dell’anziano con una triade sintomatologica di alterazione dell’andatura, deficit cognitivo e incontinenza urinaria, il cui pattern di riassorbimento alterato è visibile nell’immagine accanto);
- identificazione di ostruzioni del sistema ventricolare;
- individuazione e localizzazione di perdite di CSF (rinorrea o otorrea);
- valutazione della pervietà dei sistemi di derivazione (shunt).
Proprio gli shunt ventricolo-peritoneali rappresentano la soluzione terapeutica più comune per correggere un drenaggio alterato. Questi dispositivi artificiali deviano il liquido in eccesso dai ventricoli cerebrali alla cavità addominale, dove viene riassorbito. Sistemi simili sono utilizzati anche per la somministrazione diretta di farmaci chemioterapici in caso di tumori del SNC.
La medicina nucleare si rivela nuovamente cruciale nel follow-up di questi pazienti: uno studio di pervietà dello shunt con un radiofarmaco inoculato direttamente nel dispositivo permette di verificarne il corretto funzionamento in modo minimamente invasivo, confermando il passaggio del tracciante dal ventricolo al sito di drenaggio distale e scongiurando così il rischio di malfunzionamenti che richiederebbero un intervento chirurgico di revisione.
Fonte: A Concise Guide to Nuclear Medicine (Abdelhamid H. Elgazzar e Saud Alenezi)