Le patologie respiratorie rappresentano oggi una delle principali cause di morbilità e mortalità a livello globale. Tumori polmonari e bronchiti croniche persistono come problemi clinici di primaria importanza, con un impatto significativo sui sistemi sanitari. Questo scenario è ulteriormente complicato dall’invecchiamento generale della popolazione. Pazienti anziani, infatti, sono sempre più numerosi e presentano spesso comorbidità che li espongono a un rischio maggiore di ricovero e interventi chirurgici, sia d’urgenza che programmati. In questi contesti, i pericoli di complicanze post-operatorie, come l’embolia polmonare e le infezioni, sono particolarmente elevati.
Now loading…
In questa complessa cornice, la medicina nucleare si afferma come una disciplina indispensabile, offrendo strumenti unici per la diagnosi e il monitoraggio di numerose condizioni patologiche dell’apparato respiratorio. Il suo contributo è cruciale in ambiti come la diagnosi tempestiva dell’embolia polmonare, la caratterizzazione di processi infettivi intratoracici e la valutazione delle neoplasie maligne.
Le radici di questa applicazione risalgono agli studi pionieristici di Knipping e West alla fine degli anni Cinquanta, ma è nel 1963, con la riuscita produzione della albumina macroaggregata (MAA) da parte di G.V. Taplin, che la medicina nucleare respiratoria inizia concretamente la sua storia, basata sulla possibilità di visualizzare la perfusione sanguigna dei polmoni.
Le tecniche di medicina nucleare trovano ampia e consolidata applicazione nello studio del sistema respiratorio, distinguendosi per la loro natura non invasiva e per la capacità di fornire informazioni funzionali, spesso non ottenibili con altre metodiche di imaging. I suoi campi di applicazione principali sono:
- La diagnosi dell’embolia polmonare
- La Sarcoidosi Polmonare
- La Fibrosi Polmonare Idiopatica
- La polmonite da Pneumocystis jirovecii
- La permeabilità alveolare
- Tumore del Polmone
- Studi quantitativi pre-operatori di Ventilazione/Perfusione
La diagnosi dell’embolia polmonare
Diagnosticare un’embolia polmonare sulla base della sola clinica rappresenta una sfida notoria per i medici. I sintomi, come dispnea, dolore toracico e tosse, sono spesso aspecifici e possono essere facilmente confusi con quelli di altre patologie cardiache o respiratorie. Anche gli esami di laboratorio e la radiografia del torace standard frequentemente non mostrano alterazioni decisive. In molti casi, l’embolia può persino presentarsi in modo del tutto asintomatico, specialmente quando gli emboli sono di piccole dimensioni. Questa elusività ha conseguenze gravi: si stima che storicamente solo circa un quarto delle embolie polmonari fatali venga diagnosticato prima del decesso del paziente.
Now loading…
Il dato più allarmante riguarda la prognosi: senza un trattamento appropriato e tempestivo, il tasso di mortalità per embolia polmonare può superare il 30%. Al contrario, una diagnosi rapida e una terapia anticoagulante immediata riducono drasticamente questo rischio, portando la mortalità a valori compresi tra il 2,5% e l’8%. Questa enorme differenza sottolinea l’importanza critica di disporre di strumenti diagnostici affidabili ed efficienti.
In questo contesto, la scintigrafia polmonare ventilazione/perfusione (V/Q scan) mantiene un ruolo di primo piano, consolidato da decenni di pratica clinica e riconosciuto come il metodo di screening non invasivo più costo-efficace. Il suo principale vantaggio risiede nella capacità unica di fornire una mappa funzionale dei polmoni, offrendo informazioni sia regionali che quantitative essenziali per la diagnosi. Oltre a confermare o escludere la presenza di un’embolia, questo esame è fondamentale per valutarne la gravità e per monitorare nel tempo l’evoluzione della malattia e la risposta alla terapia.
Nella pratica clinica moderna, la scintigrafia viene spesso affiancata dalla Tomografia Computerizzata (TC) spirale con mezzo di contrasto, che permette di visualizzare direttamente il coagulo di sangue all’interno dei vasi polmonari. Non esiste un unico protocollo universalmente valido: gli algoritmi diagnostici variano da ospedale a ospedale. In alcuni centri si preferisce eseguire prima la TC, in altri, specialmente in caso di controindicazioni al mezzo di contrasto (come allergie o insufficienza renale), la scintigrafia rappresenta l’indagine di prima scelta, con l’altra metodica che interviene in un secondo momento per risolvere eventuali dubbi residui.
La procedura scintigrafica prevede una doppia fase. Per lo studio della perfusione sanguigna, viene iniettato in vena un radiofarmaco a base di macroaggregati di albumina (MAA) marcati con Tecnezio-99m. Queste microparticelle si distribuiscono nei capillari polmonari in proporzione al flusso sanguigno. Per lo studio della ventilazione, il paziente inala invece un gas radioattivo (come lo Xenon-133) o un aerosol nebulizzato (come il Tc-99m DTPA o il Technegas®, un aerosol ultrafine con comportamento simile a un gas), che visualizza il flusso d’aria negli alveoli.
Per un’interpretazione corretta, è fondamentale che il medico nucleare abbia a disposizione una radiografia del torace recente, idealmente eseguita entro le 12 ore precedenti la scintigrafia, da utilizzare come riferimento anatomico.
In un soggetto sano, sia la scintigrafia di ventilazione che quella di perfusione mostrano una distribuzione omogenea e uniforme del radiofarmaco in entrambi i polmoni.
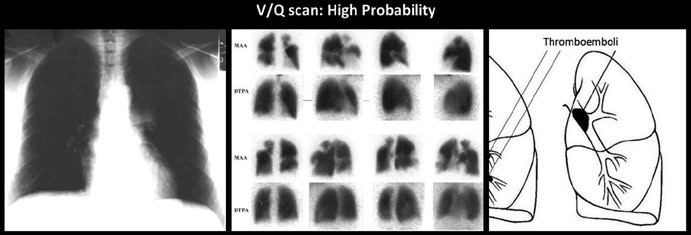
Il pattern caratteristico dell’embolia polmonare, invece, si manifesta con uno o più difetti di perfusione (aree “fredde” non irrorate) in regioni del polmone che mantengono una ventilazione normale. Questa dissociazione, definita “mismatch ventilazione/perfusione” (con perfusione assente e ventilazione conservata), è altamente suggestiva per la presenza di un embolo che ostruisce un’arteria polmonare. Tipicamente, questi difetti perfusionali hanno una forma a cuneo e sono localizzati in posizione pleurica.
La Sarcoidosi Polmonare
La sarcoidosi è una malattia granulomatosa sistemica che colpisce prevalentemente gli adulti giovani, con un’incidenza maggiore nella popolazione di colore e tra gli abitanti di zone temperate. Nonostante sia conosciuta da oltre un secolo, la sua eziologia esatta rimane un mistero. L’ipotesi più accreditata è che sia il risultato di una risposta immunitaria cellulare eccessiva, mediata da linfociti T helper, scatenata dall’esposizione ad antigeni ancora non identificati, che potrebbero essere di origine ambientale, infettiva o autoimmunitaria.
La caratteristica patologica fondamentale della malattia è la formazione di granulomi epitelioidi non caseosi (che quindi si distinguono da quelli della tubercolosi) in uno o più organi. Questi aggregati di cellule infiammatorie, se non controllati, possono evolvere verso la fibrosi, portando a un danno permanente e alla disfunzione d’organo. I polmoni sono il bersaglio principale, essendo coinvolti in oltre il 90% dei casi. Il processo inizia come un’alveolite interstiziale diffusa, per poi organizzarsi nei caratteristici granulomi, che si localizzano preferenzialmente nei setti alveolari e nelle pareti dei bronchi e dei vasi sanguigni polmonari.
La diagnosi è spesso complessa e si basa su un approccio multidisciplinare che integra tre elementi: un quadro clinico e/o radiologico suggestivo, la conferma istologica attraverso una biopsia che evidenzi i granulomi non caseosi, e l’esclusione accurata di altre patologie (come tubercolosi o linfomi) che possono mimarne le manifestazioni. Una particolarità della sarcoidosi è il suo frequente riscontro accidentale in pazienti completamente asintomatici, durante l’esecuzione di una radiografia del torace richiesta per altri motivi. Quando invece i sintomi sono presenti, quelli toracici più comuni includono dispnea (affanno), tosse secca e fastidio toracico.
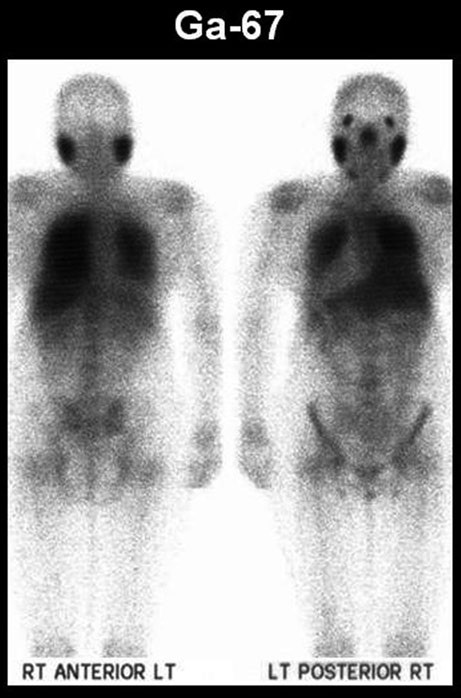
La medicina nucleare offre strumenti preziosi per la gestione di questa patologia, permettendo di valutarne l’attività infiammatoria e l’estensione. Tradizionalmente, si è utilizzato il Gallio-67 (Ga-67), un radiotracciante che si accumula nei siti di infiammazione attiva e in alcuni tumori. In condizioni normali, i polmoni non mostrano accumulo di Ga-67. La sua utilità sta nell’identificare focolai extratoracici della malattia e, soprattutto, nel valutare l’attività infiammatoria iniziale e la risposta alla terapia nel follow-up. Pattern classici all’esame sono l’accumulo diffuso a livello polmonare e il tipico “segno del lambda“, dato dall’ingrandimento delle stazioni ilari e paratracheali bilaterali. Un altro segno caratteristico è l’intensa captazione a livello delle ghiandole lacrimali e salivari, che crea un’immagine del “panda”.
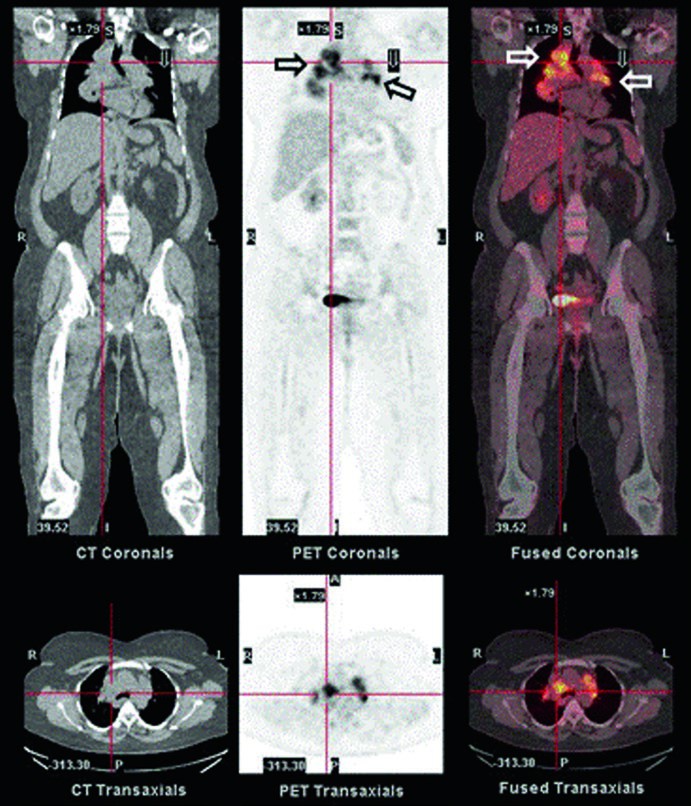
Oggi, la PET/TC con 18F-FDG si sta affermando come metodica superiore in molti contesti. Il FDG, un analogo del glucosio, viene avidamente captato non solo dalle cellule tumorali ma anche da quelle infiammatorie attive, come i macrofagi all’interno dei granulomi. La PET/TC combina quindi l’informazione funzionale della PET con il dettaglio anatomico della TC, permettendo di ottenere una mappatura morfo-funzionale completa di tutte le localizzazioni della malattia attiva. Questo la rende particolarmente adatta per valutare con precisione il mediastino, i linfonodi, le regioni polmonari posteriori e le lesioni extratoraciche.
Now loading...
Il suo ruolo è diventato indispensabile nelle forme atipiche, complesse e multisistemiche di sarcoidosi, dove fornisce una guida per le biopsie e uno strumento oggettivo e sensibile per monitorare l’efficacia delle terapie immunosoppressive, mostrando precocemente una riduzione del metabolismo del glucosio nei granulomi in risposta al trattamento.
La Fibrosi Polmonare Idiopatica
La Fibrosi Polmonare Idiopatica (IPF) è una malattia polmonare interstiziale cronica e progressiva, caratterizzata da un esito infausto. La sua essenza patologica risiede in un processo di danno alveolare ricorrente, seguito da una risposta riparativa anomala che sfocia in un’infiammazione parenchimale persistente (alveolite) e, infine, in una fibrosi interstiziale irreversibile. Questo processo distorce in modo brutale l’architettura normale del polmone, creando una caratteristica “architettura a nido d’ape” o ad “alveare” visibile alla TC ad alta risoluzione, che porta a una progressiva incapacità di ossigenare il sangue, con conseguente grave morbidità e mortalità.
Le cause scatenanti rimangono in gran parte sconosciute, da cui il termine “idiopatica”. L’ipotesi più accreditata è che la malattia si sviluppi in individui geneticamente predisposti a seguito di un’esposizione cronica a fattori ambientali non ancora del tutto identificati (come fumo di sigaretta, polveri organiche e inorganiche, o infezioni virali latenti), che innescherebbero una risposta aberrante e continua nei meccanismi di riparazione del tessuto polmonare.
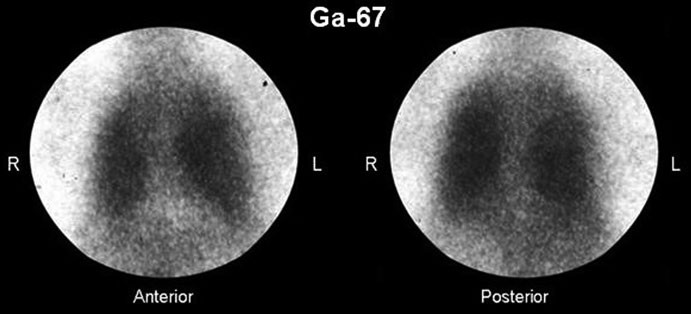
In questo contesto, la medicina nucleare fornisce strumenti cruciali per valutare l’attività della malattia, un aspetto distintivo dalla semplice estensione della fibrosi. Il Gallio-67 (Ga-67) ha storicamente un ruolo importante in questa valutazione. L’intensità dell’accumulo di questo tracciante a livello polmonare correla direttamente con il grado di cellularità infiammatoria (alveolite) riscontrabile istologicamente sulle biopsie. Pertanto, una scintigrafia al Ga-67 positiva indica un processo infiammatorio attivo, aiutando i clinici a valutare visivamente e quantitativamente l’estensione dell’infiammazione e a monitorare la risposta a terapie anti-fibrotiche o immunosoppressive.
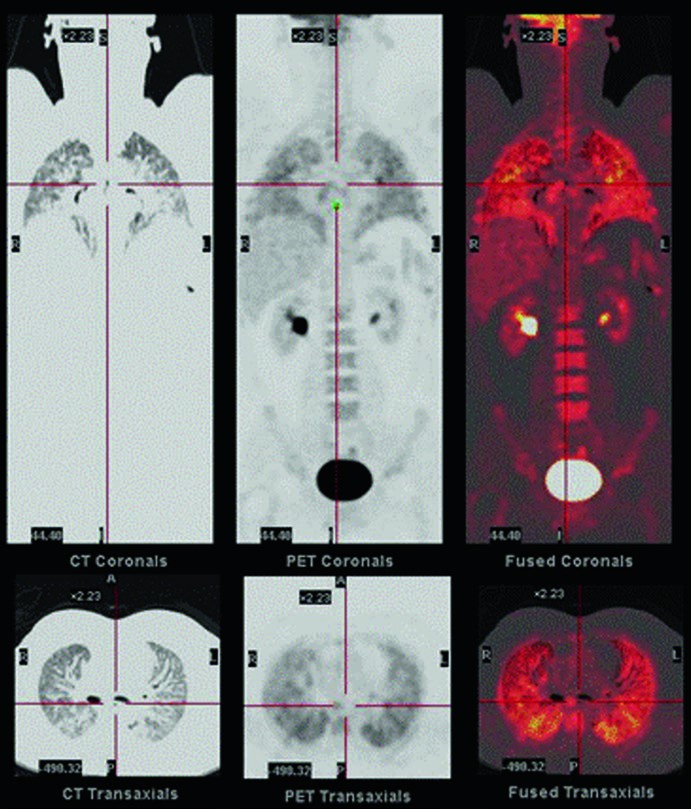
Oggi, la PET/TC con 18F-FDG si è dimostrata ancor più sensibile e specifica del Ga-67 nel valutare l’attività di malattia. L’FDG, captato avidamente dalle cellule infiammatorie attive presenti nei focolai di alveolite, permette di identificare e quantificare con precisione le aree di infiammazione in atto, anche in stadi precoci, e di monitorare oggettivamente l’efficacia della terapia nel tempo, offrendo un prezioso strumento per personalizzare il trattamento.
Now loading...
La polmonite da Pneumocystis jirovecii
La polmonite da Pneumocystis jirovecii (in passato nota come P. carinii) rimane un’infezione opportunistica temibile, classificata tra le micosi. È una causa significativa di morbidità e mortalità nei pazienti immunodepressi, in particolare quelli con HIV/AIDS, trapiantati d’organo o in terapia chemioterapica intensiva o immunosoppressiva, sebbene possa occasionalmente colpire anche individui non immunocompromessi.
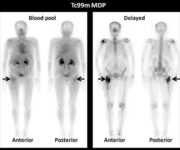
La diagnosi può essere complessa a causa della spesso aspecificità dei sintomi e dei reati radiologici. La medicina nucleare, attraverso la scintigrafia al Gallio-67, offre un valido aiuto. In caso di infezione attiva da P. jirovecii, il radiotracciante mostra tipicamente un intenso e diffuso accumulo a livello polmonare bilaterale, molto superiore al normale background. Questo esame è estremamente sensibile nel sospettare la malattia, guidando così le procedure diagnostiche più invasive (come il lavaggio bronco-alveolare) per la conferma microbiologica e permettendo di avviare precocemente una terapia salvavita.
La permeabilità alveolare
L’integrità della membrana alveolo-capillare è fondamentale per prevenire l’accumulo di liquidi negli spazi aerei e garantire gli scambi gassosi. La valutazione della sua permeabilità fornisce informazioni preziose e precoci su un eventuale danno polmonare subclinico, completamente slegato dai tradizionali test di funzionalità respiratoria (spirometria) che misurano invece volumi e flussi.
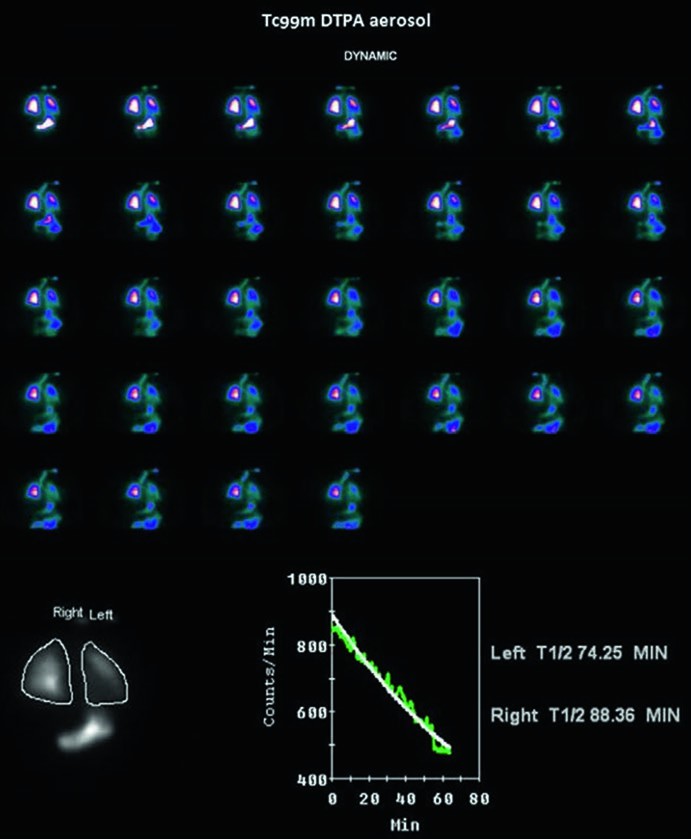
Questa valutazione è possibile grazie a uno studio di ventilazione dinamico effettuato con l’inalazione di un aerosol radioattivo, come il Tc-99m DTPA o il Technegas®. Dopo l’inalazione, una gamma-camera acquisisce immagini sequenziali per monitorare la velocità con cui il tracciante viene “ripulito” dagli alveoli e trasferito nel torrente sanguigno attraverso la membrana. Elaborando queste immagini, si calcola il tempo di dimezzamento polmonare (half-clearance time).
Un tempo di clearance accorciato è indicativo di un aumento della permeabilità della barriera alveolo-capillare. Questa condizione è riscontrabile in diverse patologie e stati, tra cui il fumo di sigaretta (anche in fumatori apparentemente sani), la sarcoidosi attiva, l’infezione cronica da epatite C e l’abuso di alcol. Al contrario, un tempo di clearance prolungato può essere osservato in condizioni come il diabete mellito.
Questa metodica si rivela quindi uno strumento sensibile per rilevare un’alveolite subclinica (un’infiammazione degli alveoli non ancora evidente con altri esami) in diverse categorie di pazienti, permettendo un intervento precoce prima che il danno diventi manifesto.
Tumore del Polmone
Il carcinoma polmonare rappresenta una delle principali sfide oncologiche a livello globale. È il secondo tumore più diagnosticato sia negli uomini (dopo quello alla prostata) che nelle donne (dopo quello al seno), ma, purtroppo, si conferma la prima causa di morte per cancro in entrambi i sessi. Questa drammatica discordanza tra incidenza e mortalità sottolinea l’aggressività della malattia e l’importanza cruciale di una diagnosi precoce e accurata.
Esistono due grandi categorie di tumore del polmone, con comportamenti biologici e approcci terapeutici molto diversi: il carcinoma a piccole cellule (SCLC), più raro e spesso associato al fumo, caratterizzato da una crescita rapida e una forte tendenza a metastatizzare; e il carcinoma non a piccole cellule (NSCLC), che raccoglie invece diverse istologie (adenocarcinoma, carcinoma squamoso, carcinoma a grandi cellule) e rappresenta la forma più comune.
La radiografia del torace (RX) rimane spesso il primo esame imaging eseguito per indagare sintomi respiratori o come controllo di routine, e può portare al riscontro fortuito di una lesione. Tuttavia, i suoi limiti intrinseci (bassa risoluzione e natura bidimensionale) la rendono poco affidabile per una caratterizzazione definitiva. La Tomografia Computerizzata (TC) del torace, con la sua elevata risoluzione spaziale e la visualizzazione tridimensionale, è lo strumento di prima scelta per la diagnosi e la stadiazione anatomica iniziale, permettendo di valutare con precisione le dimensioni del tumore e il suo rapporto con le strutture circostanti.
In questo contesto, le modalità di medicina nucleare hanno rivoluzionato la gestione del paziente oncologico. Se in passato sono stati utilizzati vari radioisotopi (come Gallio-67, Tallio-201 e 99mTc-Sestamibi), oggi la PET/TC con 18F-FDG è diventata una tappa imprescindibile nell’iter diagnostico-terapeutico. Questo esame sfrutta l’avida captazione del glucosio radioattivo (FDG) da parte della maggior parte delle cellule tumorali, che presentano un metabolismo glucidico molto più accelerato rispetto ai tessuti sani.
I suoi campi di applicazione sono vasti e cruciali:
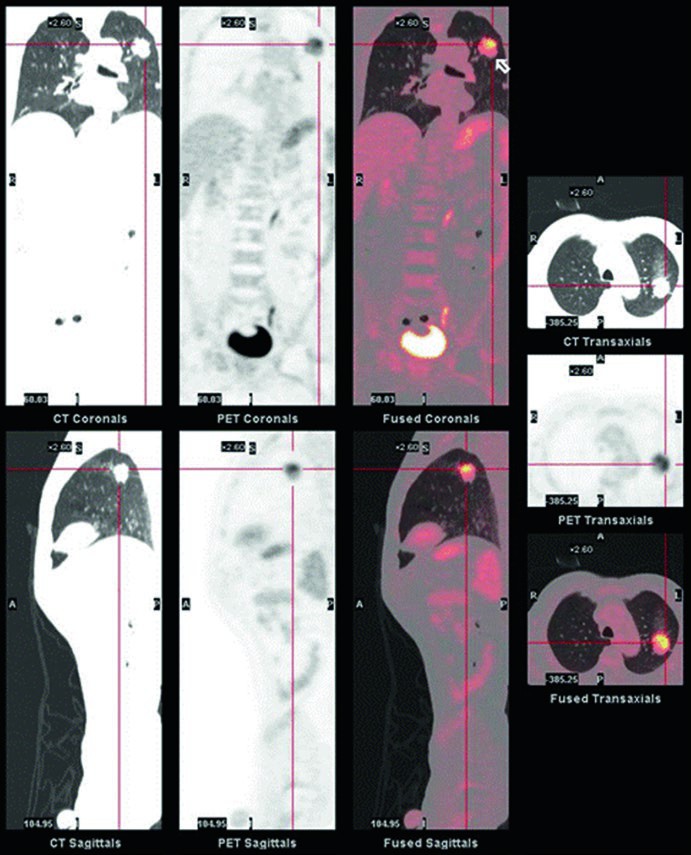
- caratterizzazione del nodulo solitario: distingue tra lesioni benigne e maligne con alta accuratezza, guidando la decisione tra il monitoraggio e l’approccio bioptico/chirurgico;
- stadiazione: valuta l’eventuale coinvolgimento dei linfonodi ilari e mediastinici e identifica metastasi a distanza (es. surreni, ossa, fegato, cervello) con una sensibilità superiore alla sola TC, modificando in modo significativo lo stadio di malattia e la strategia terapeutica in una percentuale consistente di pazienti;
- planning della radioterapia: delinea con precisione i volumi tumorali metabolicamente attivi da irradiare, risparmiando il più possibile il tessuto sano;
- valutazione della risposta alla terapia: permette di discriminare precocemente tra responders e non-responders dopo chemio o radioterapia, differenziando il tessuto necrotico e fibrotico (che non capta FDG) da quello tumorale residuo attivo.
- ristadiazione e sospetto di recidiva: identifica la ripresa di malattia in presenza di alterazioni tissutali post-terapiche poco chiare alla TC.
È fondamentale, tuttavia, essere consapevoli dei suoi limiti. Falsi negativi possono occorrere in noduli di dimensioni molto piccole (< 1 cm; 0.5 cm con gli ultimi tomografi) o in tumori con un basso metabolismo glucidico intrinseco, come il carcinoide, l’adenocarcinoma mucinoso e alcune forme di carcinoma bronco-alveolare. Allo stesso modo, falsi positivi sono possibili in presenza di condizioni infiammatorie o infettive attive (come tubercolosi, sarcoidosi o polmoniti) che, comportando un’attivazione metabolica dei macrofagi, mimano il comportamento del tessuto tumorale. Per questo, l’interpretazione dell’esame PET/TC deve sempre avvenire in un contesto di integrazione multidisciplinare, tenendo conto della clinica e degli altri reati radiologici.
Studi quantitativi pre-operatori di Ventilazione/Perfusione
La pianificazione di un intervento chirurgico ai polmoni, sia esso una resezione per tumore o una procedura in pazienti trapiantati, richiede una valutazione meticolosa della funzionalità respiratoria residua attesa. È qui che la medicina nucleare fornisce un contributo insostituibile, andando ben oltre le semplici immagini anatomiche.
Gli studi quantitativi di perfusione e ventilazione permettono di misurare con precisione la percentuale di funzione polmonare contribuita da ciascun polmone e, ancor più nel dettaglio, da ciascun lobo. Questa informazione è vitale per prevedere in modo oggettivo se, dopo l’asportazione di una parte del polmone, la capacità respiratoria rimanente sarà sufficiente a sostenere il paziente, scongiurando il rischio di un’insufficienza respiratoria post-operatoria.
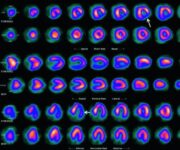
La metodica standard prevede la somministrazione di macroaggregati di albumina marcati con Tecnezio-99m (99mTc-MAA) per lo studio della perfusione. Una gamma-camera acquisisce immagini che vengono poi elaborate da un software dedicato. Il polmone viene suddiviso in regioni di interesse (ad esempio, dividendo ciascun polmone in terzi: superiore, medio e inferiore) e il sistema calcola il conteggio radioattivo in ciascuna area. Questo valore viene espresso come una percentuale della radioattività totale polmonare, che corrisponde direttamente alla frazione di flusso sanguigno (e quindi di funzione) di quella specifica regione.
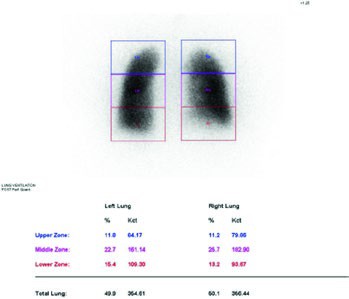
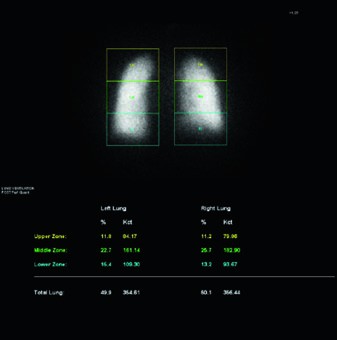
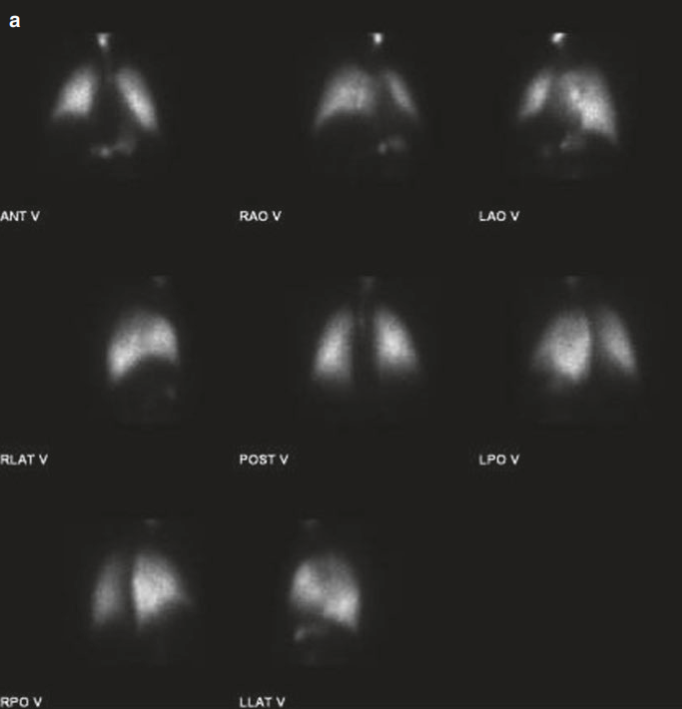
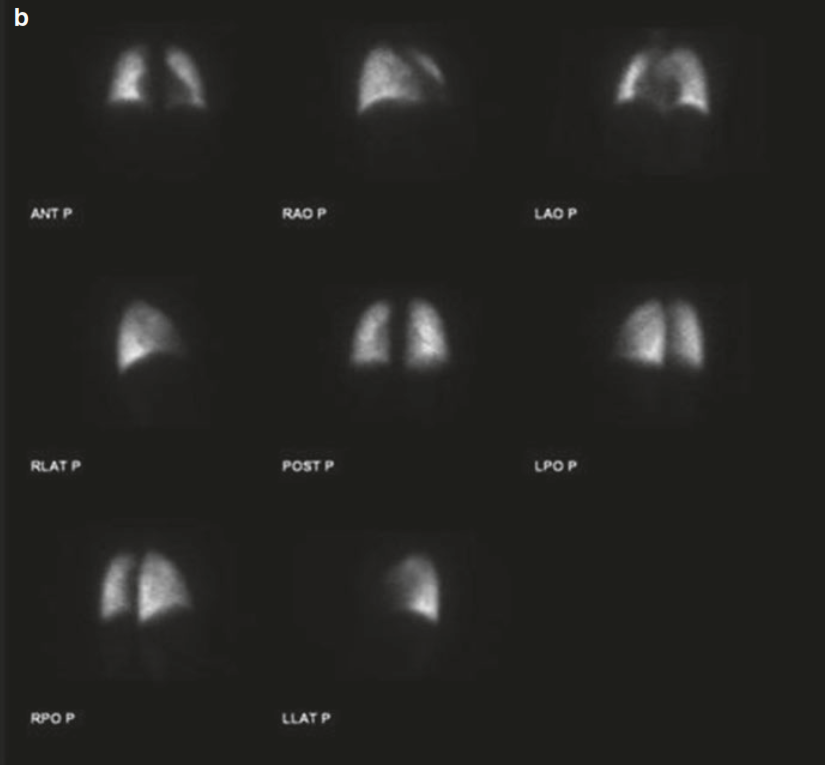
Studio di quantificazione preoperatoria della ventilazione (a) e della perfusione (b).
Questo calcolo è di cruciale importanza nei pazienti oncologici, in cui è frequente una comorbidità con la Broncopneumopatia Cronica Ostruttiva (BPCO) o con enfisema, condizioni che già compromettono la riserva funzionale polmonare. Conoscere quanto contribuisce il lobo da asportare alla funzione globale permette al chirurgo e al pneumologo di stratificare con accuratezza il rischio operatorio e di prendere decisioni informate sull’estensione della resezione.
Il progresso tecnologico ha ulteriormente affinato questa pratica. L’avvento della SPECT/CT (Single Photon Emission Computed Tomography integrata con la Tomografia Computerizzata) rappresenta un significativo passo in avanti. Questa tecnica ibrida combina i dati funzionali della perfusione con la dettagliata anatomia della TC, consentendo una delimitazione anatomica molto più precisa dei lobi polmonari. Di conseguenza, la quantificazione della funzione lobare ottenuta con SPECT/CT è notevolmente più accurata e affidabile rispetto alla planar scintigrafia tradizionale, offrendo al team chirurgico una mappa morfo-funzionale dettagliata per la massima personalizzazione del trattamento.
Fonte: A Concise Guide to Nuclear Medicine (Abdelhamid H. Elgazzar e Saud Alenezi)