Il processo di invecchiamento è un processo coordinato della perdita delle funzioni tessutali e cellulari, che fa sì che l’organismo sia meno capace di riprodursi e sopravvivere.
In una prima fase vi è la diminuzione della capacità di riserva dell’organismo dovuto allo stress (QI, infezioni, sforzo fisico). Nelle fasi più avanzate appaiono deficit funzionali in situazioni di riposo.
Basi molecolari
Durante l’invecchiamento si produce un accumulo di alterazioni biochimiche che colpiscono le funzioni degli acidi nucleici, delle proteine e dei lipidi.
Per quanto riguarda gli acidi nucleici abbiamo:
- aumento del numero di alterazioni strutturali cromosomiche per la rottura di una sola catena di DNA.
- diminuzione della metilazione del DNA, collegata con la differenziazione cellulare. Nel feto vi è una diminuzione della metilazione, a partire dalla nascita aumenta e torna a diminuire durante l’invecchiamento.
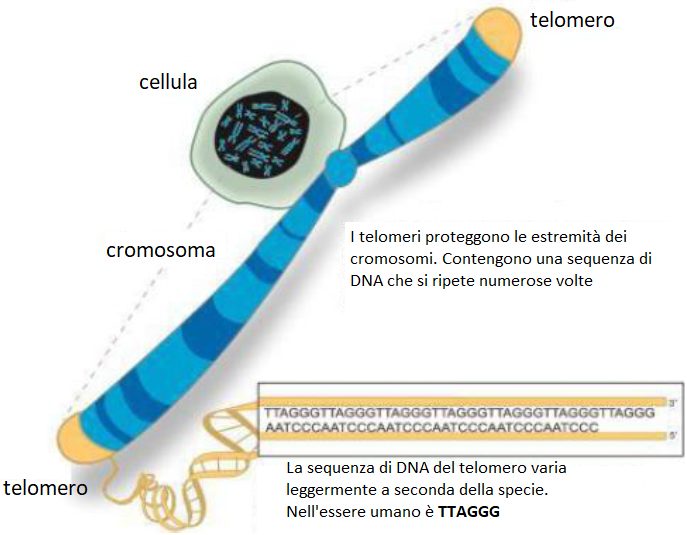
- diminuzione dei telomeri. Il numero di replicazioni cellulari è limitato ed è condizionato dalla lunghezza dei telomeri: ogni volta che la cellula si differenzia, perde alcune paia di basi. Quando la DNA polimerasi replica il DNA non lo fa in forma completa, ma lascia circa 50 paia di basi nella porzione finale, per tanto, come protezione, il telomero si accorcia sempre di più ad ogni replicazione. Quando arriva ad una fase in cui il telomero è praticamente finito, questo DNA rimane sprotetto e la cellula entra in apoptosi e muore. Quindi, la lunghezza dei telomeri è relazionata con la senescenza. Inoltre, recenti studi in vivo dimostrano che la lunghezza dei telomeri delle cellule può essere collegato con lo sviluppo di malattie degenerative.
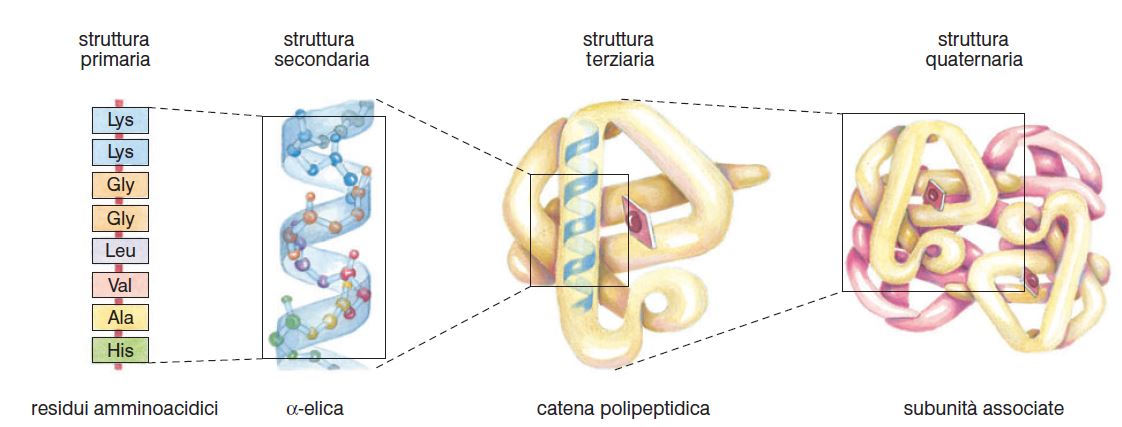
Le alterazioni che coinvolgono le proteine sono:
- glicosilazione: le proteine glicosilate perdono la loro funzione.
- ossidazione per accumulo di radicali liberi.
- deamminazione con privazione di amminoacidi.
- cambiamenti nell’acetilazione degli istoni.
- ubiquitinazione delle proteine: le proteine ormai vecchie e non funzionanti hanno normalmente un processo di degradazione che avviene nel proteasoma. Questa funzione cellulare viene persa con l’invecchiamento, per cui non vengono eliminate le proteine non funzionanti che continueranno ad essere presenti nella cellula.
I lipidi, invece, subiscono soprattutto processi di ossidazione e perossidazione, fenomeni che sono relazionati soprattutto con il processo di arteriosclerosi.
Fisiopatologia dell’invecchiamento
Il processo di invecchiamento si deve principalmente ad alterazioni cellulari in quanto le cellule senescenti assumono dei fenotipi caratteristici dovuti a cambiamenti biochimici. Recentemente sono stati descritti dei marcatori immunoistochimici che permettono di distinguere le cellule senescenti.
Tra i cambiamenti cellulari che avvengono vi sono le limitazioni nel numero di divisioni cellulari. Questo si deve alla lunghezza dei telomeri che si riduce. I telomeri, come già detto, formano protezione all’estremità dei cromosomi e contengono una sequenza di DNA che si ripete numerose volte (nell’essere umano la sequenza è TTAGGG). Con lo stress diminuisce l’attività della telomerasi, incaricata di mantenere l’integrità dei cromosomi, per cui la cellula si riproduce di meno e successivamente muore.
Un altro cambiamento molto importante è la diminuzione dell’efficacia della trasduzione dei segnali (diminuzione della funzionalità dei recettori) che alla fine porta alla morte cellulare delle cellule per apoptosi.
Inoltre il processo di invecchiamento comporta alterazioni tissutali in quanto i tessuti perdono la capacità rigenerativa e riparatoria. Infatti, il processo di riparazione di un malato che soffre una ipotensione severa perché non arriva sufficiente sangue al rene, non avviene così facilmente in una persona anziana come avverrebbe in una persona giovane. Il rene non recupera e si sviluppa un’insufficienza renale terminale. Questo accade anche in molti altri organi.
Teorie sull’invecchiamento
L’invecchiamento può essere la conseguenza di mutazioni causate e influenzate dai fattori ambientali e dalle patologie sofferte durante tutta la vita.
Secondo la teoria genetica dell’invecchiamento, esso è la conseguenza delle mutazioni che accorciano la sopravvivenza a lungo termine (non influenzato dai processi di selezione naturale). Potrebbe essere dovuto ad alcuni geni che erano utili nelle fasi iniziali della vita, e che sono dannosi in una seconda fase, dopo la fase riproduttiva. Al giorno d’oggi, nella specie umana, non è stato individuato nessuno di questi geni, tuttavia nelle specie animali sì. Quindi l’invecchiamento potrebbe essere la conseguenza di lesioni genetiche casuali multiple.
Ci sono importanti differenze tra l’invecchiamento in base alla specie (soprattutto se ci confrontiamo con il regno vegetale). Ci sono somiglianze nel processo di invecchiamento nei gemelli monozigoti.
Fonte: MeteoWeb
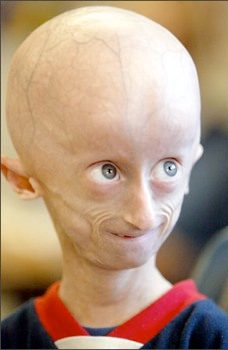
Alcune sindromi legate all’invecchiamento sono la sindrome di Progeria o di Hutchinson-Gilford (invecchiamento prematuro , persone che invecchiano precocemente) e la sindrome di Werner (invecchiamento prematuro nell’età adulta).
La sindrome di Progeria produce un’invecchiamento prematuro in tenerà età ed è causata da una mutazione sporadica del gene codificante la proteina lamina A. I bambini affetti da tale patologia hanno una testa calva e grande con vene prominenti, assenza di ciglia e sopracciglia, naso a becco, mento retratto, malattie cardiache precoci, coronaropatie per malattia arteriosclerotica, torace stretto, articolazioni grandi e rigide e pigmentazioni cutanee.
La sindrome di Werner consiste invece in un invecchiamento prematuro nell’età adulta. E’ una malattia genetica autosomica recessiva causata da mutazioni diverse nel gene WRN della regione p12. In questo gene si conoscono più di 60 mutazioni. E’ una proteina corta che non viene trasportata al nucleo, oltre a “decomporsi” più velocemente del normale. Sono coinvolti i processi di replicazione, riparazione e trascrizione. La sindrome di Werner ha un’incidenza di 3/106 persone, con una maggiore incidenza nel Giappone. Le persone affette da tale patologia hanno perdita del pelo, cataratta bilaterale, diabete, ulcere e maggiore rischio di neoplasie.
I fattori ambientali che influenzano il processo di invecchiamento sono diversi:
- stress psichico: i caregiver di pazienti anziani con demenza invecchiano più velocemente;
- alimentazione: la restrizione calorica ha molto a che fare con la longevità. Mangiare poco allunga la vita, questo si è stato visto meglio in altre specie animali;
- raggi ultravioletti: invecchiano la pelle;
- esercizio fisico: ritarda le conseguenze dell’invecchiamento. Non previene l’invecchiamento, ma le conseguenze, infatti le persone che fanno esercizio fisico hanno meno complicanze mediche.
- esposizione a fattori tossici (alcol e tabacco);
- comorbilità: aver avuto patologie durante il corso degli anni può dare luogo a sequele e la persona e più fragile.
Cambiamenti provocati dall’invecchiamento
L’invecchiamento è un processo che colpisce tutti gli organi di tutti gli apparati quindi i cambiamenti sono numerosi:
- i CAMBIAMENTI ENDOCRINOLOGICI sono diversi:
- Menopausa. E’ un cambio brusco, universale, che colpisce l’asse ipotalamo-ipofisi-gonadi nelle donne prossime ai 50 anni di età. Essa comporta una diminuzione della secrezione ovarica di estrogeni per insufficienza ovarica, aumento di FSH e LH (l’ipofisi cerca di stimolare l’ovaio per incentivare il suo funzionamento).
Negli uomini questo processo non è così brusco in quanto già dai 20 anni si ha una diminuzione dell’1% di testosterone sierico annuale (il 70% degli uomini al di sopra dei 70 anni ha livelli di testosterone paragonabili a quelli di una persona con ipogonadismo). - Tendenza all’aumento di glicemia, soprattutto in situazioni di stress (come il prediabete), per resistenza periferica all’insulina, dovuta alla diminuzione dei recettori dell’insulina, o perché i recettori non sono più molto sensibili ad essa (resistenza nella trasduzione dei segnali di molte cellule).
- Diminuzione di tiroxina (diminuzione della clearance di T4), di solito frequente nell’ipotiroidismo. Vi è sintesi di tiroxina, però c’è anche meno consumo periferico, per cui è compensato. Perciò il fabbisogno ormonale esogeno nell’ipotiroidismo diminuisce con l’avanzare dell’età.
- Diminuzione di GH-RH, GH e IGF-1 nel plasma (relazione dell’ormone della crescita con il mantenimento della massa muscolare).
- Aumento del grasso corporale. Su questo fenomeno sono state date diverse teorie, come per esempio la diminuzione di leptina.
- Minore risposta all’ADH a livello renale. Questo aumenta la diuresi. Dall’altro lato la sensazione di sete è diminuita nonostante questo stimolo osmotico, motivo per cui i soggetti anziani sono più vulnerabili alla deprivazione acquosa e soffrono più facilmente di disidratazione.
- Alterazioni della funzione pineale. L’insonnia è comune, correlata alle fasi 3 e 4 del sonno. È stato collegato alla diminuzione della secrezione di melatonina dalla ghiandola pineale.
- Alterazioni nella funzione surrenalica. I livelli di cortisolo sono del 20-50% più alti nei soggetti anziani, e c’è una risposta di cortisolo sierico più alta con lo stress. I pazienti fragili hanno livelli più elevati di cortisolo serale rispetto ai soggetti non fragili. Questi livelli di cortisolo sono inoltre associati a diminuzione della memoria, riduzione della massa ossea (BMD), maggiore rischio di fratture e aumento del grasso corporeo.
Infine vi è una diminuzione della sintesi di renina e dei livelli sierici di aldosterone con tendenza all’iponatriemia e all’iperkaliemia. - Alterazioni nel metabolismo del calcio e del fosforo. Si osserva una diminuzione di vitamina D dovuta a cause multifattoriali: diminuzione dell’apporto di calcio, diminuzione dell’assorbimento, minore esposizione solare (soprattutto in persone istituzionalizzate), diminuzione nell’idrossilazione a livello di fegato e rene. I pazienti fragili hanno livelli più bassi di 25-(OH)-vitD dei non fragili. Attualmente si consiglia ai soggetti anziani di 70 anni di assumere supplementi (minimo 600 UI) di vitamina D al giorno per ridurre l’incidenza di fratture.
Inoltre si osserva un aumento del fosforo per deterioramento della funzione renale. Con l’età si avrà quindi una tendenza all’aumento di PTH e un deficit di vitamina D3.
- Menopausa. E’ un cambio brusco, universale, che colpisce l’asse ipotalamo-ipofisi-gonadi nelle donne prossime ai 50 anni di età. Essa comporta una diminuzione della secrezione ovarica di estrogeni per insufficienza ovarica, aumento di FSH e LH (l’ipofisi cerca di stimolare l’ovaio per incentivare il suo funzionamento).
- i CAMBIAMENTI NEL SISTEMA RESPIRATORIO consistono in:
- Diminuzione del riflesso tossigeno e della funzione ciliare, per cui è più facile che si verifichino broncoaspirazioni.
- Diminuzione dell’elasticità polmonare.
- Diminuzione dei volumi polmonari (eccetto del volume residuo) e della capacità di diffusione polmonare (trasferimento di CO2).
- i CAMBIAMENTI NEL SISTEMA CARDIOVASCOLARE sono rappresentati da:
- Diminuzione del collagene e del calcio nelle arterie.
- Diminuzione della distesibilità arteriosa, diminuzione della pressione arteriosa (più frequentemente la sistolica). Questo a lungo andare provoca un’ipertrofia ventricolare sinistra. Il cuore invecchiando è meno distensibile perché è più ingrossato.
- Diminuzione della diastole cardiaca.
- Diminuzione della sensibilità dei barorecettori, che provoca ipotensione ortostatica.
- Diminuzione dell’automatismo del nodo sinusale, per cui è più facile che si verifichino bradicardie o blocchi cardiaci.
- i CAMBIAMENTI NELL’APPARATO DIGESTIVO tra cui:
- Ipomotilità del colon, che provoca stipsi e feci dure o fecaloma (è il problema che più preoccupa l’anziano). Il fecaloma è una stitichezza estrema che comporta l’impossibilità nel defecare. Le persone anziane con deficit cognitivi hanno un maggior rischio di subirlo.
- Ipocloridria.
- Diminuzione dell’attività metabolica epatica, quindi i farmaci assunti hanno una maggior probabilità di produrre effetti indesiderati.
- i CAMBIAMENTI NEL SISTEMA EMATOPOIETICO E IMMUNE consistono in:
- Diminuzione della capacità di riserva del midollo osseo.
- Ipofunzione delle cellule T, ma non delle cellule B e neanche dei neutrofili. Quindi si avrà una minore risposta ai vaccini, minori livelli di immunizzazione e maggior rischio di infezioni.
- Aumento nel numero di anticorpi (anticorpi antinucleo), dovuto all’iperfunzionamento delle cellule B. Tuttavia la maggior parte delle volte questo non ha ripercussioni patologiche.
- Aumento del rischio trombotico, aumentano i fattori FVIII, fibrinogeno, dimero-D, che condizionano la tendenza all’ipercoagulabilità.
- Aumento dei parametri infiammatori (teoria dell’invecchiamento).
- i CAMBIAMENTI NEL SISTEMA GENITO-URINARIO E RENALE sono:
- Diminuzione del filtrato glomerulare (equazione di Cockroft-Gault, equazione di MDRD4 o Levey e equazione di MDRD6).
- Diminuzione della capacità di riserva dell’epitelio tubulare. Ha importanza in situazioni di shock e di insufficienza renale secondaria a ipotensione. In questi casi si produce una necrosi tubulare acuta in cui la capacità di rigenerazione è molto ridotta rispetto a quella di un individuo giovane.
- Atrofia vaginale a causa di una diminuzione della produzione di muco. Ciò rende difficoltosa anche la relazione di coppia.
- i CAMBIAMENTI NEL SISTEMA MUSCOLO-SCHELETRICO riguardano:
- Diminuzione della massa muscolare magra.
- Aumento del collagene extracellulare.
- Diminuzione della densità minerale ossea.
- Degenerazione della cartilagine. La degenerazione inizia a partire dai 30 anni (artrosi) e la cartilagine non si rigenera.
- i CAMBIAMENTI NEL SISTEMA NERVOSO includono:
- Perdita neuronale con atrofia cerebrale conseguente a diminuzione del flusso sanguigno cerebrale. Si a una diminuzione della memoria (indipendentemente da malattie come l’Alzheimer) e un rallentamento psico-motorio (la persona anziana parla più lentamente).
- Alterazione della regolazione termica (maggiore sensibilità all’ipotermia).
- Diminuzione della sintesi di catecolamine/serotonina con una maggiore predisposizione alla depressione.
- Diminuzione della sintesi di dopamina (con quadri extrapiramidali).
- Diminuzione del sonno (insonnia).
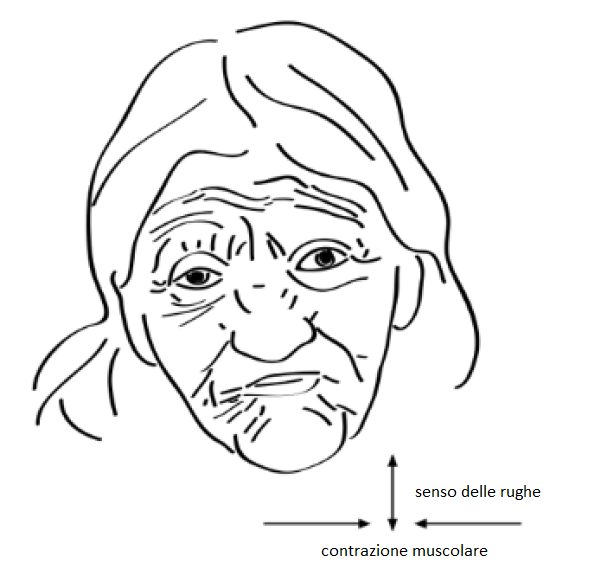
- i CAMBIAMENTI NELLA PELLE, sono quelli più visibili e consistono in:
- Atrofia cutanea.
- Rughe.
- Capelli grigi/bianchi.
- Fragilità capillare.
- Minore crescita delle unghia.
A questi cambiamenti si devono associare la tendenza nello stare sdraiati e la riduzione della funzionalità degli organi di senso (presbiopia e presbiacusia).