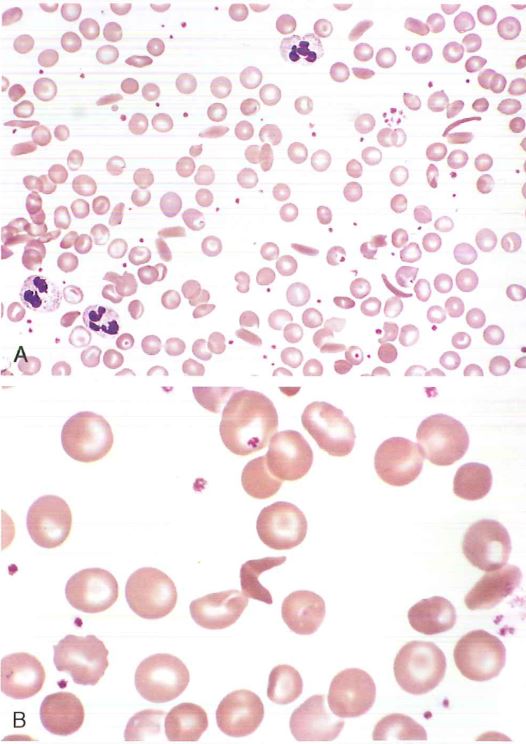
La sferocitosi ereditaria è un tipo di anemia emolitica: le anemie emolitiche mostrano caratteristiche quali distruzione prematura dei globuli rossi (emolisi extravascolare prematura), aumento dell’eritropoiesi midollare e accumulo di prodotti del catabolismo dell’emoglobina. I globuli rossi vanno incontro ad una distruzione prematura perché anomali.
Normalmente la vita media di un eritrocita è di 120 giorni, invece in caso di tale patologia può essere anche di soli 20 giorni.
Fisiologicamente la distruzione dei globuli rossi senescenti avviene in cellule fagocitiche mononucleate di milza, fegato e midollo osseo (emolisi extravascolare).
Le cause possono essere molteplici, nel caso della sferocitosi è un’anomalia nella membrana dei globuli rossi.
In generale esistono 2 tipi di emolisi: intra ed extravascolare. La differenza sostanziale è la splenomegalia (ingrossamento milza) che caratterizza la extravascolare. La milza è ingrossata a causa dei macrofagi che fagocitano i globuli rossi che si accumulano nei cordoni splenici di Billroth.
L’emolisi intravascolare è causata da danno meccanico (traumi), infezione da parassiti intracellulari come il plasmodio della malaria e fattori esogeni.
Conseguenze sono:
- emoglobinemia, anomala presenza di emoglobina in plasma sanguigno (normalmente l’emoglobina libera viene complessata ad un’aptoglobina formando un complesso che viene degradato dai fagociti mononucleati);
- anemia;
- emoglobinuria: l’emoglobina libera, non legata ad aptoglobina, si ossida a metaemoglobina che è di colore marrone. Le cellule tubulari prossimali del rene riassorbono e catabolizzano gran parte dell’emoglobina filtrata e della metaemoglobina, però una piccola quantità è rilasciata nell’urina che acquista un colore rosso marrone;
- emosiderosi: il ferro rilasciato dall’emoglobina si accumula a livello renale:
- ittero: eccesso di bilirubina derivata dal catabolismo dei gruppi eme a livello dei fagociti mononucleati.
L’emolisi extravascolare avviene quando i globuli rossi diventano meno plastici. Le conseguenze sono anemia, ittero e splenomegalia.
Le principali proteine alterate coinvolte nella sferocitosi ereditaria sono: anchirina, spettrina, proteina della banda 3 e banda 4.2.
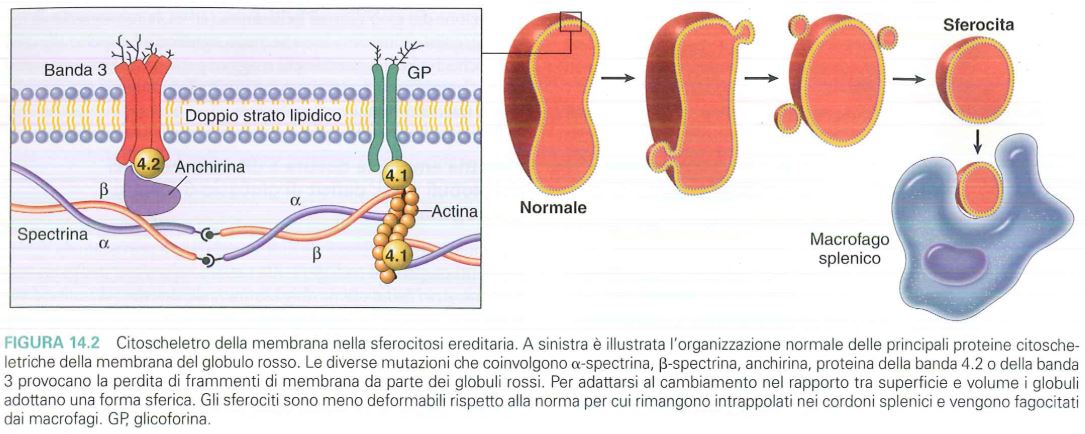
Nella membrana e citoscheletro di un globulo rosso normale troviamo la spettrina, costituita da una catena α e una catena β che si associano ad altre catene α e β a formare dei tetrameri testa-coda. Tale tetramero si associa all’actina, una delle proteine più importanti del citoscheletro, tramite dei ponti con la banda 4.1 e la glicoforina. A stabilizzare l’intero complesso troviamo altre proteine come l’anchirina, che fa da ponte con delle proteine di membrana (la banda 4.2 e la banda 3). Tutto questo complesso è soprattutto importante per l’elasticità del globulo rosso.
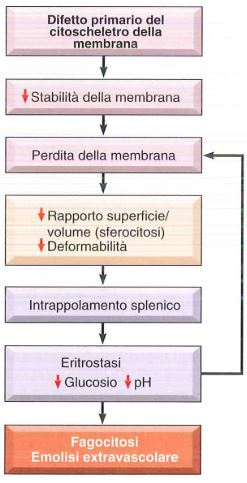
Ciascuna di queste proteine può subire una mutazione a livello di DNA e quindi risultare come proteina anomala e dar luogo a citoscheletro anomalo del globulo rosso. Avendo un citoscheletro anomalo, il globulo rosso, in seguito a forze di taglio, oltre a perdere elasticità, perde anche pezzi di membrana, quindi riduce la propria dimensione (a parità di volume, riduce la superficie) e diventa sferico invece che disco biconcavo come è normalmente. Perciò viene riconosciuto come anomalo e fagocitato dai macrofagi splenici.
Normalmente il globulo rosso è una cellula che per poter circolare nel distretto capillare, deve essere in grado di modificare continuamente la sua forma: i globuli rossi normali devono ampiamente deformarsi per lasciare i cordoni di Billroth ed entrare nei sinusoidi splenici. A causa della loro ridotta deformabilità conseguente ad una ridotta elasticità, questi “sferociti” rimangono intrappolati nei cordoni splenici dove vengono fagocitati.
Quindi a seguito dell’intrappolamento si ha un’eritrostasi (congestionamento dei globuli rossi in milza): questo porta ad un abbassamento dei livelli di glucosio e quindi ad una ridotta sintesi di ATP che aumenta il danno a livello di membrana perché l’ATP serve per tutta una serie di processi metabolici all’interno della cellula, inoltre si abbassa il pH e questo provoca ulteriormente la distruzione di queste cellule che poi vengono fagocitate.
La prevalenza della malattia è 1/5.000 soprattutto nelle popolazioni del Nord Europa. Nella sferocitosi ereditaria sono coinvolti tutti geni autosomici. La mutazione più frequente riguarda l’anchirina.
Se l’ereditarietà è dominante ci sono mutazioni frameshift e non-senso che portano ad una mancata produzione di proteina, perciò basta una sola mutazione affinché si abbia la malattia. Se l’ereditarietà è recessiva ci sono mutazioni di senso in cui l’anchirina viene prodotta ma è anomala, e in questo caso affinché si abbia la sferocitosi entrambi gli alleli devono essere mutati.
Per quanto riguarda l’α-spectrina, questa normalmente viene sintetizzata in quantità doppie rispetto alla β-spectrina, quindi se si ha la mutazione di una singola copia (che significa una carenza del 50% della proteina), questa non da problemi, mentre se entrambi gli alleli sono mutati, la spectrina non si produce e quindi abbiamo la sferocitosi.
Le altre mutazioni delle altre proteine coinvolte sono dominanti, cioè basta che una singola copia sia mutata affinché si abbia la patologia.

Caratteristiche sferocitosi:
- anemia emolitica (vita media dei globuli rossi 10-20 giorni). L’anemia può essere compensata da iperproduzione di eritropoietina EPO (30% pazienti asintomatica) da parte del midollo osseo che induce quindi una maggiore produzione di globuli rossi.
- si possono manifestare possibili crisi aplastiche secondarie causate da infezioni da parvovirus che infetta e lisa i precursori delle cellule eritroidi;
- splenomegalia: dovuta alla congestione dei cordoni di Billroth e all’iperplasia per aumento dell’eritrofagocitosi, trattabile con splenectomia che però porta ad un aumento del rischio di infezioni;
- ittero da eccessiva produzione di bilirubina derivante dal metabolismo della emoglobina liberata in seguito alla distruzione dei globuli rossi;
La gravità della patologia e l’ereditarietà dipendono dal tipo di mutazione. Un gene mutato in membri della stessa famiglia avrà una espressione simile.