Lo shock neurogeno rappresenta una condizione clinica critica derivante da una lesione acuta del sistema nervoso centrale (SNC). Si tratta di un’emergenza medica che esige un’immediata identificazione e un intervento terapeutico tempestivo per ridurre significativamente la morbilità e la mortalità associate. Una gestione inadeguata, infatti, può compromettere irrimediabilmente l’esito neurologico e la stabilità sistemica del paziente.
Lo shock neurogeno è definito come una sindrome scatenata da una lesione midollare acuta o del SNC. È caratterizzato da una severa ipotensione che non deriva da una perdita di volume ematico (ipovolemia assoluta), bensì da una condizione di vasoplegia, ovvero una paralisi del tono vascolare. Sebbene possa avere diverse eziologie, l’evento traumatico ne costituisce la causa più comune.
È imperativo operare una chiara distinzione terminologica, poiché parte della letteratura utilizza i termini in modo intercambiabile, tra shock neurogeno e shock spinale. Sebbene le due condizioni siano clinicamente correlate e possano coesistere, descrivono fenomeni fisiopatologici distinti:
- lo shock neurogeno si riferisce primariamente alla compromissione emodinamica, ovvero la vasodilatazione periferica e le sue conseguenze cardiovascolari;
- lo shock spinale descrive invece il fenomeno neurologico della perdita transitoria dei riflessi mediati dal midollo spinale al di sotto del livello della lesione.
Un paziente con una lesione trasversa del midollo toracico alto, ad esempio, manifesterà simultaneamente l’instabilità emodinamica dello shock neurogeno e la paralisi flaccida con areflessia caratteristica dello shock spinale.
Caricamento…
Fisiopatologia
La comprensione dei meccanismi fisiopatologici che governano lo shock neurogeno è cruciale per interpretare correttamente il quadro clinico e per impostare una terapia razionale. La sindrome è il risultato diretto di uno squilibrio acuto del sistema nervoso autonomo, con conseguenze sistemiche profonde.
Il meccanismo emodinamico centrale dello shock neurogeno origina da un danno alla catena dei gangli ortosimpatici a livello toraco-lombare. Questa lesione provoca una drastica interruzione dell’attività del sistema nervoso simpatico. Di conseguenza, l’attività del sistema nervoso parasimpatico (vagale) rimane incontrastata, determinando uno squilibrio autonomico che si manifesta con effetti cardiovascolari devastanti.
Le conseguenze di questo squilibrio sono dirette e clinicamente evidenti:
- ipotensione: è il risultato della perdita del tono simpatico, che causa una marcata vasodilatazione periferica (vasoplegia). Le arteriole e le venule si dilatano, aumentando la capacità del sistema circolatorio e causando un crollo della pressione arteriosa sistemica, pur in assenza di una reale perdita ematica;
- bradicardia: questo segno rappresenta un “effetto paradosso” e un elemento distintivo dello shock neurogeno. In condizioni normali, l’ipotensione scatena una tachicardia riflessa mediata dai barocettori, che inviano efferenze simpatiche al nodo senoatriale per aumentare la frequenza cardiaca. Nello shock neurogeno, il danno alla via efferente simpatica toraco-lombare interrompe questo meccanismo compensatorio. Il paziente, pertanto, manifesta una frequenza cardiaca ridotta (bradicardia) anziché aumentata, aggravando ulteriormente l’instabilità emodinamica.
Questa cascata diretta dalla disregolazione autonomica al collasso emodinamico detta la classica, sebbene paradossa, presentazione clinica che deve essere immediatamente riconosciuta.
Clinica e approccio diagnostico
Il riconoscimento del pattern clinico tipico dello shock neurogeno è fondamentale per differenziarlo da altre forme di shock, specialmente nel contesto di un paziente politraumatizzato, dove potrebbe coesistere uno shock emorragico. Un’accurata valutazione clinica e strumentale è pertanto imperativa.
Il quadro clinico del paziente con shock neurogeno è caratterizzato da una triade di segni e sintomi specifici che riflettono la disfunzione autonomica e neurologica:
- segni cardiovascolari: la presentazione classica include l’associazione di ipotensione e bradicardia. La profonda vasoplegia e la conseguente caduta della pressione arteriosa media portano a un’ipoperfusione sistemica, che si manifesta con oligo-anuria, un indicatore critico di flusso ematico renale compromesso, comune a tutti gli stati di shock;
- deficit neurologici: a seconda della localizzazione e della gravità della lesione midollare, il paziente può presentare tetraplegia (paralisi dei quattro arti) o paraplegia (paralisi degli arti inferiori), accompagnate da una riduzione del tono muscolare e dalla perdita dei riflessi al di sotto del livello della lesione;
- compromissione respiratoria: nelle lesioni che interessano il midollo cervicale o toracico alto, il coinvolgimento dei muscoli respiratori (diaframma e intercostali) può compromettere la meccanica ventilatoria, conducendo a un quadro di insufficienza respiratoria acuta, caratterizzata da ipercapnia, ipossiemia e acidosi.
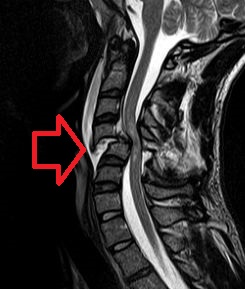
L’approccio diagnostico richiede un monitoraggio emodinamico intensivo per la valutazione continua di pressione arteriosa, frequenza cardiaca e stato di perfusione.
Parallelamente, è essenziale confermare la presenza, la sede e l’entità della lesione midollare attraverso indagini radiologiche mirate, quali radiografia (RX), tomografia computerizzata (TC) e risonanza magnetica (RM) della colonna vertebrale.
Shock Spinale: fasi e caratteristiche distintive
Lo shock spinale è un fenomeno neurologico distinto, sebbene clinicamente correlato e spesso concomitante allo shock neurogeno. Mentre lo shock neurogeno descrive la disfunzione cardiovascolare, lo shock spinale si riferisce alla perdita temporanea della funzione riflessa del midollo spinale al di sotto della lesione, con una specifica evoluzione temporale.
Descritto per la prima volta da Whytt nel 1750, lo shock spinale è definito come una perdita di sensibilità accompagnata da paralisi motoria flaccida e dalla completa perdita dei riflessi mediati dal midollo spinale. La sua evoluzione clinica è stata suddivisa in quattro fasi:
- Fase 1 (areflessia): caratterizzata dalla perdita completa e immediata dei riflessi al di sotto del livello della lesione.
- Fase 2 (recupero iniziale dei riflessi): inizia tipicamente entro 1-2 giorni, con la ricomparsa dei primi riflessi cutanei o polisinaptici.
- Fase 3 (iperreflessia): si manifesta con una risposta riflessa esagerata agli stimoli, indicativa di una riorganizzazione neuronale post-lesionale.
- Fase 4 (evoluzione in spasticità): l’iperreflessia progredisce verso una condizione di spasticità muscolare cronica.
La durata complessiva di queste fasi può variare da 3-6 settimane fino a diversi mesi. Una condizione simile può manifestarsi anche in ambito ostetrico, come conseguenza di eventi di stress correlati al parto.
Trattamento e gestione clinica
La gestione dello shock neurogeno richiede un duplice approccio: il supporto immediato delle funzioni vitali compromesse (emodinamica e respiratoria) e, ove possibile, il trattamento della lesione midollare sottostante, che rappresenta la risoluzione definitiva del quadro clinico. Le strategie terapeutiche mirano a ripristinare una perfusione d’organo adeguata e a prevenire il danno secondario.
Il trattamento iniziale dell’ipotensione prevede l’infusione endovenosa di cristalloidi isotonici per aumentare il precarico e, di conseguenza, la gittata cardiaca. È tuttavia fondamentale procedere con cautela per evitare un sovraccarico volemico del circolo polmonare e il conseguente rischio di edema polmonare iatrogeno, specialmente in pazienti con ridotta riserva cardiovascolare. L’ipotensione refrattaria alla terapia fluidica impone l’utilizzo di farmaci vasopressori, come la noradrenalina o la dopamina, che agiscono aumentando il tono vascolare periferico per contrastare la vasoplegia.
Il trattamento di prima scelta per la bradicardia sintomatica è l’atropina. Il suo impiego è specificamente indicato quando la frequenza cardiaca scende al di sotto di 30-35 battiti per minuto (bpm), al fine di ripristinare una frequenza adeguata a sostenere la gittata cardiaca.
Parte integrante del trattamento è la somministrazione di ossigeno per correggere l’ipossiemia, in particolare nei pazienti con compromissione della funzione respiratoria a causa di lesioni midollari alte che coinvolgono i muscoli respiratori.
L’efficacia del trattamento con alte dosi di metilprednisolone (30 mg/kg in bolo, seguito da 5,4 mg/kg/ora per 24 ore), somministrato entro 8 ore dal trauma per ridurre il danno midollare, non è stata dimostrata. Il suo utilizzo rimane pertanto controverso e non è universalmente raccomandato.
L’approccio terapeutico deve essere personalizzato e guidato da un monitoraggio continuo e attento dei parametri vitali del paziente.
Conclusioni
Lo shock neurogeno e lo shock spinale rappresentano due manifestazioni critiche di una lesione acuta del midollo spinale, la cui gestione efficace richiede una profonda comprensione fisiopatologica. Il riconoscimento della presentazione clinica unica dello shock neurogeno, caratterizzata dalla combinazione di ipotensione e bradicardia paradossa, è essenziale per una diagnosi differenziale rapida, soprattutto in contesti traumatici complessi.
La gestione clinica si fonda su un attento e mirato supporto emodinamico e respiratorio. L’uso giudizioso di fluidi, l’impiego tempestivo di vasopressori per l’ipotensione refrattaria e di atropina per la bradicardia severa costituiscono i pilastri del trattamento. Tuttavia, la risoluzione definitiva della sindrome dipende dal trattamento della lesione neurologica primaria.
In definitiva, la capacità del clinico di differenziare il collasso emodinamico dello shock neurogeno dall’areflessia transitoria dello shock spinale non è una mera distinzione accademica; è la pietra angolare di una strategia terapeutica mirata a preservare la perfusione d’organo e a massimizzare il potenziale di recupero neurologico.
Fonte: Manuale di anestesia e rianimazione. Concorso Nazionale SSM.
Altre fonti: