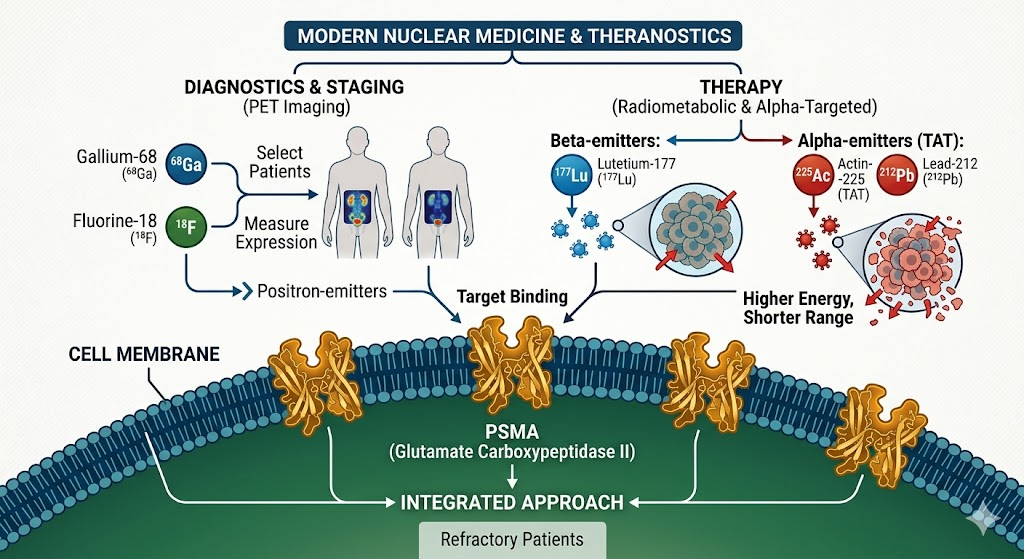
L’evoluzione del trattamento per il carcinoma prostatico metastatico ha subito una trasformazione radicale nell’ultimo decennio, spostandosi da un approccio puramente palliativo a una gestione di precisione basata sulle caratteristiche molecolari della malattia. In questo scenario, la medicina nucleare è emersa non solo come uno strumento diagnostico di supporto, ma come un pilastro terapeutico centrale attraverso il paradigma della teranostica. Questo approccio combina la capacità dell’imaging molecolare di identificare bersagli cellulari specifici con la potenza dei radioligandi per erogare dosi citotossiche di radiazioni direttamente alle cellule tumorali, minimizzando al contempo il danno ai tessuti sani circostanti.1 2
Il bersaglio principale di questa rivoluzione è la proteina di membrana specifica della prostata (PSMA), un enzima transmembrana (glutammato carbossipeptidasi II) sovraespresso nella quasi totalità dei tumori prostatici, la cui espressione aumenta parallelamente all’aggressività biologica, al grado di Gleason e allo stato di resistenza alla castrazione.3
La medicina nucleare moderna integra radioisotopi diversi per scopi differenti: emettitori di positroni come il Gallio-68 (68Ga) o il Fluoro-18 (18F) per la Tomografia a Emissione di Positroni (PET) finalizzata alla stadiazione e alla selezione dei pazienti, ed emettitori di particelle beta o alfa per la terapia radiometabolica.
L’attuale panorama clinico è dominato dall’impiego del Lutezio-177 (177Lu), un emettitore beta, e dall’emergere di terapie alfa-mirate (TAT) che utilizzano isotopi come l’Attinio-225 (225Ac) o il Piombo-212 (212Pb), offrendo nuove speranze anche per i pazienti refrattari alle linee di trattamento convenzionali.4 5
Basi molecolari e biologiche dell’imaging PSMA-mirato
Il successo della medicina nucleare nel carcinoma prostatico metastatico è intrinsecamente legato alla biologia del PSMA. Questa glicoproteina di tipo II non è solo un marcatore di tessuto prostatico, ma un enzima funzionale coinvolto nell’assorbimento dei nutrienti e nella segnalazione cellulare. La sua espressione è fino a 100-1000 volte superiore nelle cellule neoplastiche rispetto al tessuto normale, e tale up-regulation è ulteriormente esacerbata dalla deprivazione androgenica, creando una finestra terapeutica ideale per i pazienti con carcinoma prostatico metastatico resistente alla castrazione (mCRPC).
Evoluzione dei traccianti diagnostici: dalla Colina al PSMA
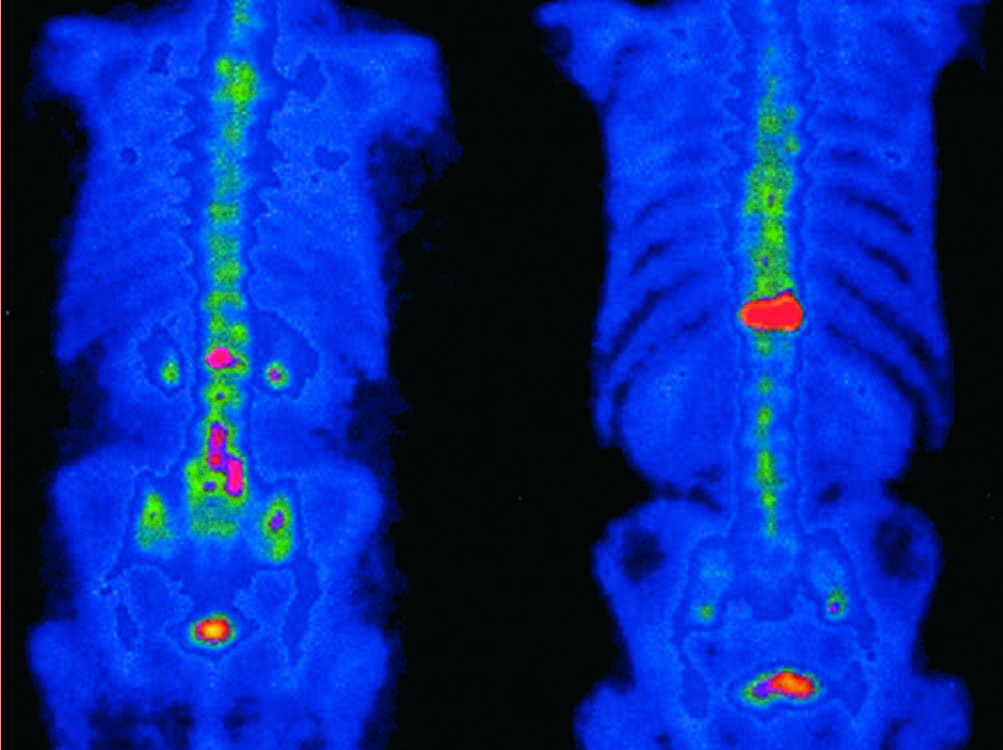
Storicamente, la diagnosi strumentale della metastatizzazione prostatica si è basata sulla scintigrafia ossea e sulla TC. Tuttavia, queste metodiche presentano una sensibilità limitata, specialmente nella fase di recidiva biochimica precoce, dove le lesioni sono spesso di dimensioni microscopiche.
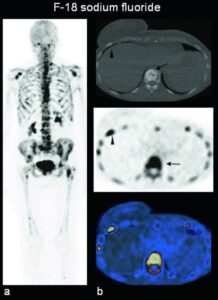
L’introduzione della PET/TC con colina (11C-colina o 18F-colina) ha rappresentato un progresso significativo, sfruttando l’aumentata biosintesi delle membrane cellulari nelle cellule tumorali. Tuttavia, la colina mostra un’accuratezza subottimale quando i livelli di PSA sono inferiori a 1 ng/ml, rendendo difficile la localizzazione della malattia in fasi precocemente trattabili con intento curativo.
L’avvento dei ligandi del PSMA ha cambiato questo scenario. La PET/TC con 68Ga–PSMA-11 o ligandi marcati con 18F (come il 18F–DCFPyL) ha dimostrato una sensibilità e una specificità nettamente superiori rispetto alla colina e alla diagnostica convenzionale. Questa metodica consente di identificare metastasi linfonodali di pochi millimetri e lesioni ossee precoci, impattando significativamente sul management clinico e sulla scelta della strategia terapeutica.
| Parametro diagnostico | PET/TC Colina | PET/TC PSMA |
|---|---|---|
| Meccanismo di captazione | Metabolismo dei fosfolipidi | Legame recettoriale specifico |
| Sensibilità per PSA < 1 ng/ml | < 60% | > 75% |
| Sensibilità per PSA > 2 ng/ml | Elevata | Eccellente |
| Escrezione urinaria | Presente (limita studio pelvi) | Variabile (dipende dal ligando) |
| Ruolo nella stadiazione iniziale | Non raccomandata (bassa sensibilità) | Raccomandata per alto rischio |
Secondo le linee guida AIOM 2024 e le recenti indicazioni, la PSMA PET/TC è considerata raccomandata per i pazienti con tumore ad alto o molto alto rischio, in presenza di PSA persistente dopo prostatectomia o in caso di recidiva biochimica. Tuttavia, non è mandatoria in tutte le situazioni: in casi di fallimento biochimico isolato con risalita del PSA, la TC e la scintigrafia ossea possono ancora essere considerate adeguate per definire lo stato M0 o M1, riservando la PET a situazioni specifiche per massimizzare il beneficio terapeutico.
Il concetto di eterogeneità tumorale e l’imaging multimodale
Un limite critico del PSMA è l’eterogeneità della sua espressione. Circa il 10-15% dei pazienti con mCRPC può presentare lesioni PSMA-negative, specialmente in presenza di varianti neuroendocrine o fenotipi altamente dedifferenziati. In questi casi, l’integrazione con la PET/TC con 18F–FDG è fondamentale. Il cosiddetto “mismatch” (lesioni positive al FDG ma negative al PSMA) è un predittore di scarsa risposta alla terapia radioligandica e indica la necessità di approcci chemioterapici o terapie mirate alternative.
La selezione del paziente ideale per la medicina nucleare terapeutica richiede quindi una valutazione visiva in cui l’uptake del PSMA in tutte le lesioni misurabili sia superiore a quello del fegato (criteri VISION).
Terapia radioligandica con Lutezio-177 (177Lu): lo standard attuale
Il Lutezio-177 (177Lu) marcato con PSMA-617 (nome commerciale Pluvicto) rappresenta la prima terapia radioligandica mirata approvata per il trattamento del mCRPC. Il Lutezio-177 è un radioisotopo che emette particelle beta con un’energia moderata e un raggio d’azione tessutale di circa 1-2 mm. Questa caratteristica lo rende ideale per trattare sia le lesioni linfonodali che le metastasi ossee, poiché la radiazione è sufficientemente penetrante da distruggere il tumore ma ha un raggio d’azione limitato che preserva il midollo osseo circostante.6 Inoltre, l’emissione di una piccola quota di raggi gamma consente di eseguire l’imaging post-terapeutico per confermare la corretta biodistribuzione del farmaco.
Risultati dei trial registrativi: VISION e TheraP
L’approvazione del 177Lu–PSMA-617 si basa su evidenze cliniche di alto livello. Lo studio di fase III VISION ha arruolato pazienti con mCRPC già trattati con almeno un inibitore della via del recettore degli androgeni (ARPI) e uno o due regimi di chemioterapia con taxani.
| Endpoint clinico (Trial VISION) | Lu-PSMA-617 + standard of care | solo standard of care |
|---|---|---|
| Sopravvivenza globale mediana (OS) | 15.3 mesi | 11.3 mesi |
| Sopravvivenza libera da progressione (rPFS) | 8.7 mesi | 3.4 mesi |
| Risposta del PSA ≥ 50% | 46% | 7.1% |
| Risposta obiettiva (ORR) | 29.8% | 1.7% |
| Risposta completa (CR) | 5.6% | 0% |
L’analisi dei dati di VISION indica una riduzione del rischio di morte del 38% nel braccio sperimentale.
Complementare a VISION è lo studio australiano TheraP (fase II), che ha confrontato direttamente il 177Lu–PSMA-617 con il cabazitaxel in pazienti progrediti dopo docetaxel. TheraP ha dimostrato una percentuale di risposta biochimica significativamente superiore per il radioligando (66% vs 37%) e una minore incidenza di eventi avversi di grado 3-4, sottolineando il ruolo della medicina nucleare come opzione preferibile in termini di tollerabilità e qualità della vita.
Gestione clinica e protocolli di somministrazione
Il protocollo standard approvato prevede la somministrazione endovenosa di 7.4 GBq (200 mCi) ogni 6 settimane, per un massimo di 6 cicli.
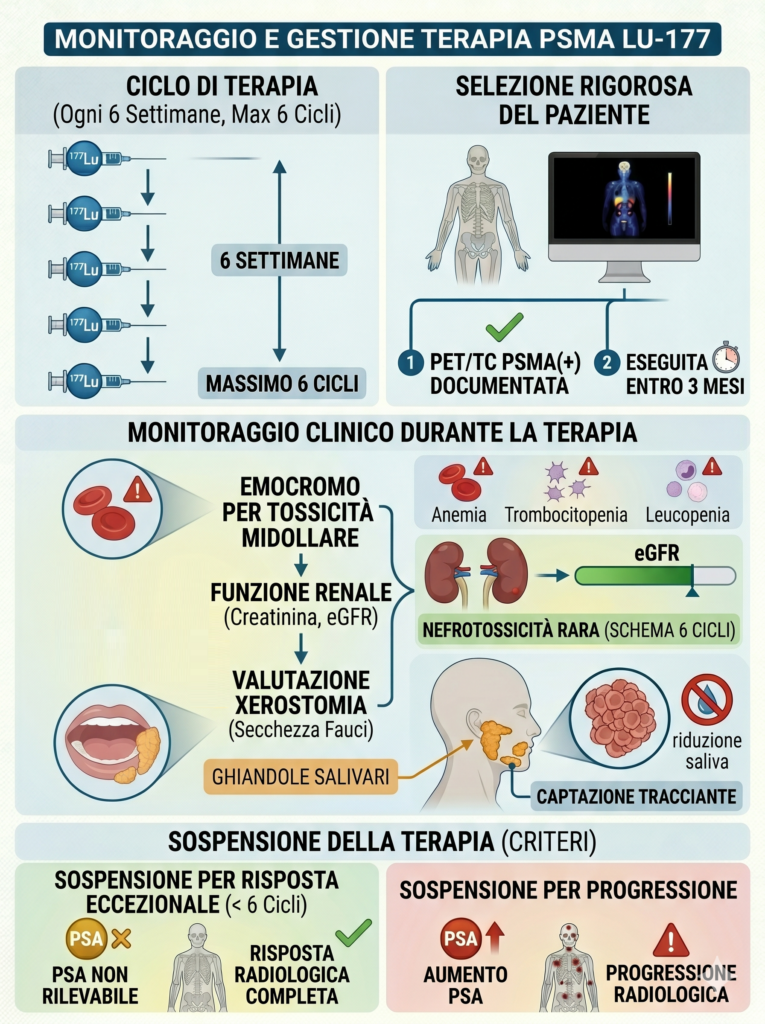
La selezione del paziente è rigorosa: deve essere documentata la positività al PSMA tramite PET/TC eseguita entro 3 mesi dall’inizio del trattamento. Durante la terapia, il monitoraggio include:
- valutazione periodica dell’emocromo per rilevare la tossicità midollare (anemia, trombocitopenia, leucopenia);
- monitoraggio della funzione renale (creatinina, eGFR), sebbene la nefrotossicità sia rara con lo schema a 6 cicli;7
- valutazione della xerostomia (secchezza delle fauci), causata dalla captazione del tracciante nelle ghiandole salivari.
La sospensione della terapia può essere considerata in caso di risposta eccezionale (PSA non rilevabile o risposta radiologica completa) prima del sesto ciclo, o deve essere attuata in caso di progressione inequivocabile.
Now loading…
Terapie con emettitori alfa
Nonostante i successi del Lutezio-177, una percentuale significativa di pazienti mostra una resistenza primaria o acquisita al trattamento. In questo scenario, la ricerca si è spostata verso l’uso di emettitori alfa. Le particelle alfa (nuclei di elio) sono molto più pesanti delle particelle beta (elettroni) e possiedono un trasferimento lineare di energia (LET) estremamente elevato (∼100 keV/μm contro i 0.2 keV/μm delle beta). Questo significa che una singola particella alfa può causare rotture multiple e letali del doppio filamento di DNA, rendendo il danno cellulare indipendente dal ciclo cellulare o dall’ossigenazione del tessuto. Inoltre, il raggio d’azione cortissimo (< 100 μm) permette una precisione millimetrica, potenzialmente riducendo la mielotossicità in pazienti con midollo compromesso.
Radio-223 Dicloruro (223Ra)
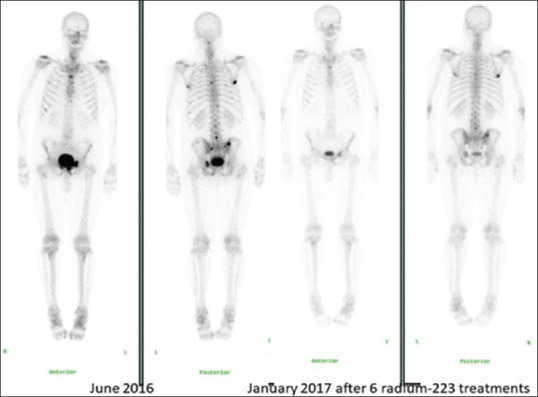
Il Radio-223 è stato il primo emettitore alfa a dimostrare un beneficio in termini di sopravvivenza nel mCRPC con metastasi ossee sintomatiche e assenza di metastasi viscerali note.
Essendo un analogo del calcio, il Radio-223 si lega selettivamente alle aree di formazione ossea reattiva attorno alle metastasi.
Lo studio ALSYMPCA ha stabilito una sopravvivenza globale mediana di 14.9 mesi nel braccio 223Ra rispetto agli 11.3 mesi del placebo. Un’evidenza cruciale emersa dalla pratica reale è che il completamento di tutti i 6 cicli previsti è fondamentale: i pazienti che terminano il trattamento mostrano una sopravvivenza mediana di 31 mesi, contro gli 8-16 mesi di chi interrompe precocemente.8
| Parametro | Radio-223 (223Ra) | Lutezio-177 (177Lu–PSMA) |
|---|---|---|
| Bersaglio | Turnover osseo (analogo del calcio) | Recettore PSMA |
| Tipo di metastasi trattate | Solo ossee | Ossee, linfonodali, viscerali |
| Indicazione principale | mCRPC con sintomi ossei | mCRPC post-chemioterapia e post-ARPI |
| Impatto sul PSA | Spesso minimo o assente | Significativo nella maggior parte dei casi |
Attualmente, il ruolo del Radio-223 dopo l’approvazione del Lutezio-177 è in fase di ridefinizione, ma rimane una scelta elettiva per pazienti con malattia limitata all’osso e scarsa espressione di PSMA.
Attinio-225 (225Ac)
Caricamento…
L’impiego dell’Attinio-225 marcato con PSMA-617 rappresenta una delle frontiere più avanzate della medicina nucleare. A differenza del Radio-223, il ligando PSMA indirizza le particelle alfa contro ogni sito di malattia metastatica.
Studi clinici su pazienti pesantemente pre-trattati e refrattari al Lutezio-177 hanno mostrato risultati sorprendenti, con tassi di risposta biochimica (PSA50) del 63-65% e casi di remissione completa delle immagini PET.9 Tuttavia, la tossicità limitante è la xerostomia severa, dovuta all’elevata energia depositata nelle ghiandole salivari, che può portare alla distruzione irreversibile del tessuto acinare.
La sopravvivenza mediana in contesti di salvataggio si attesta tra i 12 e i 18 mesi.
Piombo-212 (212Pb)
Il Piombo-212 è emerso come un candidato ideale per superare alcuni limiti dell’Attinio-225. Con un’emivita di 10.6 ore, il Piombo-212 si adatta perfettamente alla farmacocinetica dei piccoli ligandi del PSMA, che raggiungono il target tumorale rapidamente.
I risultati dello studio TheraPb (fase Ib), presentati ad ESMO 2025, hanno dimostrato per il 212Pb–ADVC001 un profilo di sicurezza eccezionale senza tossicità limitanti la dose (DLT) e un’attività antitumorale marcata, con l’80% di risposte PSA50 a dosi terapeutiche.
Un vantaggio clinico significativo del Piombo-212 è la minore incidenza di xerostomia grave (prevalentemente di grado 1 e spesso reversibile), unitamente alla possibilità di somministrazione ambulatoriale semplificata.
Gestione della tossicità e protezione degli organi a rischio
L’uso dei radioligandi richiede protocolli rigorosi per la gestione degli effetti collaterali, al fine di preservare la qualità della vita dei pazienti e permettere il completamento dei cicli terapeutici.
Xerostomia e protezione delle ghiandole salivari
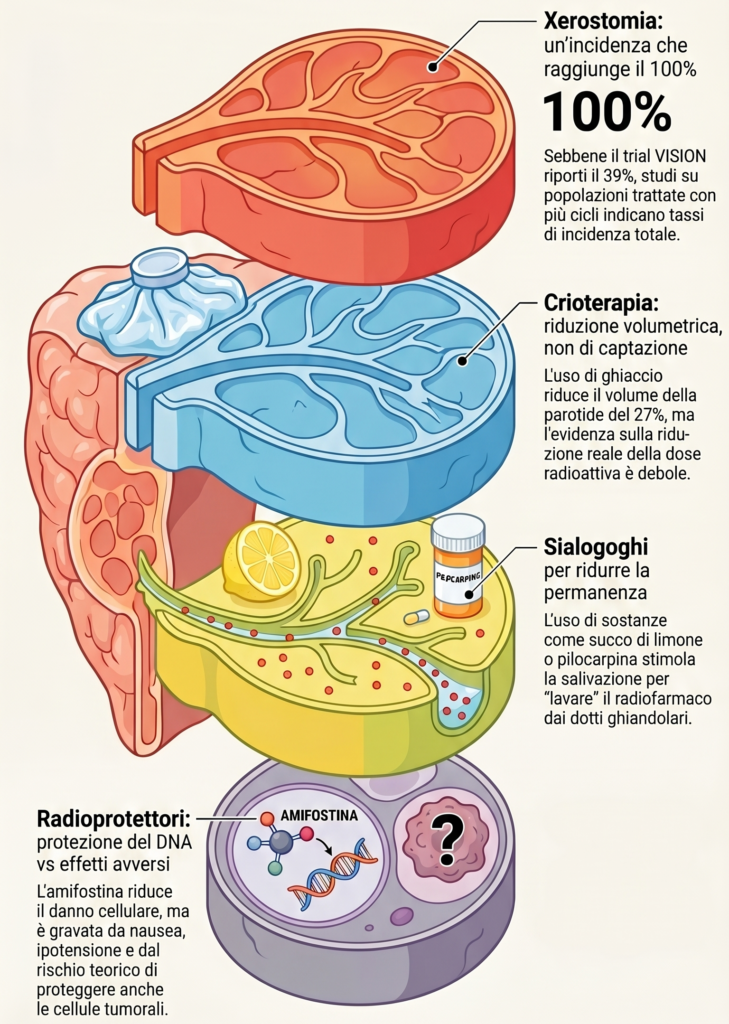
La secchezza delle fauci è la tossicità più frequente e impattante, specialmente con gli emettitori alfa. Nel trial VISION, il tasso di xerostomia di grado 1-2 è stato del 39%, ma studi su popolazioni trattate con più cicli indicano tassi che possono raggiungere il 100%. Diverse strategie sono state testate:
- crioterapia (ice packs): l’applicazione di impacchi di ghiaccio sulle ghiandole parotidi durante l’infusione per indurre vasocostrizione. Sebbene sia una pratica comune, le evidenze sulla sua reale efficacia sono deboli; alcuni studi PET non hanno mostrato una riduzione significativa della captazione del tracciante nonostante una riduzione volumetrica transitoria della ghiandola;10
- sialogoghi: l’uso di sostanze che stimolano la salivazione, come la pilocarpina o il succo di limone, può aiutare a ridurre il tempo di permanenza del radiofarmaco nei dotti ghiandolari, ma i dati clinici sull’efficacia preventiva sono limitati;
- radioprotettori: l’amifostina ha dimostrato capacità di ridurre il danno al DNA indotto dalle radiazioni nelle ghiandole salivari, ma il suo impiego è gravato da effetti collaterali come nausea e ipotensione, e dal timore che possa proteggere anche le cellule tumorali dal trattamento.11
Tossicità ematologica e riserva midollare
La soppressione del midollo osseo è un rischio reale, in particolare per i pazienti con metastasi ossee diffuse (“superscan“). Tuttavia, studi sulla terapia con Attinio-225 hanno dimostrato che la tossicità ematologica grave (grado 3-4) è rara anche in questi scenari, verificandosi in meno del 5% dei pazienti.
I principali predittori di tossicità ematologica sono l’età avanzata, il numero di cicli ricevuti e la presenza di una compromissione renale preesistente che rallenta l’eliminazione del farmaco.
Caricamento….
Sequenziamento terapeutico e integrazione multidisciplinare
La sfida attuale per l’oncologo e il medico nucleare è determinare il momento ottimale per inserire la terapia radioligandica nell’algoritmo di trattamento del mCRPC. Le linee guida EAU 2024/2025 e le indicazioni AIOM 2024 forniscono un quadro strutturato per le decisioni cliniche.
L’algoritmo decisionale nel mCRPC
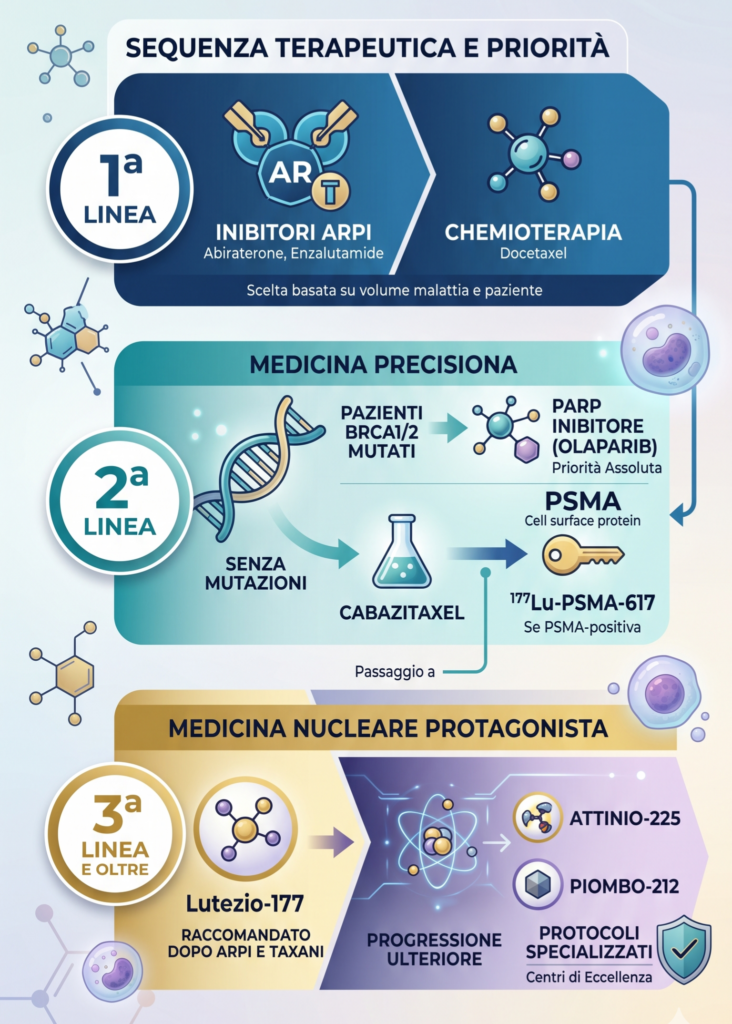
Il trattamento del mCRPC segue generalmente una sequenza che privilegia le terapie con il miglior profilo di efficacia e tollerabilità:
- prima linea: inibitori del segnale del recettore degli androgeni (ARPI come abiraterone o enzalutamide) o chemioterapia con docetaxel, a seconda del volume di malattia e delle caratteristiche del paziente;
- seconda linea: in pazienti con mutazioni dei geni di riparazione del DNA (BRCA1/2), gli inibitori di PARP (come Olaparib) rappresentano la priorità assoluta. In pazienti senza tali mutazioni, si considera il cabazitaxel o il passaggio al 177Lu–PSMA-617 se la malattia è PSMA-positiva;
- terza linea e oltre: la medicina nucleare diventa protagonista. Il Lutezio-177 è raccomandato per i pazienti già trattati con taxani e almeno un ARPI. In caso di progressione ulteriore, l’accesso a protocolli con Attinio-225 o Piombo-212 può essere considerato in centri specializzati.
Terapia Tandem e approcci combinati
Un concetto emergente è la “Terapia Tandem“, che consiste nella co-somministrazione di Lutezio-177 e Attinio-225. Questa strategia mira a sfruttare la penetrazione tessutale delle particelle beta per le masse tumorali voluminose e la letalità delle particelle alfa per le micrometastasi o le cellule resistenti.
I dati preliminari indicano un tasso di risposta PSA50 di circa il 47% e una sopravvivenza mediana di 11.8 mesi in popolazioni molto avanzate, con un profilo di tossicità accettabile e una minore incidenza di xerostomia rispetto alla monoterapia con Attinio.12
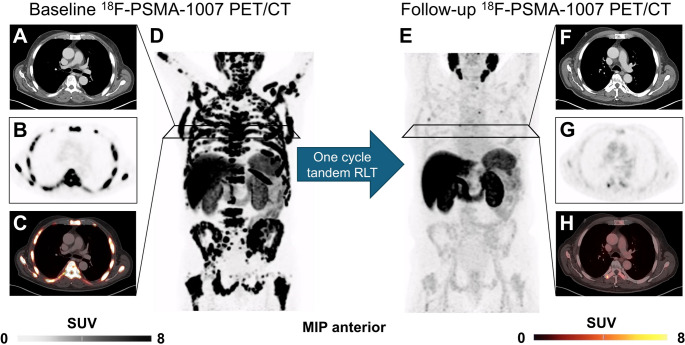
Questo paziente presentava un’elevata espressione di PSMA alla PET pre-terapeutica, in particolare nella colonna toracica e nelle coste. Il valore di captazione standardizzato (SUVmean) era superiore alla soglia di 8,54. Dopo un solo ciclo di RLT tandem, l’antigene prostatico specifico (PSA) è sceso da 674 μg/l a 15,6 μg/l (-97,69%).
n linea con la risposta biochimica, si è verificata anche una risposta parziale basata sull’imaging, con il volume tumorale PSMA-positivo sceso da 2061,17 ml a 3,36 ml (-99,84%) e in assenza di nuove lesioni. Nonostante l’esteso carico tumorale, il paziente non ha manifestato eventi avversi di grado 3 durante il trattamento.
| Strategia di combinazione | Razionale biologico | Risultati attesi |
|---|---|---|
| Beta + Alfa (Tandem) | Controllo simultaneo di macro e micrometastasi | Maggiore durata della risposta |
| RLT + Inibitori di PARP | Sinergia nel danno al DNA e inibizione riparazione | Efficacia in fenotipi aggressivi |
| RLT + Immunoterapia | Induzione di morte cellulare immunogenica | Attivazione risposta immunitaria sistemica |
Now loading…
Aspetti economici e organizzativi della Medicina Nucleare in Italia
L’implementazione delle terapie radioligandiche comporta sfide non solo cliniche ma anche logistiche ed economiche. In Italia, la PET/TC con PSMA è coperta dal Sistema Sanitario Nazionale, garantendo un accesso equo nonostante i costi elevati (circa 1000-1500 euro per esame).
Il costo del trattamento con Lutezio-177 è significativo, ma deve essere valutato nel contesto del beneficio clinico e della riduzione del carico sintomatico per il paziente.
L’accessibilità al trattamento è condizionata dalla disponibilità di centri di medicina nucleare autorizzati alla gestione di radioisotopi terapeutici e dotati di letti di degenza protetta, se richiesto dalle normative locali di radioprotezione. Tuttavia, l’evoluzione verso isotopi con emivita più breve come il Piombo-212 potrebbe facilitare la somministrazione in regime ambulatoriale, riducendo la pressione sulle infrastrutture ospedaliere e migliorando la qualità della vita dei pazienti.
Conclusioni e prospettive future
Caricamento…
La medicina nucleare ha ridefinito gli standard di cura per il tumore della prostata metastatico, portando la precisione molecolare dalla diagnostica alla terapia. Il Lutezio-177 si è consolidato come un’opzione terapeutica fondamentale capace di prolungare la vita e migliorare il benessere dei pazienti con mCRPC. L’ascesa delle terapie alfa-mirate promette di superare le resistenze biologiche attuali, offrendo soluzioni efficaci anche nelle fasi più critiche della malattia.
Le direzioni future della ricerca si stanno concentrando su due fronti principali:
- l’anticipazione della terapia: trial clinici come PSMAfore e altri stanno valutando l’efficacia del Lutezio-177 in contesti pre-chemioterapici e nel carcinoma prostatico metastatico sensibile alla castrazione (mHSPC), dove l’eradicazione precoce della malattia potrebbe portare a risposte molto più durature;
- la personalizzazione dosimetrica: il passaggio da dosi standard a dosi personalizzate basate sulla captazione reale del tumore (dosimetria individuale) consentirà di massimizzare l’efficacia terapeutica minimizzando gli effetti collaterali sugli organi a rischio.
In definitiva, il ruolo della medicina nucleare è destinato ad espandersi, richiedendo una collaborazione sempre più stretta tra oncologi, urologi, radioterapisti e medici nucleari all’interno di team multidisciplinari capaci di guidare il paziente attraverso le complesse sequenze terapeutiche dell’oncologia moderna.
Fonti:
- Targeted Alpha Therapy: Exploring the Clinical Insights into [225Ac … ↩︎
- Therapeutic outcomes of ²²⁵Ac/¹⁷⁷Lu-PSMA combination therapy in advanced metastatic Castration-Resistant prostate cancer: A systematic review and Meta-Analysis – PMC ↩︎
- Long-Term Safety and Survival Outcomes of [225Ac]Ac-PSMA (Prostate-Specific Membrane Antigen) and [225Ac]Ac-/[177Lu]Lu-PSMA (TANDEM) Radioligand Therapy (PRLT) in Metastatic Castration-Resistant Prostate Cancer – MDPI ↩︎
- Lutetium-177-PSMA-617: A Vision of the Future – PMC ↩︎
- First-in-Human Phase 0 Study of AB001, a Prostate-Specific Membrane Antigen–Targeted 212Pb Radioligand, in Patients with Metastatic Castration-Resistant Prostate Cancer | Journal of Nuclear Medicine ↩︎
- Tandem Isotope Therapy with 225Ac- and 177Lu-PSMA-617 in a Murine Model of Prostate Cancer | Journal of Nuclear Medicine ↩︎
- Joint EANM/SNMMI procedure guideline for the use of 177Lu-labeled PSMA-targeted radioligand-therapy (177Lu-PSMA-RLT) – PMC ↩︎
- Quantifying the survival benefit of completing all the six cycles of radium-223 therapy in patients with castrate-resistant prostate cancer with predominant bone metastases – PMC ↩︎
- Time for action: actinium-225 PSMA-targeted alpha therapy for metastatic prostate cancer – a systematic review and meta-analysis – Theranostics ↩︎
- 68Ga-PSMA PET/CT: effect of external cooling on salivary gland uptake – PMC ↩︎
- Localized Delivery of Amifostine Enhances Salivary Gland Radioprotection – PMC ↩︎
- Refining the clinical utility of [177Lu]Lu/[225Ac]Ac-PSMA tandem RLT in patients with metastatic castration resistant prostate cancer – PMC ↩︎