L’osteoporosi si definisce come una patologia sistemica dell’apparato scheletrico, caratterizzata da una compromissione della resistenza ossea che predispone un individuo a un aumentato rischio di fratture.1 2 Tale resistenza riflette l’integrazione di due fattori principali: la densità ossea e la qualità ossea.
La densità ossea viene espressa come grammi di minerale per volume o per area, mentre la qualità ossea si riferisce all’architettura, al turnover, all’accumulo di micro-danni e alla mineralizzazione.
Caricamento…
Dal punto di vista epidemiologico, l’osteoporosi rappresenta una sfida di salute pubblica di proporzioni crescenti, influenzando significativamente la morbilità e la mortalità della popolazione anziana.3 In Italia, la prevalenza è stimata in circa 4,5 milioni di individui, di cui la stragrande maggioranza sono donne in post-menopausa. La rilevanza clinica della patologia risiede quasi esclusivamente nelle sue complicanze fratturative, le quali comportano costi sociali enormi e una drastica riduzione della qualità della vita.
- Classificazione e inquadramento clinico dell’osteoporosi
- Principi fisici della Mineralometria Ossea Computerizzata (MOC)
- L’equazione dell’attenuazione e il calcolo della BMD
- Tecniche di generazione del fascio duale
- Tomografia Computerizzata Quantitativa (QCT) e pQCT
- Calibrazione e Unità Hounsfield
- Ultrasonografia Ossea Quantitativa (QUS)
- Parametri QUS: SOS e BUA
- Indicazioni cliniche e criteri di accesso
- Soggetti a rischio e tempistiche
- Protocolli di acquisizione e criteri di qualità
- Scansione della colonna lombare (L1-L4)
- Scansione del femore prossimale
- Sorgenti d’errore e limiti della metodica
- Artefatti degenerativi e calcificazioni
- Fattori legati al paziente
- Dosimetria e radioprotezione
- Confronto delle dosi efficaci
- Obblighi del D.Lgs 101/2020 nel referto
- La refertazione e l’interpretazione clinica
- Requisiti minimi del referto (ISCD/SIOMMMS)
- Il ruolo dello Z-score
- Conclusioni e prospettive
Classificazione e inquadramento clinico dell’osteoporosi
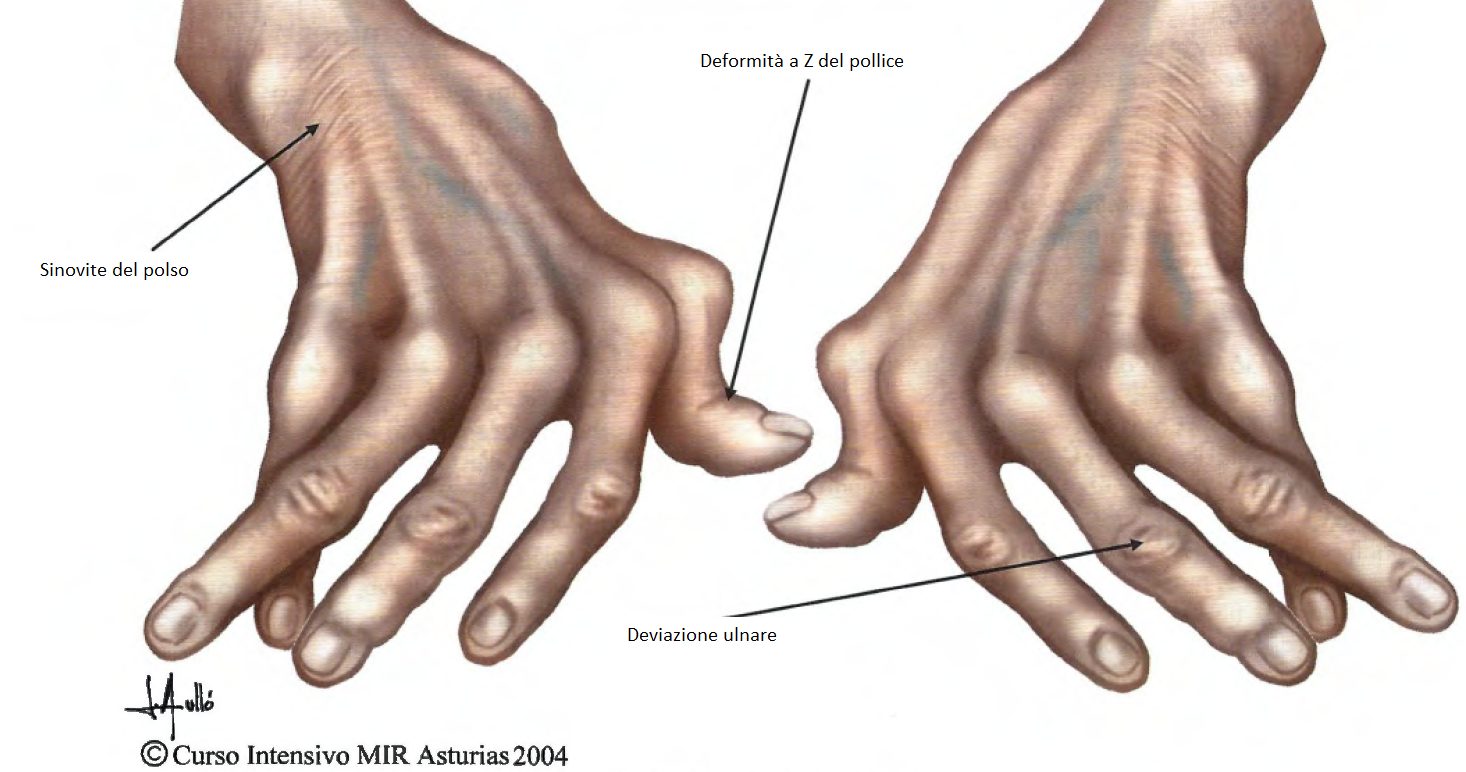
L’osteoporosi non deve essere considerata una condizione monolitica, bensì il risultato finale di diversi processi fisiopatologici. La classificazione clinica distingue primariamente tra forme primitive e forme secondarie.
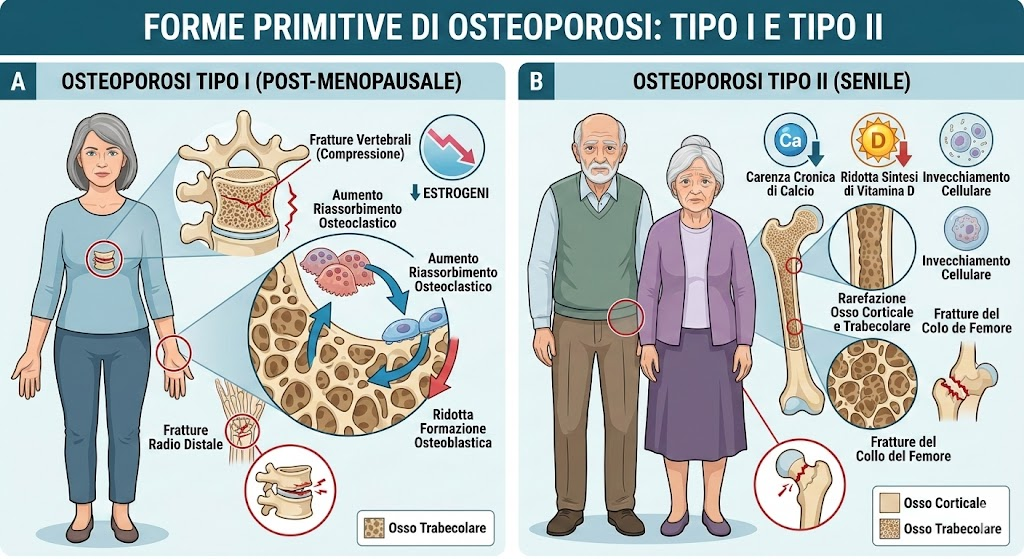
Le forme primitive comprendono l’osteoporosi post-menopausale (Tipo I) e l’osteoporosi senile (Tipo II):
- l’osteoporosi di Tipo I è strettamente legata al calo degli estrogeni, il quale determina un’accelerazione del turnover osseo con una prevalenza dell’attività riassorbitiva degli osteoclasti rispetto a quella formativa degli osteoblasti. Questo processo colpisce elettivamente l’osso trabecolare, spiegando l’elevata incidenza di fratture vertebrali e del radio distale in questa popolazione;
- l’osteoporosi di Tipo II, o senile, colpisce entrambi i sessi dopo i 70 anni ed è legata a una carenza cronica di calcio, ridotta sintesi di vitamina D e invecchiamento cellulare, interessando sia l’osso corticale che quello trabecolare.
Le forme secondarie di osteoporosi derivano da una vasta gamma di condizioni mediche e trattamenti farmacologici che interferiscono negativamente con il metabolismo osseo.
L’identificazione di queste forme è cruciale poiché il trattamento della causa sottostante può spesso arrestare o invertire la perdita di massa ossea.
| Categoria fisiopatologica | Esempi di condizioni e farmaci |
|---|---|
| Malattie endocrine | Iperparatiroidismo primario, sindrome di Cushing, ipertiroidismo, ipogonadismo, diabete di tipo 1 e 2 |
| Malattie gastrointestinali | Celiachia, malattie infiammatorie croniche intestinali (MICI), chirurgia bariatrica, malassorbimento |
| Malattie ematologiche e neoplastiche | Mieloma multiplo, mastocitosi sistemica, leucemie, linfomi |
| Malattie renali | Insufficienza renale cronica, acidosi tubulare renale, osteodistrofia uremica |
| Farmaci osteopenizzanti | Glucocorticoidi, eparina, anticonvulsivanti, inibitori dell’aromatasi, metotrexato, diuretici dell’ansa |
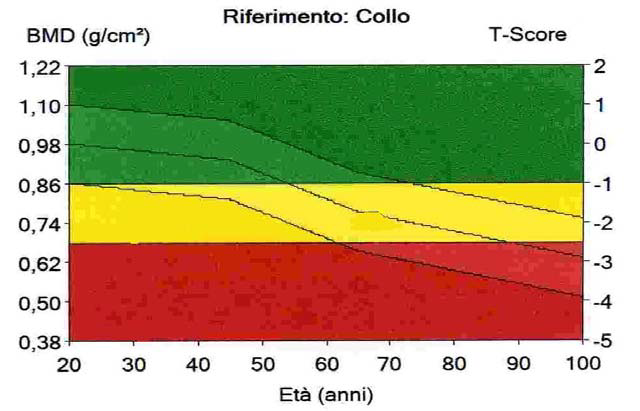
La diagnosi densitometrica di osteoporosi si basa sui criteri stabiliti dall’Organizzazione Mondiale della Sanità (OMS), che utilizza il T-score come parametro di riferimento.4
Il T-score è definito come il numero di deviazioni standard (DS) di cui il valore di densità minerale ossea (BMD) del paziente differisce dal valore medio di una popolazione di riferimento di giovani adulti sani (20-29 anni) dello stesso sesso.
| Classificazione OMS | Criterio T-score |
|---|---|
| Normalità | T-score ≥ -1.0 DS |
| Osteopenia (bassa massa ossea) | T-score compreso tra -1.0 e -2.5 DS |
| Osteoporosi | T-score ≤ -2.5 DS |
| Osteoporosi severa (conclamata) | T-score ≤ -2.5 DS in presenza di una o più fratture da fragilità |
È fondamentale sottolineare che il T-score non è l’unico determinante del rischio di frattura. Molte fratture da fragilità si verificano in soggetti con valori di BMD nel range dell’osteopenia, rendendo necessaria una valutazione clinica globale che includa fattori di rischio indipendenti dalla densità ossea.5 Tra questi, l’età avanzata, una precedente frattura da fragilità e la familiarità per frattura di femore sono i predittori più potenti.6
Principi fisici della Mineralometria Ossea Computerizzata (MOC)
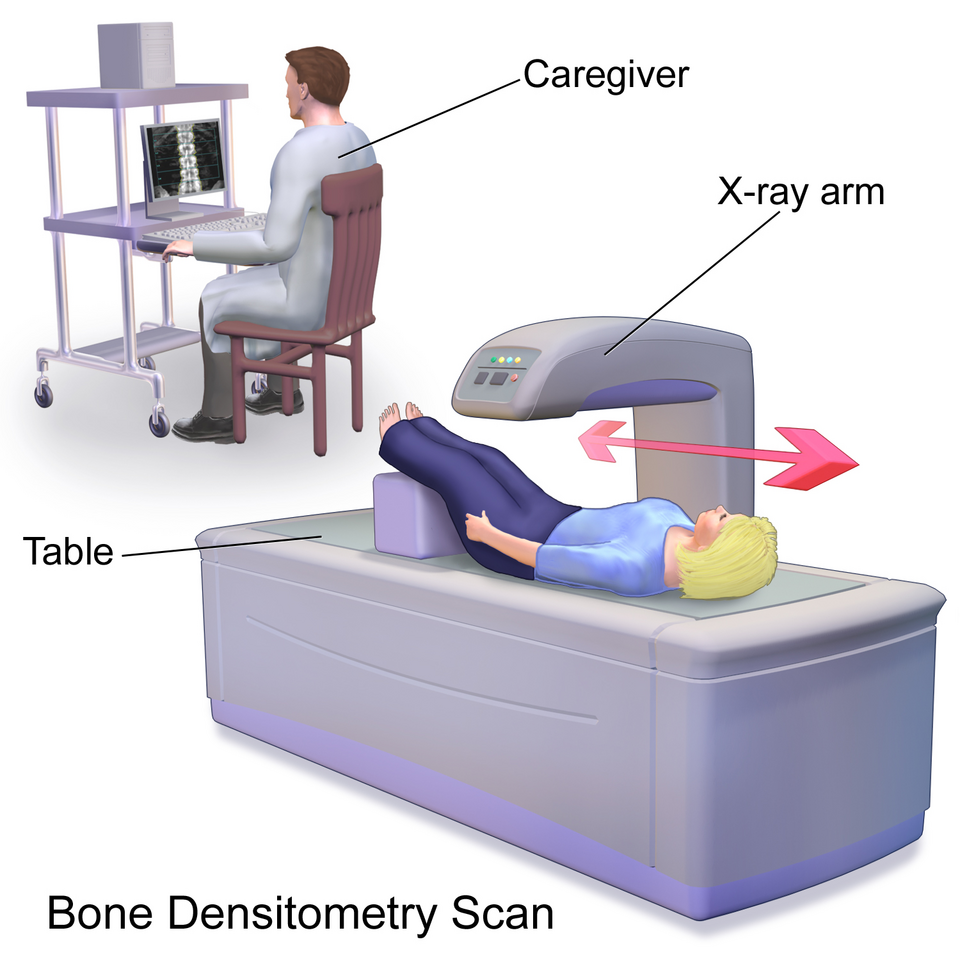
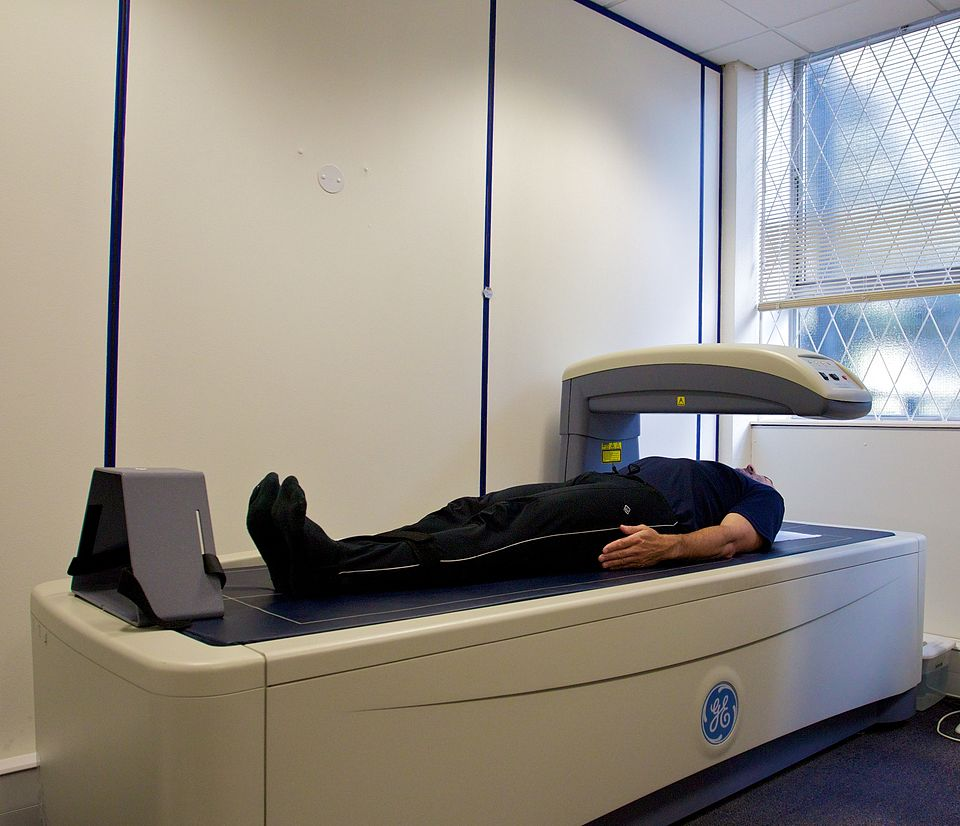
La tecnica di riferimento per la misurazione della BMD è la Dual-Energy X-ray Absorptiometry (DXA).7
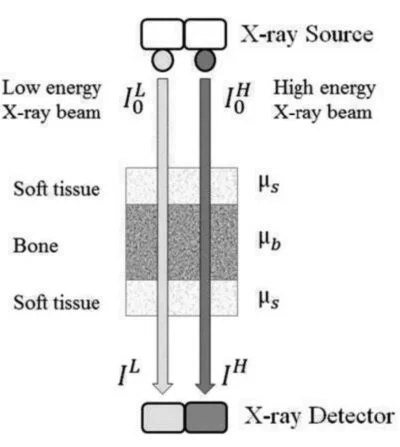
Il principio fisico su cui si basa la DXA è l’attenuazione differenziale di un fascio di raggi X a due diversi livelli energetici. Quando un fascio di fotoni attraversa il corpo umano, l’attenuazione subita dipende dall’energia dei fotoni stessi, dallo spessore del tessuto e dalla composizione atomica del materiale attraversato (numero atomico efficace).8
L’equazione dell’attenuazione e il calcolo della BMD
L’attenuazione dei raggi X attraverso un mezzo può essere descritta dalla legge di Beer-Lambert:
dove I è l’intensità del fascio trasmesso, I0 l’intensità iniziale, μ il coefficiente di attenuazione lineare e d lo spessore del materiale.
Poiché il corpo umano è composto da diversi tessuti, in particolare tessuto osseo e tessuti molli (muscolo e grasso), un singolo raggio energetico non è sufficiente per distinguere tra una variazione di spessore del tessuto molle e una variazione della densità minerale ossea.9
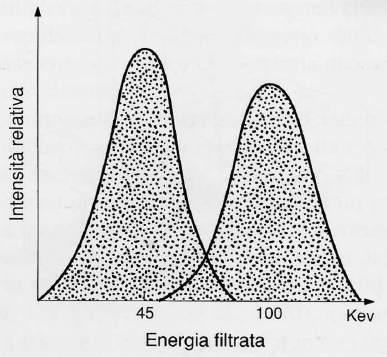
L’utilizzo di due energie (tipicamente picchi intorno a 40 keV e 100 keV) permette di creare un sistema di due equazioni in due incognite, consentendo di sottrarre matematicamente il contributo dei tessuti molli e isolare l’assorbimento dovuto esclusivamente al minerale osseo.
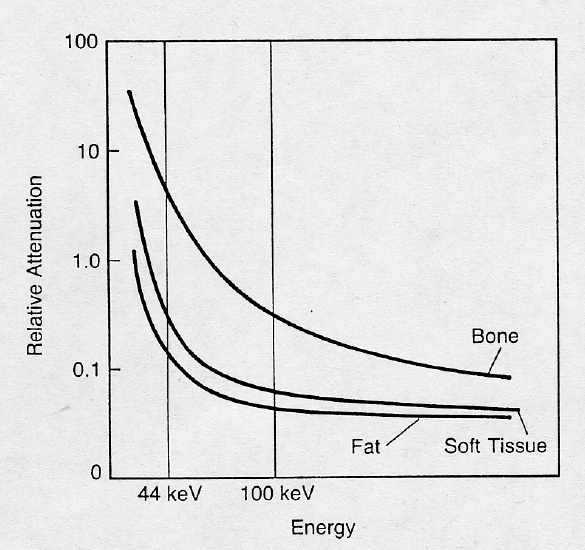
Il software calcola quindi il Bone Mineral Content (BMC, espresso in grammi) e la Bone Area (cm2), derivando la Bone Mineral Density (BMD) come rapporto tra i due (g/cm2). È importante notare che la DXA fornisce una densità areale, non volumetrica; pertanto, le ossa di dimensioni maggiori possono apparire artificialmente più dense di quanto non siano realmente, un limite intrinseco della proiezione bidimensionale.10
Tecniche di generazione del fascio duale
Esistono due metodi principali per generare le due energie necessarie per la DXA:
- commutazione rapida del potenziale del tubo (Voltage Switching): il tubo radiologico alterna rapidamente la tensione tra 100 kVp e 140 kVp. Questo metodo richiede sistemi elettronici complessi per stabilizzare l’emissione e il rilevamento sincronizzato;
- filtrazione K-edge (rare-earth filtration): il tubo opera a tensione costante, ma il fascio passa attraverso un filtro di terre rare (come il cerio o il gadolinio) che presenta un’improvvisa variazione di assorbimento (K-edge). Questo divide lo spettro di emissione in due picchi energetici distinti.
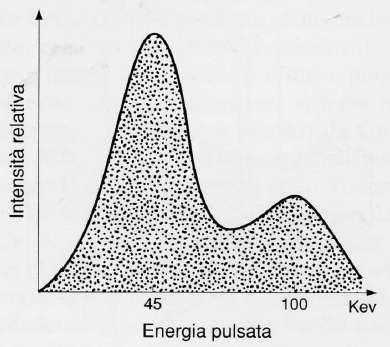
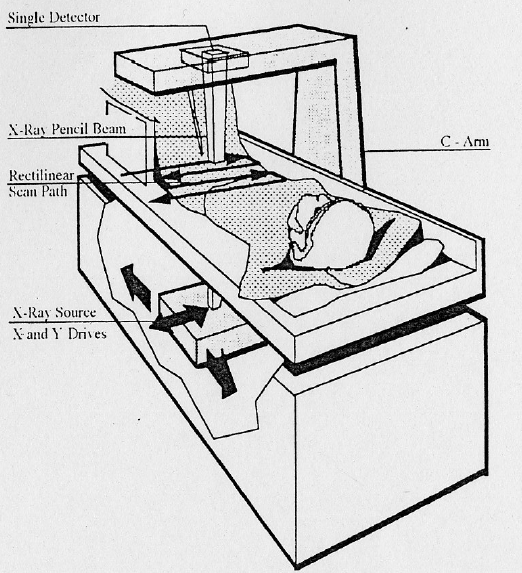
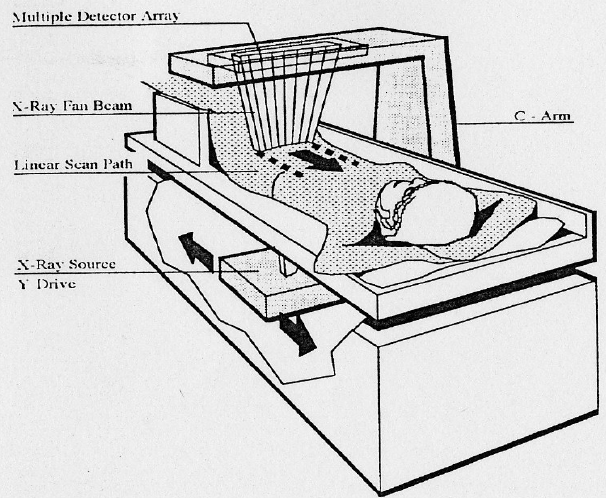
La tecnologia dei rivelatori si è evoluta dai sistemi a raggio sottile (“pencil beam“), che scansionano il corpo pixel per pixel con un unico rivelatore, ai sistemi a raggio a ventaglio (“fan beam“), che utilizzano una schiera di rivelatori per acquisire un’intera riga di dati simultaneamente.11 Sebbene i sistemi fan beam siano molto più veloci, introducono una leggera distorsione geometrica e richiedono algoritmi di correzione per l’ingrandimento, oltre a comportare una dose di radiazioni leggermente superiore.
Caricamento…
Tomografia Computerizzata Quantitativa (QCT) e pQCT
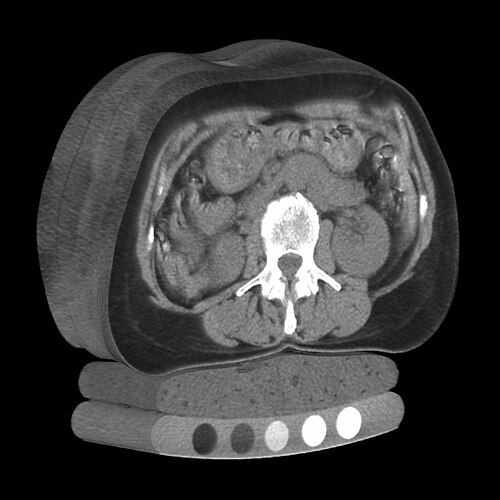
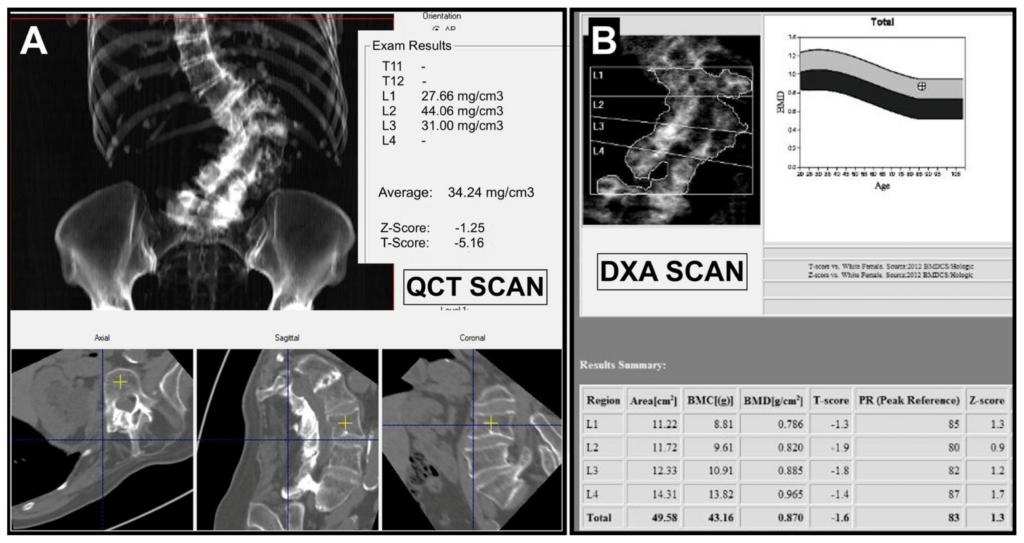
La Tomografia Computerizzata Quantitativa (QCT) rappresenta un’alternativa tridimensionale alla DXA. Mentre la DXA fornisce una misura bidimensionale che somma l’osso corticale e quello trabecolare, la QCT è in grado di isolare spazialmente l’osso trabecolare all’interno del corpo vertebrale.12
Questo è clinicamente significativo perché l’osso trabecolare ha un turnover metabolico circa otto volte superiore rispetto all’osso corticale, rendendolo più sensibile ai cambiamenti precoci indotti da malattie o terapie.13
Calibrazione e Unità Hounsfield

Il processo QCT trasforma uno scanner TC convenzionale in uno strumento densitometrico attraverso l’uso di un fantoccio di calibrazione (phantom) posizionato sotto il paziente durante l’acquisizione.
Il phantom contiene concentrazioni note di idrossiapatite di calcio (CaHA) espresse in mg/cm3. Il software correla i valori di attenuazione (espressi in Unità Hounsfield, HU) dei pixel ossei con quelli del phantom, generando una curva di calibrazione che permette di convertire gli HU in densità minerale volumetrica (vBMD).14 15
| Parametro | DXA (MOC) | QCT (vBMD) |
|---|---|---|
| Unità di misura | g/cm2 (areale) | mg/cm3 (volumetrica) |
| Distinzione corticale/trabecolare | no (somma dei due) | sì (isolamento selettivo) |
| Sensibilità agli osteofiti | elevata (sovrastima BMD) | bassa (esclusione spaziale) |
| Dose di radiazioni | molto bassa (∼ 1-15 μSv) | moderata (200-400 μSv) |
La QCT periferica (pQCT) applica gli stessi principi a siti come l’avambraccio o la tibia, permettendo non solo la misurazione della densità ma anche l’analisi della geometria ossea e degli indici di resistenza meccanica (come lo Stress-Strain Index, SSI) con dosi di radiazioni estremamente contenute.
Ultrasonografia Ossea Quantitativa (QUS)
L’ultrasonografia quantitativa (QUS) non utilizza radiazioni ionizzanti e valuta le proprietà dell’osso attraverso la propagazione di onde acustiche ad alta frequenza (solitamente nel range 0.1-1.0 MHz).16
Il sito di misurazione più comune è il calcagno, scelto per la sua elevata percentuale di osso trabecolare e per l’accessibilità anatomica.
Parametri QUS: SOS e BUA
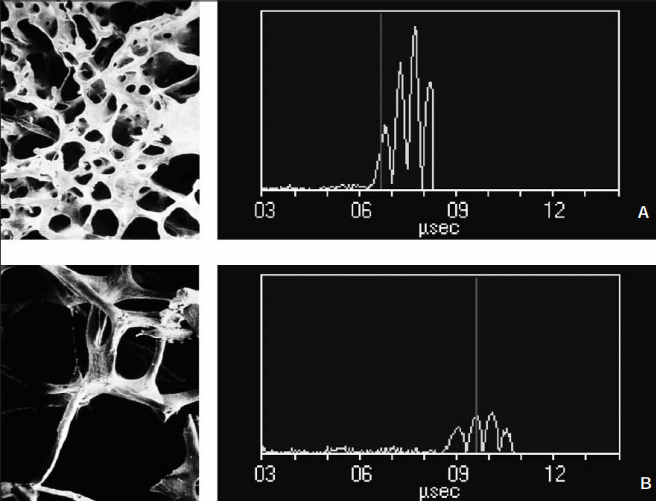
La QUS fornisce informazioni che vanno oltre la semplice densità minerale, riflettendo anche proprietà qualitative come l’elasticità e l’integrità strutturale delle trabecole. I due parametri principali sono:
- Speed of Sound (SOS): misura la velocità di attraversamento dell’onda attraverso l’osso (m/s). La velocità è influenzata dalla densità e dalle proprietà elastiche (modulo di Young) del tessuto. In un osso osteoporotico, la velocità diminuisce a causa della perdita di minerale e della riduzione del modulo elastico;
- Broadband Ultrasound Attenuation (BUA): descrive la perdita di energia (attenuazione) dell’onda sonora mentre attraversa l’osso, misurata in dB/MHz. L’attenuazione è causata principalmente dallo scattering (dispersione) delle onde sulle trabecole ossee; una struttura trabecolare rarefatta produce meno attenuazione rispetto a una fitta.
Molti sistemi combinano SOS e BUA in un unico valore, il “Stiffness Index” o “Quantitative Ultrasound Index” (QUI), che offre una precisione clinica superiore rispetto ai singoli parametri.
Sebbene la QUS sia un eccellente predittore del rischio di frattura, non può essere utilizzata per la diagnosi formale di osteoporosi secondo i criteri OMS, i quali rimangono legati esclusivamente alla tecnica DXA.17
Caricamento....
Indicazioni cliniche e criteri di accesso
In Italia, l’accesso alla densitometria ossea è regolato da linee guida nazionali (SIOMMMS) e dai Livelli Essenziali di Assistenza (LEA), che definiscono le categorie di pazienti per le quali l’esame è clinicamente giustificato e rimborsabile.
Soggetti a rischio e tempistiche
Le indicazioni principali includono:
- donne di età > 65 anni e uomini > 70 anni, indipendentemente dai fattori di rischio;
- soggetti con pregresse fratture da fragilità (vertebrali, femorali, di polso o omero);
- pazienti in terapia cronica con farmaci che inducono perdita ossea, in particolare glucocorticoidi (equivalenti a ≥ 5 mg/die di prednisone per > 3 mesi);
- condizioni patologiche associate a osteoporosi secondaria (iperparatiroidismo, celiachia, ipogonadismo);
- donne in post-menopausa precoce (< 45 anni) o con periodi prolungati di amenorrea (> 6 mesi).
Il monitoraggio densitometrico non deve essere eseguito a intervalli troppo brevi. Generalmente, un intervallo di 18-24 mesi è appropriato per valutare la risposta alla terapia o l’evoluzione della patologia, poiché le variazioni biologiche della BMD sono lente.
Un follow-up più frequente (12 mesi) può essere considerato solo in casi di perdita ossea estremamente rapida, come l’inizio di terapie steroidee ad alte dosi o dopo trapianti d’organo.
Protocolli di acquisizione e criteri di qualità
L’affidabilità della DXA dipende criticamente dal rigoroso rispetto dei protocolli di acquisizione. Gli errori di posizionamento sono la causa principale di referti non accurati.18
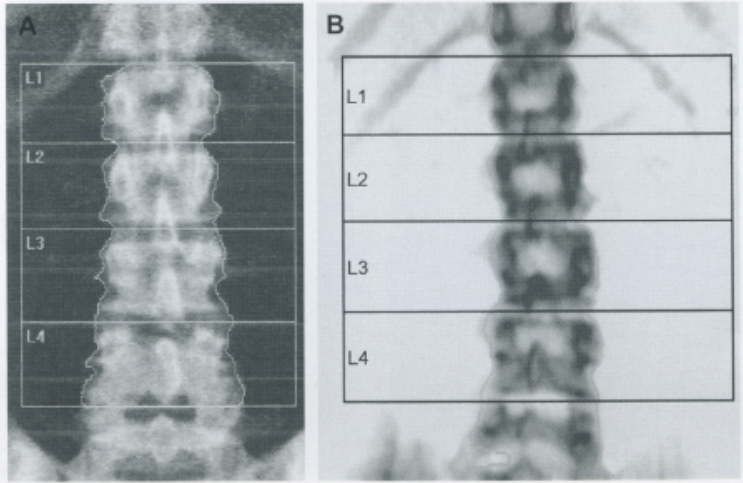
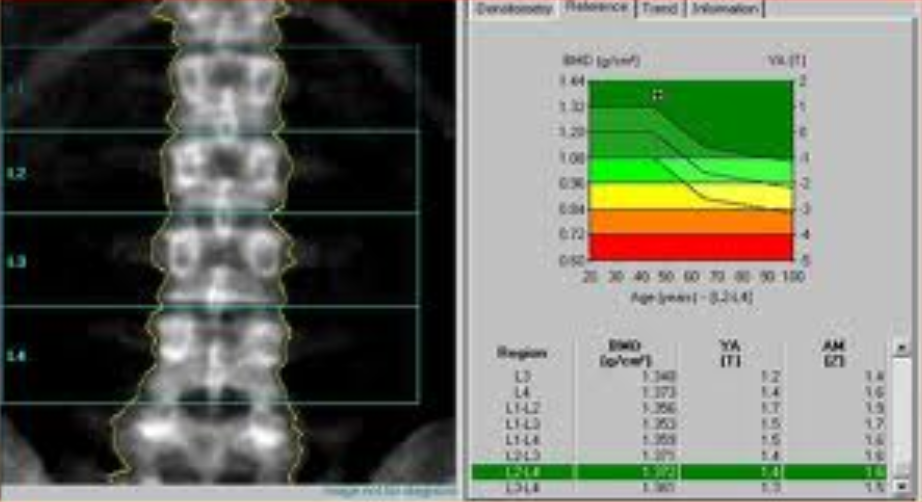
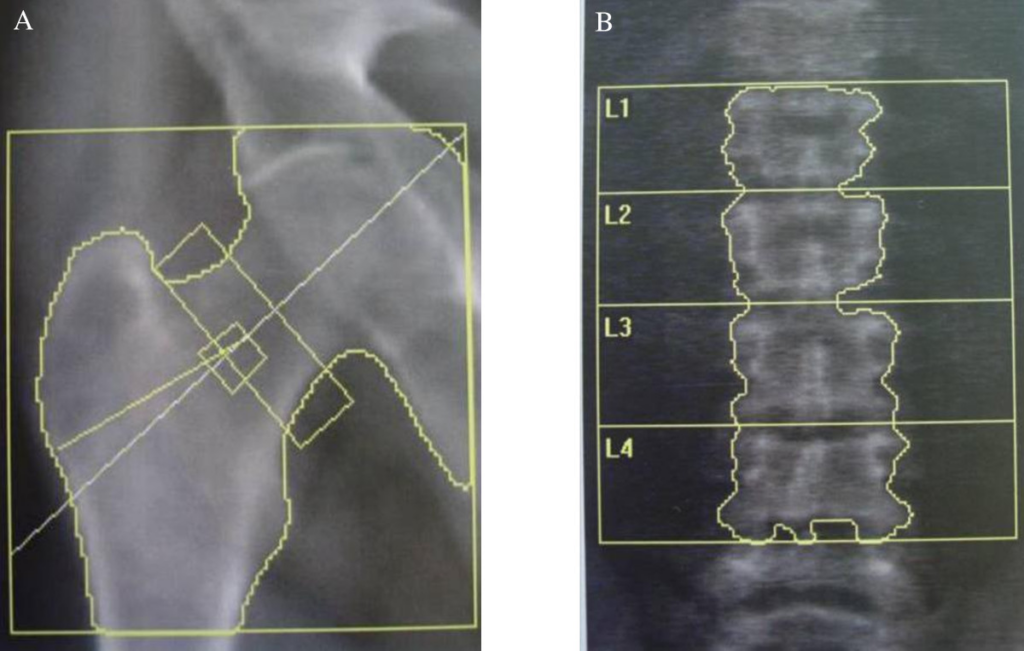
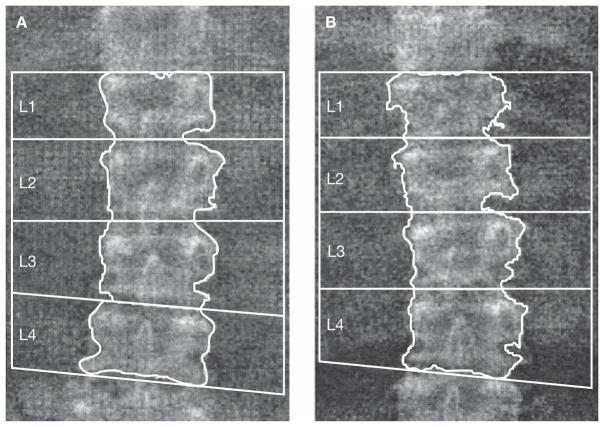
Scansione della colonna lombare (L1-L4)
Il paziente deve essere posizionato supino con i femori flessi a 90 gradi su un apposito cubo di gommapiuma per ridurre la lordosi lombare e appiattire la colonna sul tavolo di scansione.19
L’immagine acquisita deve essere centrata, con la colonna parallela ai bordi e deve includere la parte superiore delle creste iliache e l’ultima coppia di coste (T12) come punti di riferimento anatomico.20 Un’analisi corretta richiede l’inclusione di almeno due vertebre contigue.
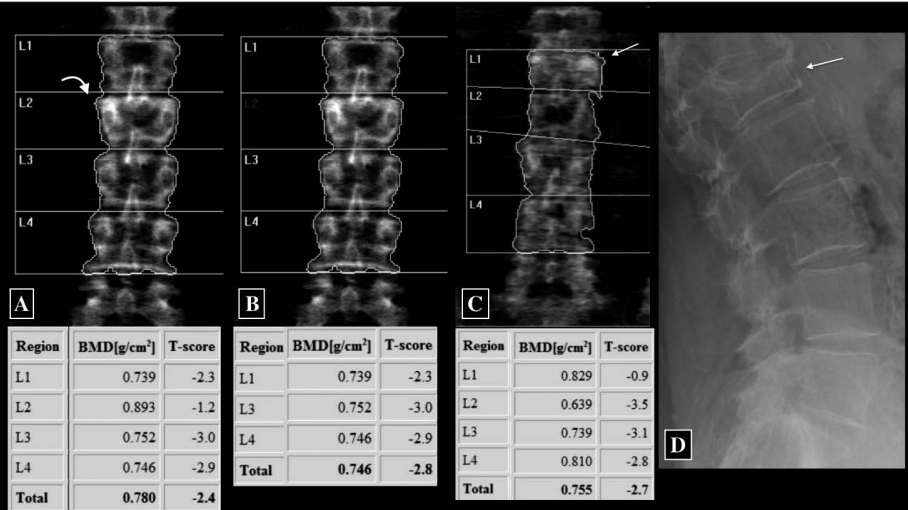
Una vertebra deve essere esclusa se è presente una frattura, un’alterazione strutturale grossolana (come un emangioma o esiti chirurgici) o se il suo T-score differisce di oltre 1.0 DS rispetto alle vertebre adiacenti.
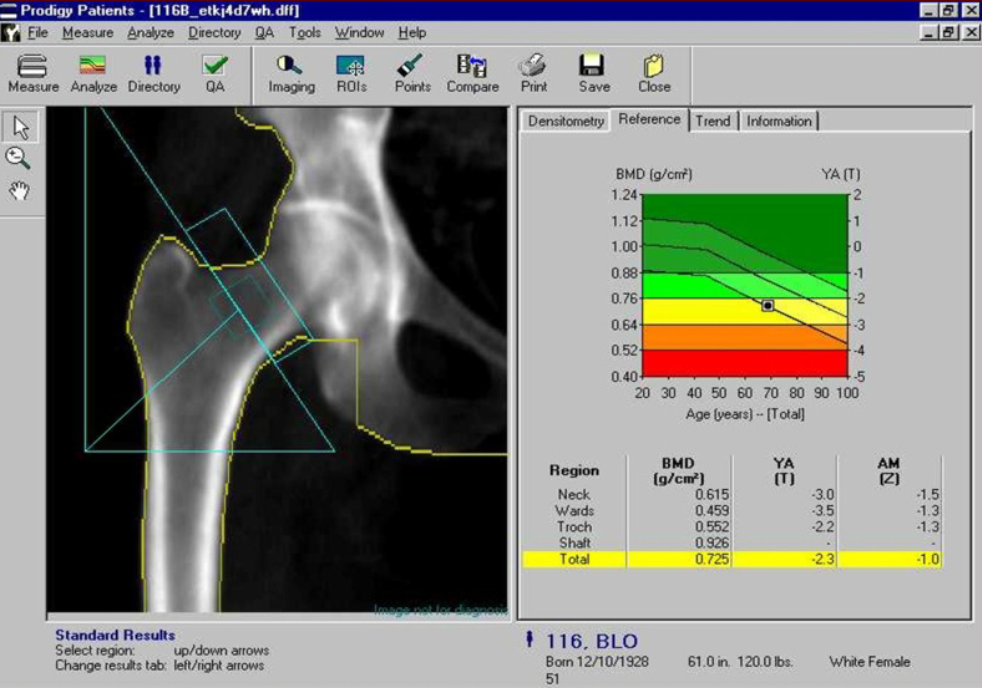
Scansione del femore prossimale
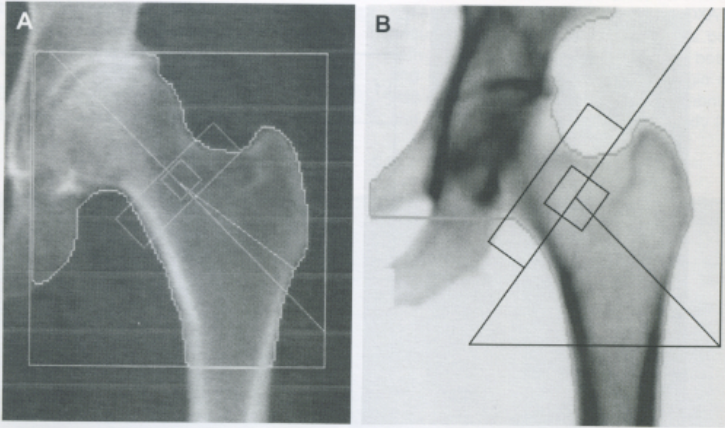
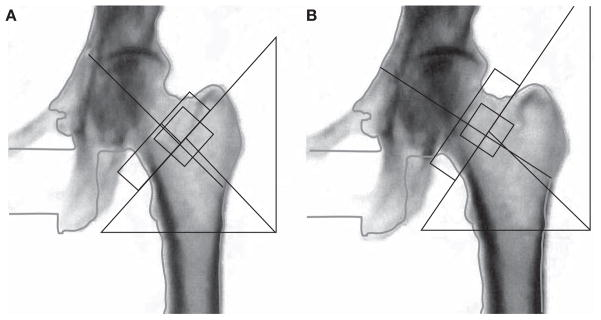
Per il femore, è essenziale indurre una rotazione interna dell’arto di circa 15-25 gradi utilizzando un apposito posizionatore per i piedi. Questa manovra serve a distendere il collo femorale, portandolo parallelo al piano di scansione e riducendo la sovrapposizione del grande trocantere.
Il piccolo trocantere deve essere minimamente visibile o assente in una scansione eseguita correttamente.
Le regioni di interesse (ROI) diagnostiche sono il “collo femorale” (Femoral Neck) e il “femore totale” (Total Hip). Il valore di BMD più basso tra i due deve essere utilizzato per la classificazione densitometrica.
L’area di Ward non deve essere usata per la diagnosi a causa della sua elevata variabilità e piccola dimensione.
Sorgenti d’errore e limiti della metodica
Nonostante la DXA sia il gold standard, essa è soggetta a numerosi artefatti che possono portare a una sovrastima o sottostima della densità ossea, influenzando le decisioni cliniche.
Artefatti degenerativi e calcificazioni
Dopo i 65 anni, la colonna lombare diventa spesso inaffidabile per la diagnosi a causa dell’artrosi.
Gli osteofiti, la sclerosi delle faccette articolari e le calcificazioni dei legamenti vengono proiettati nell’area di scansione e aggiungono “massa minerale” che non appartiene al corpo vertebrale, portando a un T-score falsamente elevato.21
Allo stesso modo, le calcificazioni dell’aorta addominale, visibili come formazioni radiopache davanti alla colonna, contribuiscono alla sovrastima della BMD.
In questi casi, la valutazione del femore prossimale è considerata più accurata per la diagnosi di osteoporosi sistemica.
Fattori legati al paziente
L’obesità estrema può degradare la qualità dell’immagine a causa dello scattering dei fotoni nei tessuti molli addominali, aumentando il rumore di fondo e riducendo la precisione. Al contrario, pazienti estremamente magri o con bassa statura possono ricevere una diagnosi di osteoporosi dovuta puramente a un effetto geometrico di sottostima dell’area ossea (effetto “small bone“).
Altre sorgenti di errore includono la presenza di mezzi di contrasto radiologici residui (bario, iodio) o pregressi interventi chirurgici con mezzi di sintesi metallici.
Now loading…
Dosimetria e radioprotezione
In conformità con il decreto legislativo 101/2020, che recepisce la direttiva Euratom 2013/59, ogni esposizione medica deve essere giustificata e ottimizzata.22
La densitometria ossea DXA si distingue per livelli di esposizione estremamente contenuti, rendendola una delle procedure radiologiche più sicure.
Confronto delle dosi efficaci
La dose efficace per un esame DXA standard (colonna + femore) è compresa tra 1 e 15 microSievert (μSv). Per contestualizzare questi valori, è possibile confrontarli con altre fonti di esposizione:
| Procedura / Fonte | Dose Efficace approssimativa (μSv) |
|---|---|
| Radiazione di fondo naturale (giornaliera) | ∼ 7-10 |
| Volo transatlantico | ∼ 30-50 |
| Radiografia del torace (2 proiezioni) | ∼ 50-100 |
| Densitometria DXA | 1-15 |
| Tomografia Computerizzata Quantitativa (QCT) | 200-400 |
Obblighi del D.Lgs 101/2020 nel referto
La normativa vigente impone che il referto di ogni prestazione radiologica includa l’indicazione della dose di radiazioni.
Nelle more di una definizione precisa dei parametri dosimetrici per ogni specifica apparecchiatura, la Federazione delle Società Scientifiche Radiologiche (come la SIRM) ha proposto l’adozione delle “Classi di Dose“.
La densitometria ossea DXA ricade pienamente nella Classe I (dose efficace < 1 mSv). Il referto deve pertanto riportare esplicitamente la dicitura: “Classe di dose secondo l’art. 161 del D.Lgs 101/2020: Classe I“. Questo garantisce la trasparenza verso il paziente e il rispetto dei requisiti legali di tracciabilità dell’esposizione.
Now loading…
La refertazione e l’interpretazione clinica
Un referto densitometrico di alta qualità non deve limitarsi a riportare i valori numerici, ma deve fornire un’interpretazione che guidi il clinico nella gestione del paziente.
Requisiti minimi del referto (ISCD/SIOMMMS)
Secondo le posizioni ufficiali della International Society for Clinical Densitometry (ISCD) e della SIOMMMS, il referto deve contenere:
- identificazione tecnica: modello dello strumento e versione del software;
- dati biometrici: età, sesso ed etnia del paziente (essenziali poiché i database di riferimento variano per questi parametri);
- dettaglio delle ROI: indicazione chiara delle vertebre incluse/escluse e del lato del femore scansionato;
- parametri quantitativi: BMD assoluta (g/cm2), T-score (per donne post-menopausa e uomini > 50 anni) e Z-score;
- giudizio diagnostico: classificazione secondo i criteri OMS;
- analisi del trend: se è disponibile un esame precedente, il referto deve indicare se la variazione della BMD è statisticamente significativa. Questo calcolo deve basarsi sulla precisione in vivo del centro, definita come “Minima Variazione Significativa” (Least Significant Change, LSC). Una variazione è considerata reale solo se supera il valore di LSC (tipicamente intorno al 3-5%).
Il ruolo dello Z-score
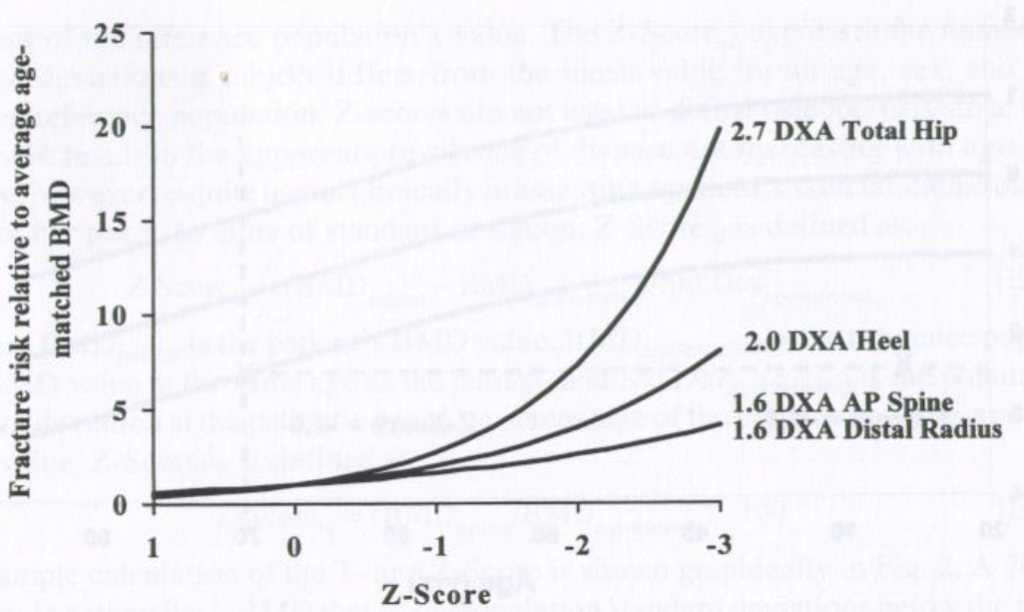
Mentre il T-score è il parametro per la diagnosi di osteoporosi nell’anziano e misura la differenza tra la densità ossea misurata nel paziente e il valore medio di giovani adulti dello stesso sesso, lo Z-score è fondamentale per la valutazione di bambini, adolescenti, donne in pre-menopausa e uomini sotto i 50 anni. Misura (in DS) la differenza tra la densità ossea del paziente e il valore medio di soggetti sani di pari età e sesso.
In queste popolazioni, non si dovrebbe usare il termine “osteoporosi” basandosi solo sulla densitometria.
Un valore di Z-score ≤−2.0 viene definito come “densità ossea inferiore al range atteso per l’età” e deve spingere il medico a ricercare attivamente cause secondarie di perdita ossea o mancato raggiungimento del picco di massa ossea.
Caricamento....
Conclusioni e prospettive
La densitometria ossea rappresenta lo strumento diagnostico insostituibile per la gestione delle malattie metaboliche dello scheletro.
La DXA rimane il gold standard per la sua capacità di predire accuratamente il rischio di frattura con un’esposizione radiologica minima. Tuttavia, la diagnosi densitometrica non deve mai essere isolata dal contesto clinico: fattori come la qualità ossea, il rischio di cadute e le comorbidità del paziente sono altrettanto determinanti per la decisione terapeutica.
Le tecnologie emergenti, come il Trabecular Bone Score (TBS) e la morfometria vertebrale (VFA) integrata nei densitometri, stanno gradualmente spostando il paradigma dalla semplice misurazione della quantità minerale a una valutazione più complessa della qualità e dell’integrità strutturale dello scheletro.
Il futuro della densitometria risiede nell’integrazione di questi parametri in algoritmi di rischio (come il FRAX) per identificare con sempre maggiore precisione i pazienti che beneficeranno maggiormente di un intervento farmacologico preventivo.
Caricamento….
Fonti:
- Linee Guida per la Diagnosi, Prevenzione e Terapia dell’Osteoporosi – SIOMMMS ↩︎
- Bone Density Scan (DEXA or DXA) – Radiologyinfo.org ↩︎
- Densità minerale ossea. Quale relazione con le fratture? ↩︎
- Densitometria ossea e morfometria: strumenti, lettura e interpretazione ↩︎
- Indicazioni all’esecuzione della densitometria ossea in Medicina Generale – SIMG ↩︎
- Commissione Intersocietaria per l’Osteoporosi – simfer ↩︎
- Dual-energy X-ray absorptiometry – Wikipedia ↩︎
- Dual Energy X-Ray Absorptiometry How Does it Work? – Scintica Instrumentation ↩︎
- PRINCIPI FISICI E METODOLOGICI – Fisiokinesiterapia ↩︎
- Comparison Between Quantitative Computed Tomography-Based Bone Mineral Density Values and Dual-Energy X-Ray Absorptiometry-Based Parameters of Bone Density and Microarchitecture: A Lumbar Spine Study – MDPI ↩︎
- Radiation protection of patients during DXA – International Atomic Energy Agenc ↩︎
- Quantitative computed tomography – Wikipedia ↩︎
- Assessment of Technical and Biological Parameters of Volumetric Quantitative Computed Tomography in the Foot: A Phantom Study – PMC ↩︎
- Retrospective Study of Bone Mineral Density through Phantom-Less Quantitative CT ↩︎
- Quantification of the difference in hounsfield units of an electron density phantom between a conventional and standing computed tomography machine – PMC ↩︎
- L’ultrasonografia ossea quantitativa: stato dell’arte e prospettive ↩︎
- Quantitative heel ultrasound as a predictor for osteoporosis | The Medical Journal of Australia ↩︎
- (PDF) Densitometria Ossea (DEXA): come interpretarla evitando le trappole ↩︎
- Common mistakes in the clinical use of bone mineral density testing – PMC ↩︎
- SIOMMMS_2_2021.pdf ↩︎
- Errori e pitfalls della densitometria ossea – Associazione Medici Endocrinologi ↩︎
- D.Lgs. 101/20: novità e conferme in riferimento alle esposizioni mediche – AIFM ↩︎