L’insufficienza cardiaca non rappresenta una singola entità nosologica, bensì una sindrome clinica complessa e progressiva, caratterizzata da una costellazione di sintomi e segni derivanti da un’anomalia strutturale o funzionale della pompa cardiaca.1 Tale condizione determina l’incapacità del cuore di espellere una quantità di sangue adeguata alle richieste metaboliche dei tessuti o, se ciò avviene, solo a discapito di un aumento patologico delle pressioni di riempimento intraventricolari.
La comprensione moderna di questa patologia ha subito un’evoluzione paradigmatica, passando da una visione puramente emodinamica a una prospettiva neuro-ormonale e molecolare, dove il rimodellamento del ventricolo e l’attivazione sistemica di vari assi endocrini giocano un ruolo determinante nella progressione del danno.
Il presente articolo analizza in modo esaustivo ogni aspetto della sindrome, integrando le più recenti evidenze delle linee guida internazionali per fornire un quadro accademico e professionale di riferimento.
Indice
Caricamento….
- Indice
- Definizione ed evoluzione del concetto di insufficienza cardiaca
- Classificazione eziologica e determinanti del danno miocardico
- Classificazione e forme cliniche
- Classificazione in base alla frazione di eiezione (LVEF)
- Forme cliniche
- Severità e tempistiche: NYHA e stadiazione
- Cardiotossicità e cardio-oncologia
- Fisiopatologia: meccanismi di adattamento
- Meccanismo di Frank-Starling e ipertrofia
- Attivazione neuro-umorale
- Manifestazioni cliniche ed emodinamiche
- Scompenso sinistro e sintomi polmonari
- Scompenso destro e manifestazioni sistemiche
- Manifestazioni anterograde e alterazioni del ritmo
- La sindrome cardiorenale (CRS)
- Diagnostica dell’insufficienza cardiaca
- Criteri di Framingham
- Laboratorio e imaging
- Terapia dello scompenso cardiaco cronico
- Trattamento farmacologico della HFrEF
- Terapia per HFmrEF e HFpEF
- Prevenzione della morte improvvisa e CRT
- Gestione dell’insufficienza cardiaca acuta grave
- Trattamento dell’edema polmonare acuto e dello Shock Cardiogeno
- Supporto meccanico: IABP e VAD
- Trapianto cardiaco
Definizione ed evoluzione del concetto di insufficienza cardiaca
La definizione universale di insufficienza cardiaca, recepita dalle principali società scientifiche globali, pone l’accento sulla correlazione tra evidenza oggettiva di disfunzione cardiaca e manifestazioni cliniche.
Una diagnosi formale richiede la presenza di sintomi tipici (dispnea, astenia, edemi) accompagnati da segni clinici (tachicardia, tachipnea, turgore giugulare) e la conferma di una sottostante causa cardiaca, identificata tramite imaging (ecocardiografia) o livelli elevati di peptidi natriuretici.2
La disfunzione può essere di natura strutturale, coinvolgendo alterazioni macroscopiche come la dilatazione delle camere o l’ipertrofia delle pareti, oppure funzionale, riguardando anomalie nel ciclo contrattile (sistole) o nel rilassamento e riempimento (diastole).3 4
Un elemento cardine è il ridotto output cardiaco, che in condizioni di riposo può apparire inizialmente preservato grazie a meccanismi di compenso, ma che fallisce nel rispondere adeguatamente allo stress fisico, portando a una discrepanza tra offerta e domanda di ossigeno nei tessuti periferici.5
Classificazione eziologica e determinanti del danno miocardico
L’identificazione dell’eziologia è il primo passo per un trattamento mirato, poiché molte forme di insufficienza cardiaca possono essere reversibili se la causa sottostante viene corretta precocemente. Le cause possono essere raggruppate in categorie principali che riflettono il meccanismo primario del danno miocardico.
| Categoria eziologica | Esempi specifici | Meccanismo prevalente |
| Miocardica primaria ischemica | Infarto miocardico, coronaropatia cronica, danno ischemico acuto (stunning), cicatrice miocardica, patologia coronarica epicardica o microvascolare, disfunzione endoteliale | Perdita di miociti contrattili, fibrosi post-infartuale |
| Miocardica primaria tossica | Alcol, cocaina, anfetamine, farmaci citostatici/chemioterapici (es. antracicline), FANS, antidepressivi, immunomodulanti (interferone, trastuzumab, cetuximab), radiazioni | Danno citotossico diretto, stress ossidativo |
| Miocardica primaria metabolica | Diabete, tireotossicosi e tireopatie, carenze vitaminiche, alterazioni ipofisarie (deficienza di GH), patologie surrenaliche | Alterazione energetica cellulare, disfunzione mitocondriale |
| Infiltrativa e infiammatoria | Amiloidosi, sarcoidosi, miocarditi da agenti infettivi (batteri, funghi, protozoi, parassiti), miocardite eosinofilica, miocarditi autoimmuni (da LES, artrite reumatoide) | Sostituzione del tessuto contrattile con materiale inerte o flogistico |
| Sovraccarico emodinamico | Ipertensione arteriosa, valvulopatie (difetti strutturali congeniti o acquisiti: mitralica, aortica, tricuspidalica, polmonare), stati ad alta gittata (anemia severa, sepsi, gravidanza), sovraccarico di volume (insufficienza renale) | Aumento cronico del postcarico o del precarico |
| Inadeguato riempimento | Pericardite costrittiva, cardiomiopatia restrittiva, versamento pericardico | Impedimento meccanico all’espansione diastolica |
| Cardiopatie genetiche | Cardiomiopatia ipertrofica, cardiomiopatia dilatativa, miocardio non compatto | Alterazioni strutturali su base genetica (proteine sarcomeriche o citoscheletriche) |
| Aritmie | Bradiaritmie (malattia del nodo del seno), tachiaritmie (fibrillazione atriale, aritmie ventricolari). | Alterazioni della genesi o della conduzione dell’impulso elettrico |
La cardiopatia ischemica resta la causa principale nei paesi sviluppati, dove la necrosi miocardica e il successivo rimodellamento portano alla dilatazione ventricolare.6
Le cause tossiche, in particolare l’alcol, inducono la cosiddetta cardiomiopatia alcolica (A-DCM), che si manifesta dopo un consumo eccessivo protratto (oltre 60-80 g/die per 5 anni), portando a una riduzione della contrattilità e a dilatazione simile alla cardiomiopatia dilatativa idiopatica.7
Sostanze simpaticomimetiche come la cocaina causano invece insufficienza cardiaca attraverso vasospasmo, ipertensione acuta e tossicità miocitaria diretta.
Caricamento….
Classificazione e forme cliniche
La classificazione dell’insufficienza cardiaca è stratificata secondo criteri emodinamici, temporali e sintomatologici per guidare la scelta terapeutica e definire la prognosi.
Classificazione in base alla frazione di eiezione (LVEF)
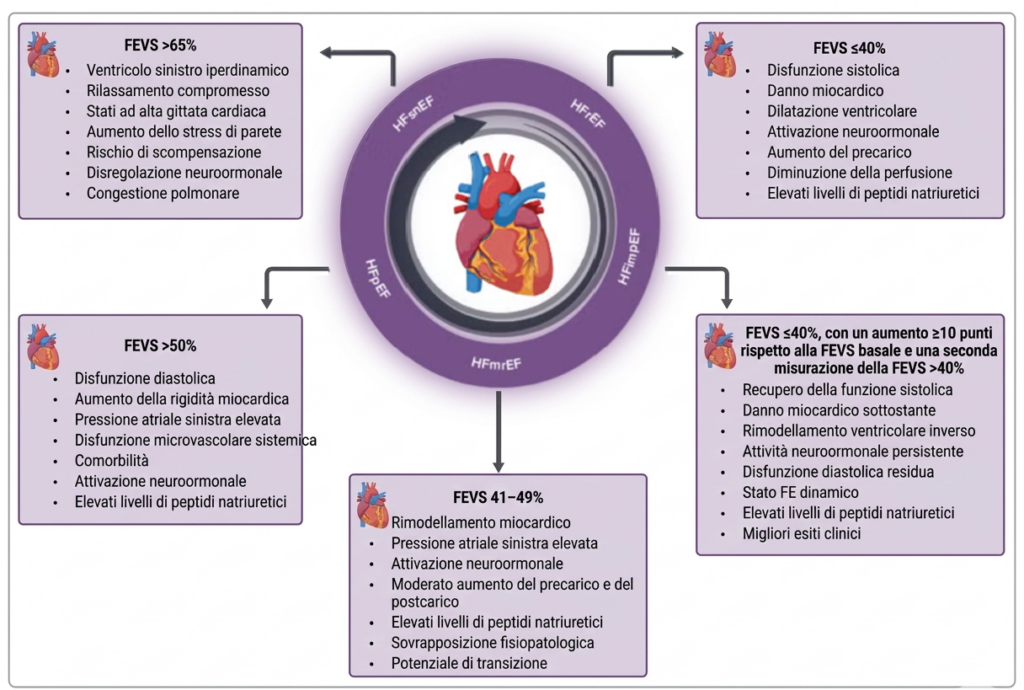
La frazione di eiezione del ventricolo sinistro rimane il parametro fondamentale per la fenotipizzazione dei pazienti:
- HFrEF (HF with Reduced Ejection Fraction): LVEF ≤40%. In questi pazienti, il deficit contrattile è il problema dominante. La maggior parte degli studi clinici ha dimostrato benefici di mortalità in questo sottogruppo;
- HFmrEF (HF with Mildly Reduced Ejection Fraction): LVEF 41-49%. Rappresenta una zona grigia con caratteristiche cliniche sovrapponibili sia alla HFrEF che alla HFpEF;
- HFpEF (HF with Preserved Ejection Fraction): LVEF ≥50%. Spesso associata a pazienti anziani, ipertesi e obesi. La fisiopatologia è legata principalmente all’irrigidimento ventricolare e all’aumento delle pressioni di riempimento diastolico;
- HFimpEF (HF with Improved Ejection Fraction): pazienti precedentemente HFrEF che, grazie alla terapia, presentano ora una LVEF >40%. È fondamentale che questi pazienti continuino il trattamento medico ottimale per evitare recidive.
Forme cliniche
In relazione alla localizzazione del deficit prevalente, si distingue tra insufficienza sinistra e destra. L’insufficienza sinistra è dominata dalla congestione polmonare e dalla riduzione della perfusione sistemica, mentre quella destra si manifesta con segni di stasi nel circolo venoso sistemico.8
La distinzione tra insufficienza anterograda e retrograda è di tipo fisiopatologico: l’anterograda (forward failure) è legata all’incapacità di fornire sangue ossigenato alla periferia (causando astenia, pallore, ipotensione), mentre la retrograda (backward failure) riguarda l’accumulo di sangue “a monte” delle camere cardiache, portando a edema polmonare o periferico.
Le forme ad alta portata sono meno comuni e derivano da stati ipercinetici dove il cuore non riesce a soddisfare richieste metaboliche patologicamente aumentate.
Severità e tempistiche: NYHA e stadiazione
La classificazione NYHA (New York Heart Association) valuta la tolleranza allo sforzo del paziente9:
- Classe I: attività fisica ordinaria non causa sintomi;
- Classe II: lieve limitazione; sintomi per sforzi ordinari;
- Classe III: marcata limitazione; sintomi per sforzi minimi;
- Classe IV: sintomi presenti a riposo.
Le tempistiche di insorgenza definiscono la forma acuta, caratterizzata da un’emergenza medica improvvisa che richiede trattamento immediato, e la forma cronica, spesso intermezzata da episodi di riacutizzazione dovuti a cause scatenanti come infezioni, aritmie o mancata aderenza alla dieta.
Cardiotossicità e cardio-oncologia
Il legame tra oncologia e cardiologia è diventato centrale con l’aumento della sopravvivenza dei pazienti oncologici. La tossicità cardiovascolare correlata alla terapia del cancro (CTR-CVT) può manifestarsi con insufficienza cardiaca grave.
Le antracicline inducono un danno dose-dipendente e irreversibile dovuto allo stress ossidativo e alla rottura dei legami nel DNA dei miociti.10
Al contrario, gli inibitori di HER2 come il Trastuzumab causano spesso una disfunzione reversibile (Tipo II), che però richiede un monitoraggio ecocardiografico trimestrale.
La prevenzione si basa sulla stratificazione del rischio tramite il punteggio HFA-ICOS e, nei pazienti ad alto rischio, sull’uso profilattico di beta-bloccanti e ACE-inibitori.
Caricamento….
Fisiopatologia: meccanismi di adattamento
Quando la funzione cardiaca declina, l’organismo attiva una serie di meccanismi di compenso per mantenere la pressione arteriosa e l’irrorazione degli organi vitali.
Meccanismo di Frank-Starling e ipertrofia
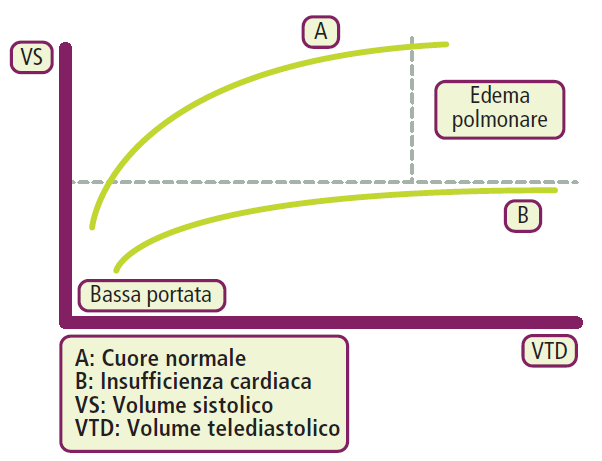
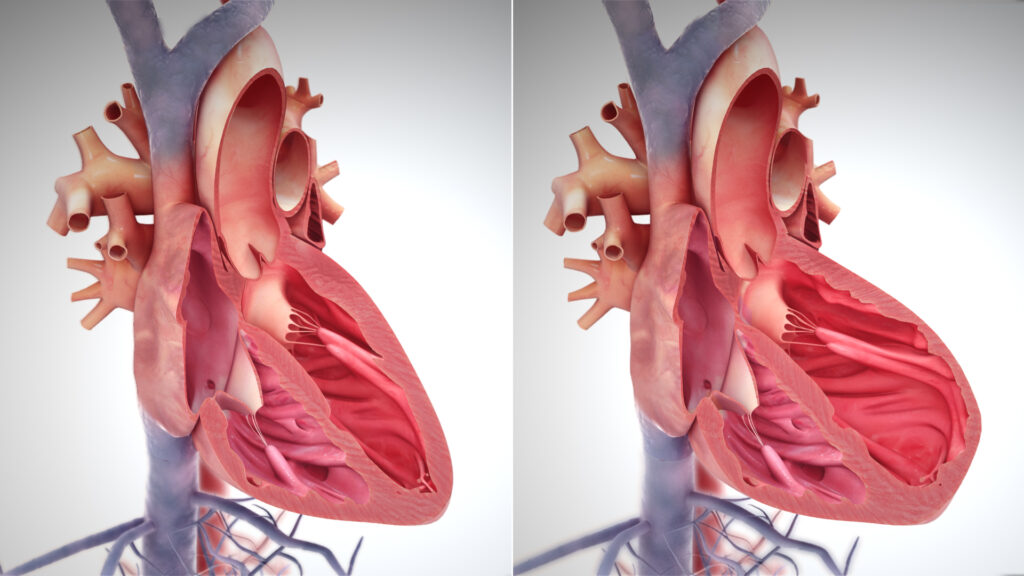
Il cuore risponde all’aumento del volume telediastolico stirando le fibre miocardiche, il che aumenta la forza di contrazione secondo il meccanismo di Frank-Starling.11 Tuttavia, nel cuore insufficiente, la curva di prestazione è piatta: l’ulteriore stiramento non produce più un aumento della gittata, ma solo un aumento della pressione venosa polmonare o sistemica.
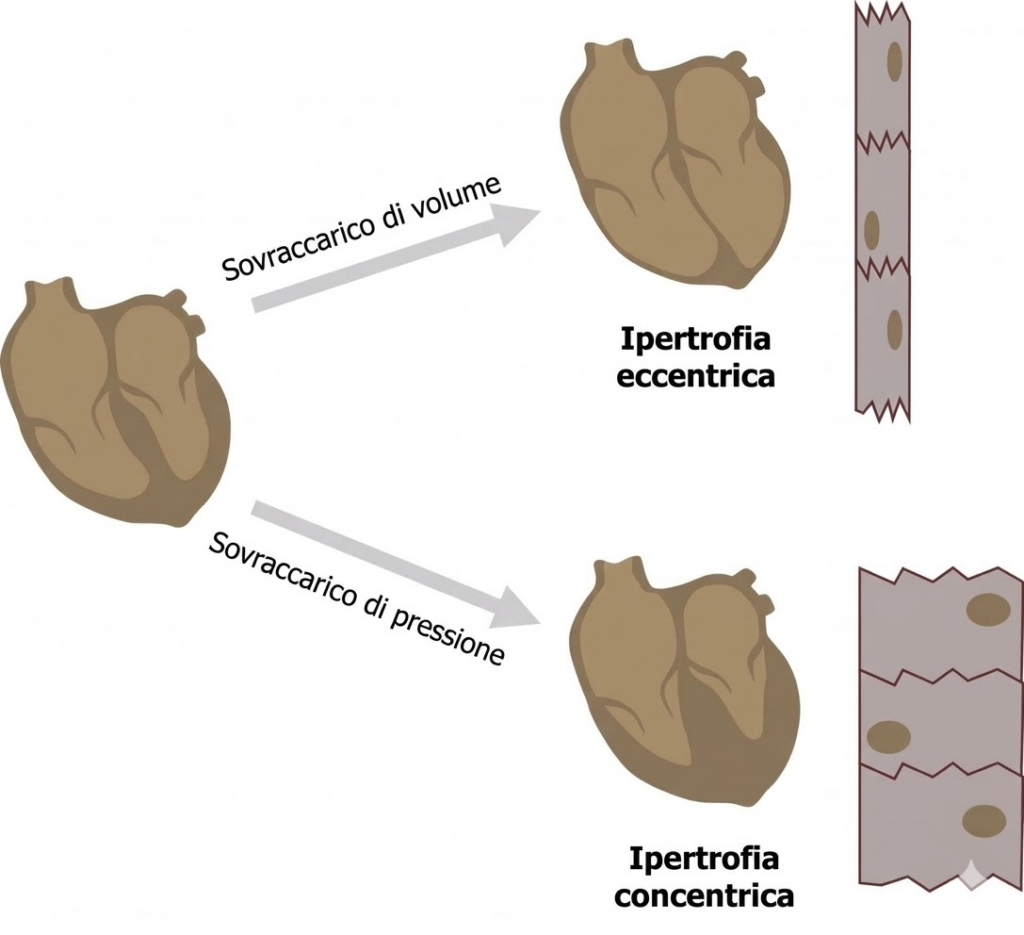
Il rimodellamento strutturale segue la legge di Laplace. Per ridurre lo stress di parete dovuto all’aumento della pressione o del raggio della camera, il cuore aumenta lo spessore delle pareti (ipertrofia):
- ipertrofia eccentrica: causata da sovraccarico di volume. I sarcomeri si aggiungono in serie, portando a una dilatazione della camera con spessore di parete che può rimanere normale o ridursi proporzionalmente;
- ipertrofia concentrica: causata da sovraccarico di pressione. I sarcomeri si aggiungono in parallelo, le pareti si ispessiscono e il volume della camera diminuisce.
Attivazione neuro-umorale
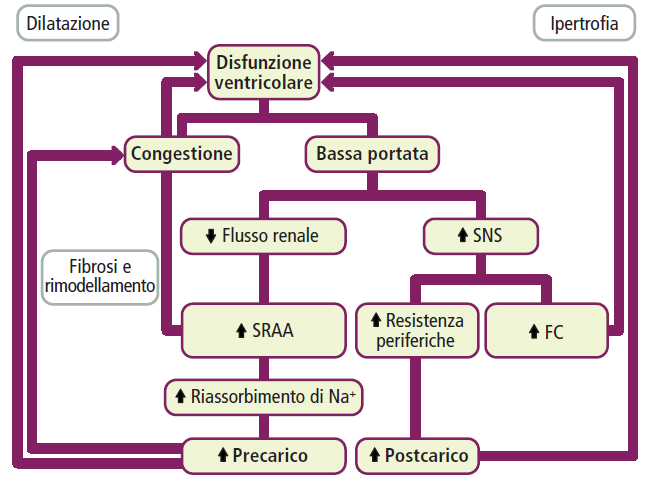
L’attivazione del Sistema Nervoso Simpatico (SNS) e del Sistema Renina-Angiotensina-Aldosterone (SRAA) è il pilastro della fisiopatologia moderna.12
| Sistema | Effetto acuto (compenso) | Effetto cronico (danno) |
|---|---|---|
| SNS | Aumento frequenza e contrattilità, vasocostrizione | Tossicità diretta da catecolamine, aritmie, aumento postcarico |
| SRAA | Ritenzione di sodio e acqua, aumento precarico | Edema, fibrosi miocardica, ipertrofia maladattativa |
| Peptidi natriuretici | Vasodilatazione, natriuresi | Meccanismo di contro-regolazione che fallisce nel tempo per sbilanciamento |
L’angiotensina II e l’aldosterone non solo aumentano il volume circolante, ma stimolano la sintesi di collagene, portando alla fibrosi che irrigidisce il cuore e ne compromette la funzione sia sistolica che diastolica.
Caricamento....
Now loading…
Manifestazioni cliniche ed emodinamiche
Scompenso sinistro e sintomi polmonari
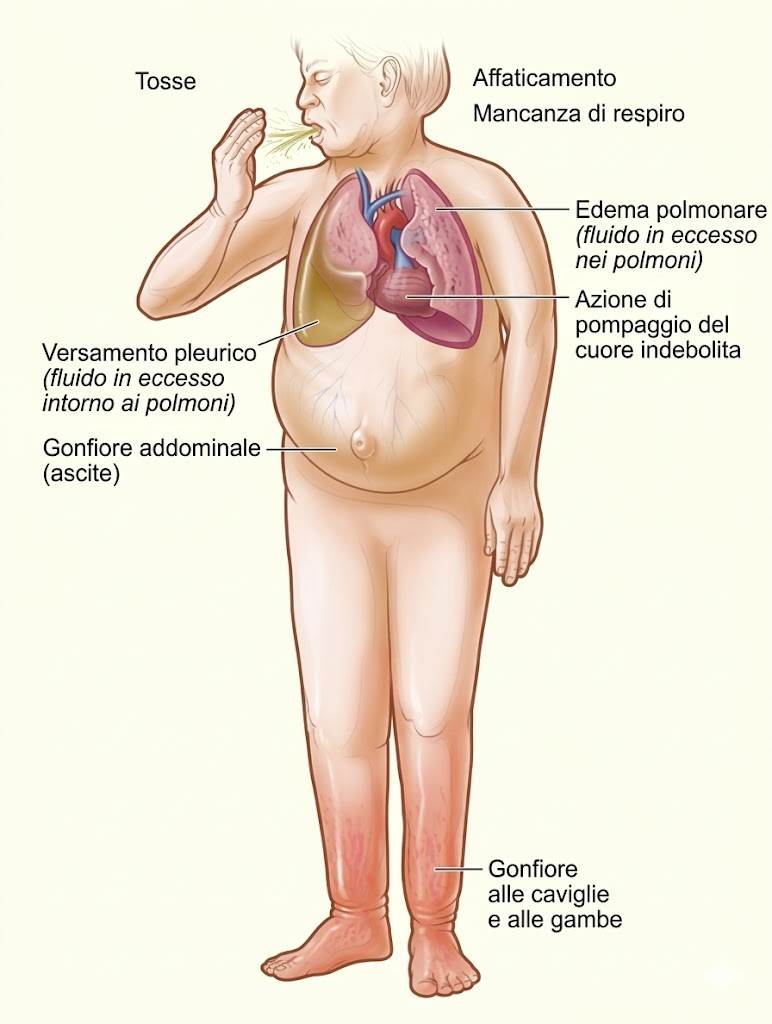
La congestione retrograda del circolo polmonare causa la trasudazione di liquidi nell’interstizio e negli alveoli, generando sintomi quali:
- dispnea da sforzo: il sintomo più precoce, causato dall’aumento delle pressioni capillari polmonari durante l’esercizio;
- ortopnea: difficoltà respiratoria in posizione supina, alleviata dai cuscini, dovuta alla ridistribuzione dei liquidi dagli arti al torace;
- dispnea parossistica notturna (DPN): attacchi improvvisi di dispnea che insorgono dopo alcune ore di sonno;
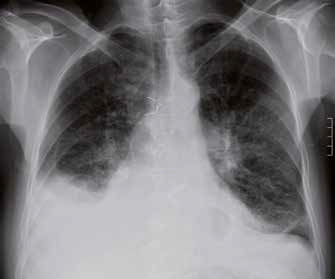
- edema polmonare acuto: emergenza estrema con rantoli crepitanti diffusi, espettorato schiumoso e grave ipossia.
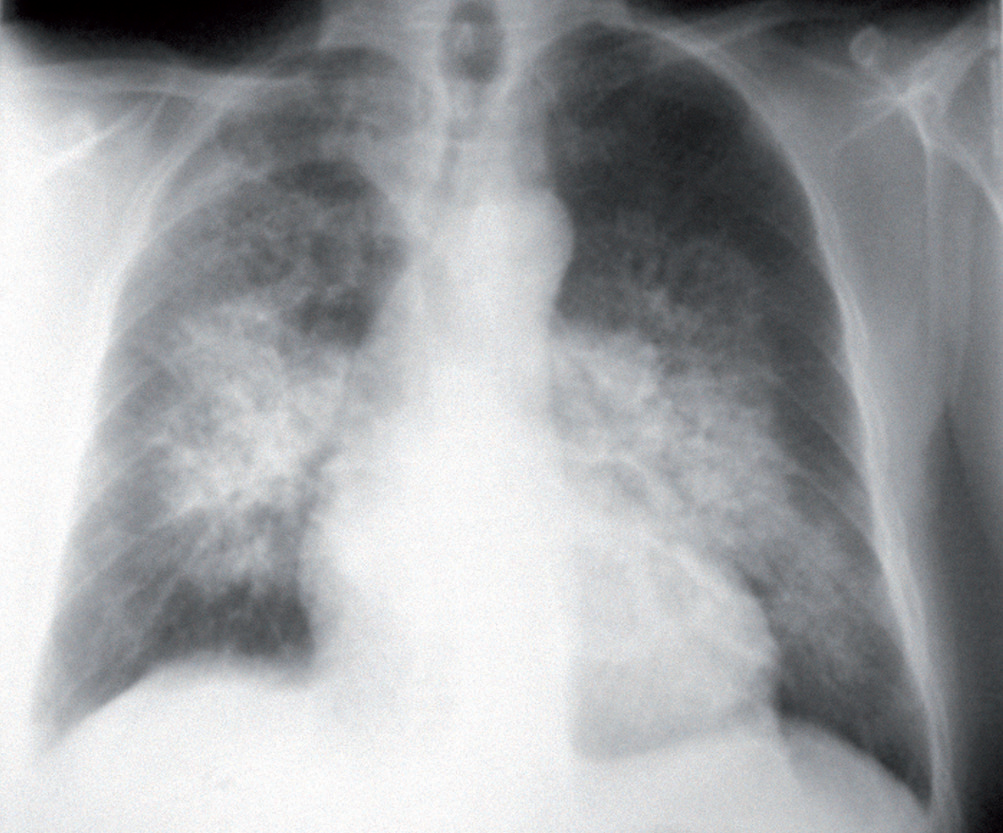
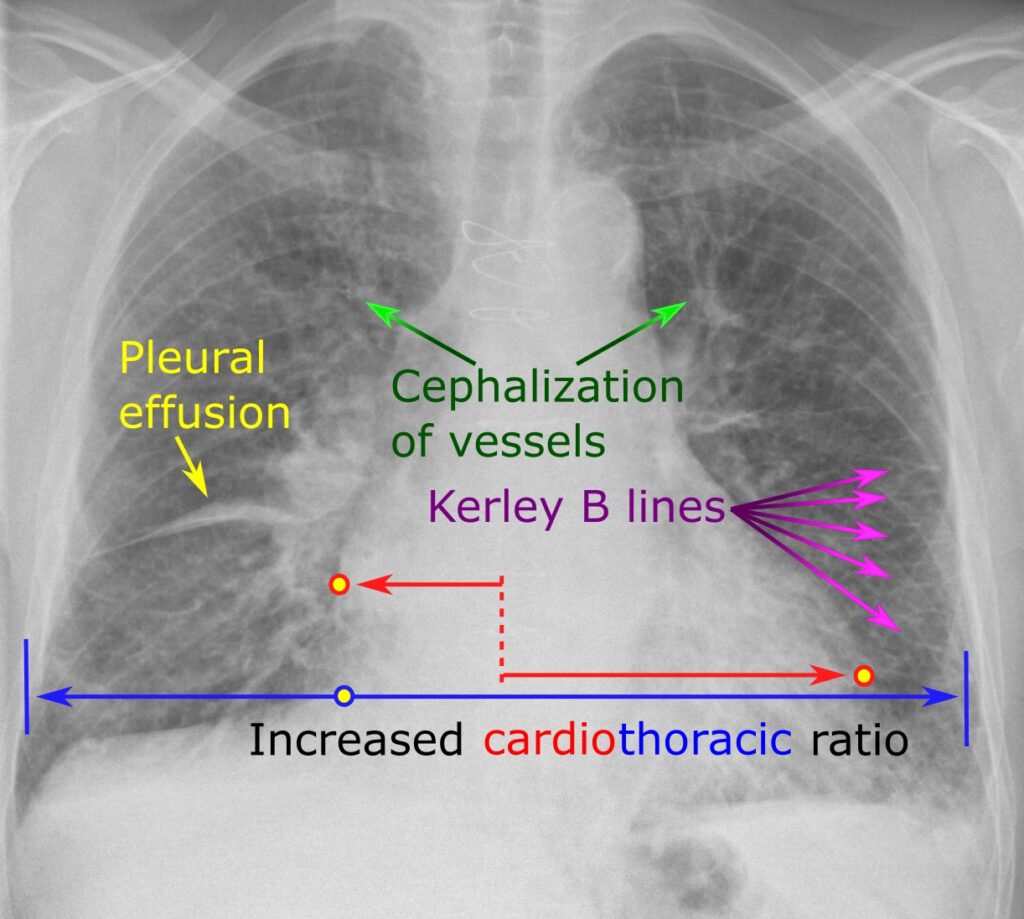
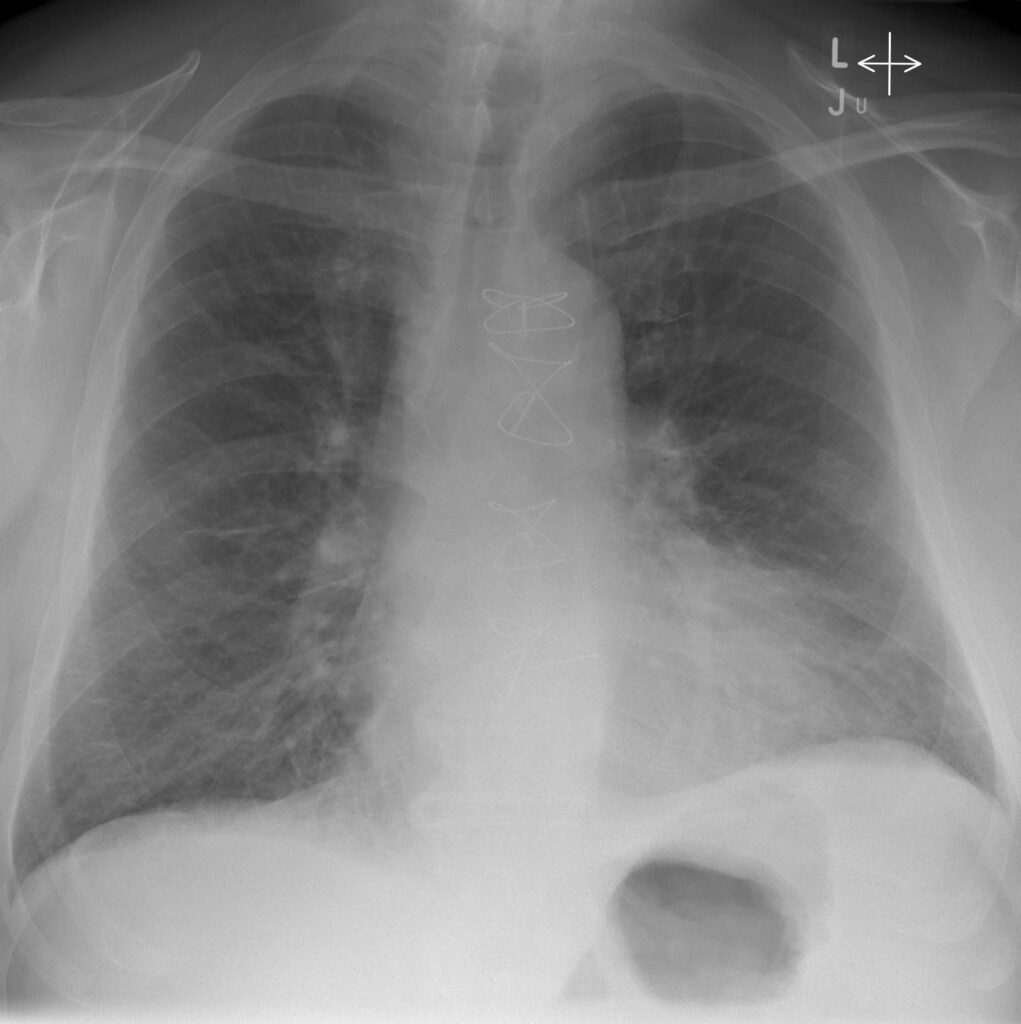
Si notino i segni di ridistribuzione vascolare verso i campi superiori e l’ingrandimento secondario alla congestione di entrambi gli ili polmonari definito “ad ali di farfalla”.
Caricamento....
Scompenso destro e manifestazioni sistemiche
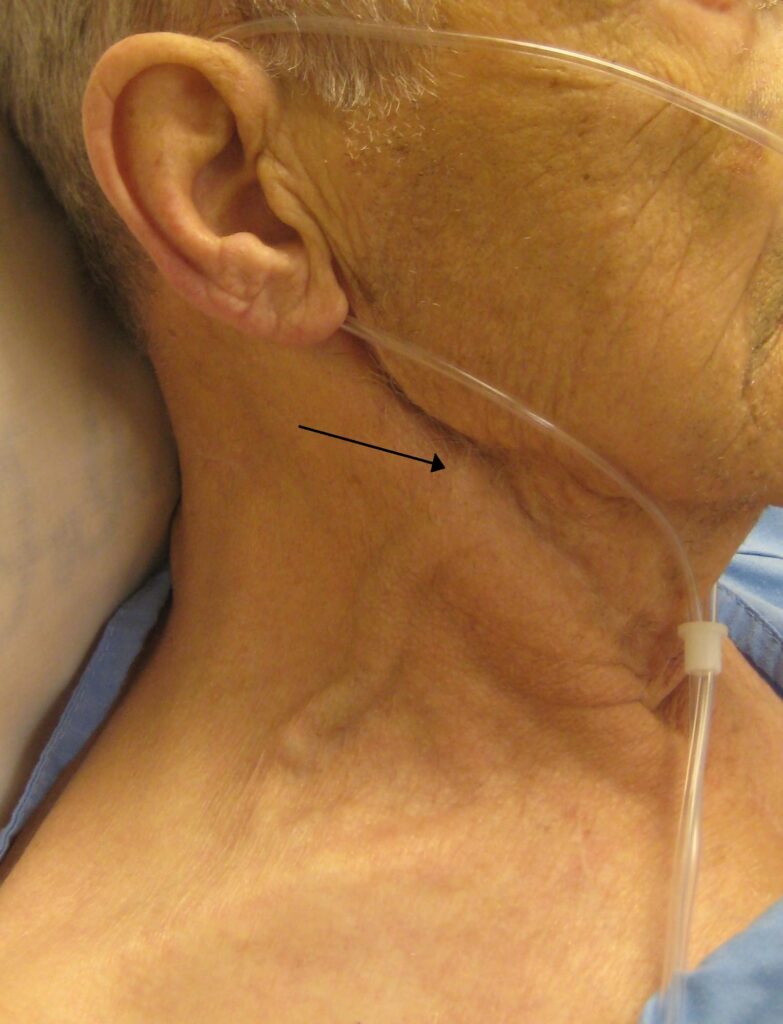
- Turgore giugulare: riflesso diretto dell’aumento della pressione in atrio destro;
- epatomegalia e ascite: la stasi venosa nel circolo portale causa ingrossamento del fegato e accumulo di liquido peritoneale;
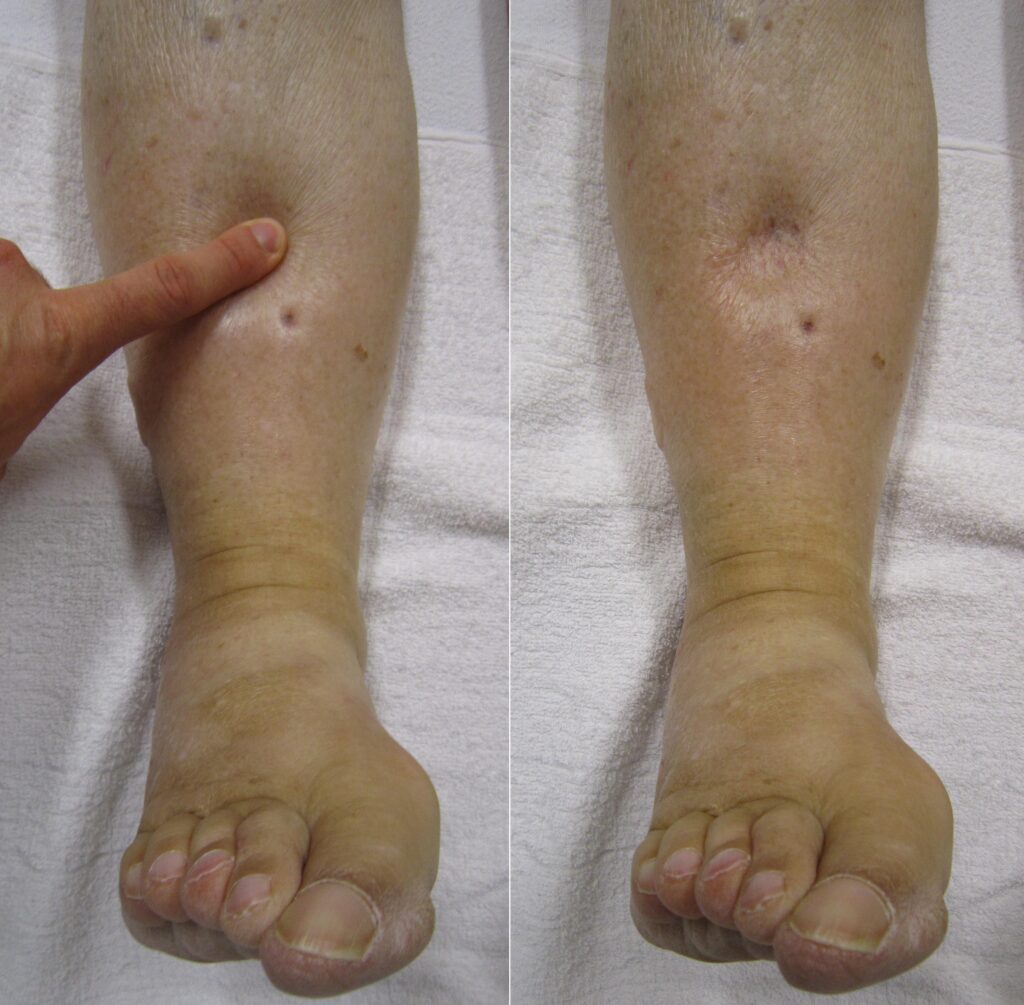
- edemi periferici: tipicamente bilaterali, declivi (caviglie), con segno della fovea.
Manifestazioni anterograde e alterazioni del ritmo
La riduzione della portata causa oliguria diurna e nicturia notturna (quando il riposo migliora la perfusione renale).13
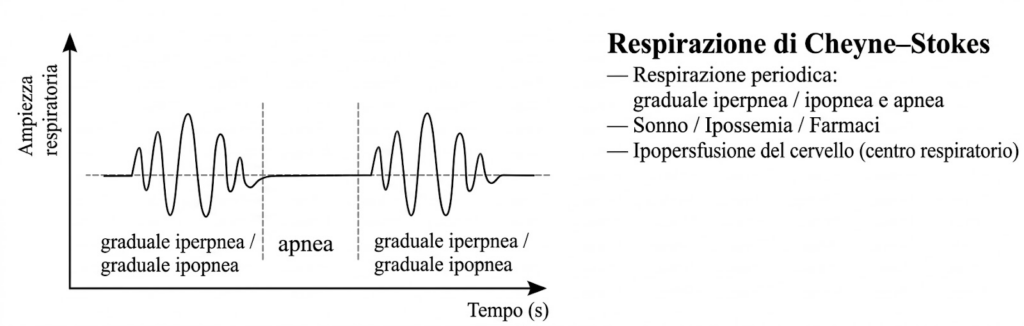
Possono comparire sintomi cerebrali come letargia o il respiro di Cheyne-Stokes, un pattern respiratorio periodico legato all’instabilità del centro del respiro e al ritardato tempo di circolo.14
All’auscultazione, il ritmo di galoppo (S3 o S4) è un segno cardine di disfunzione ventricolare.15
Il polso alternante, caratterizzato da un’alternanza regolare di battiti forti e deboli, indica una grave compromissione della contrattilità.
La sindrome cardiorenale (CRS)
La CRS descrive l’interazione patologica tra cuore e reni, classificata in cinque tipi16:
- tipo 1 (acuta): insufficienza cardiaca acuta che causa danno renale acuto (AKI). Il meccanismo principale è la congestione venosa renale piuttosto che la bassa portata;
- tipo 2 (cronica): insufficienza cardiaca cronica che porta a malattia renale cronica progressiva;
- tipo 3 (renocardiaca acuta): un danno renale acuto (es. glomerulonefrite) induce insufficienza cardiaca acuta tramite sovraccarico di volume e ipertensione;
- tipo 4 (renocardiaca cronica): la nefropatia cronica induce ipertrofia e disfunzione cardiaca;
- tipo 5 (secondaria): condizioni sistemiche come sepsi, diabete o lupus che colpiscono contemporaneamente entrambi gli organi.
Caricamento….
Diagnostica dell’insufficienza cardiaca
L’iter diagnostico deve essere rapido e preciso, basandosi su criteri clinici validati e test strumentali.
Criteri di Framingham
La diagnosi richiede la presenza di 2 criteri maggiori o 1 maggiore e 2 minori.17
| Criteri maggiori | Criteri minori |
| Dispnea parossistica notturna, ortopnea | Edemi declivi (edema malleolare) |
| Edema polmonare acuto | Dispnea da sforzo |
| Crepitii (rantoli polmonari) | Tosse notturna |
| Distensione della vena giugulare (turgore giugulare) | Versamento pleurico |
| Aumento della pressione venosa (>16 cm H2O) | Capacità vitale ridotta di 1/3 |
| Reflusso (o riflesso) epato-giugulare positivo | Epatomegalia |
| Ritmo di galoppo (S3) | Tachicardia (>120 bpm) |
| Cardiomegalia (Rx) | Perdita di peso (se usata come criterio minore) |
Laboratorio e imaging
I peptidi natriuretici (BNP e NT-proBNP) sono fondamentali per lo screening. Un valore di NT-proBNP <300 pg/ml in acuto o <125 pg/ml in cronico ha un altissimo valore predittivo negativo per escludere l’insufficienza cardiaca.
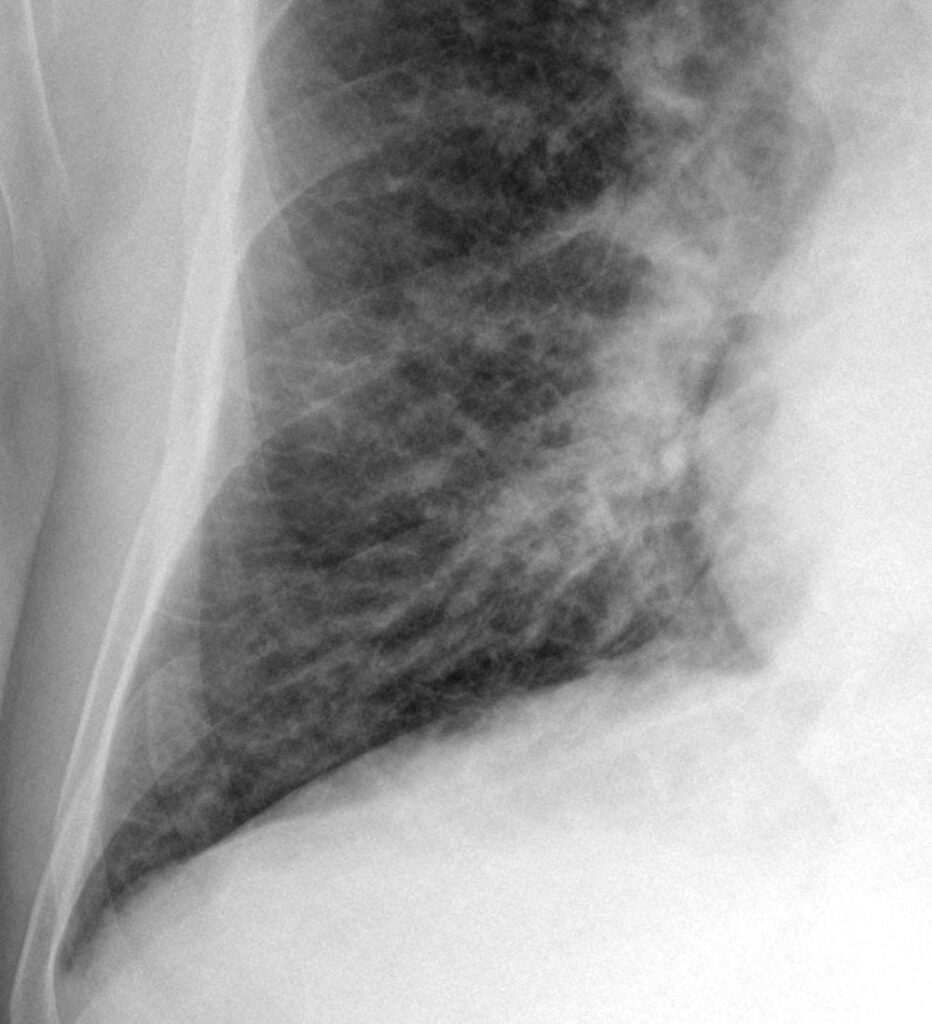
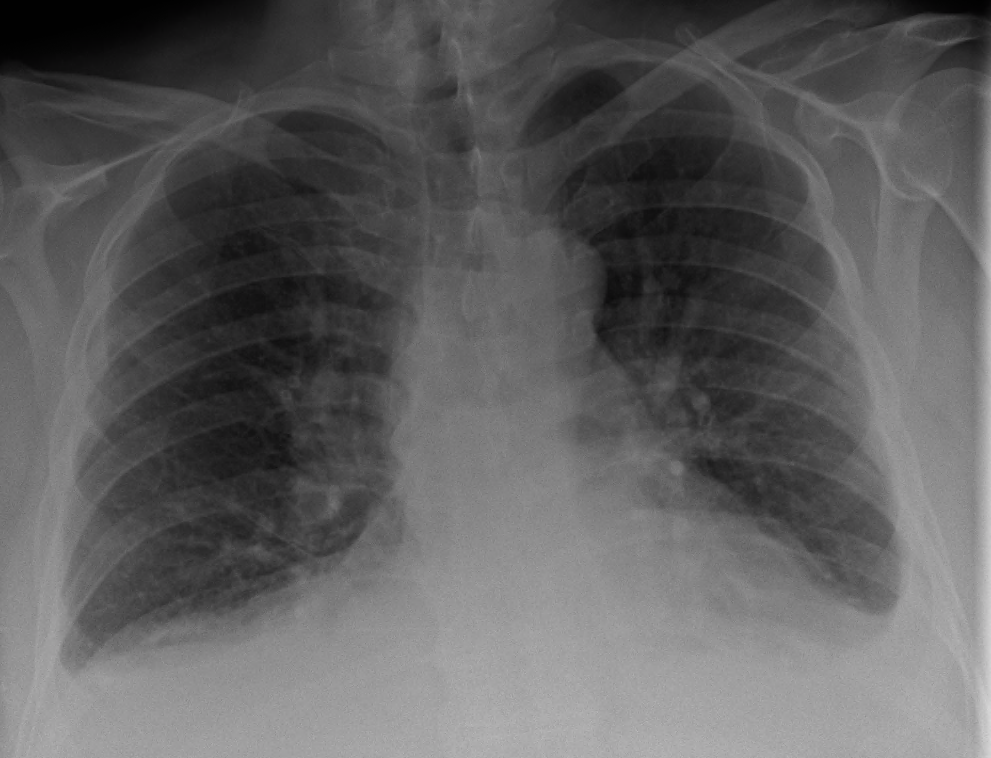
La radiografia del torace può mostrare segni di congestione interstiziale (linee di Kerley B), l’edema alveolare ad “ali di farfalla” e quote di versamento pleurico bilaterale.
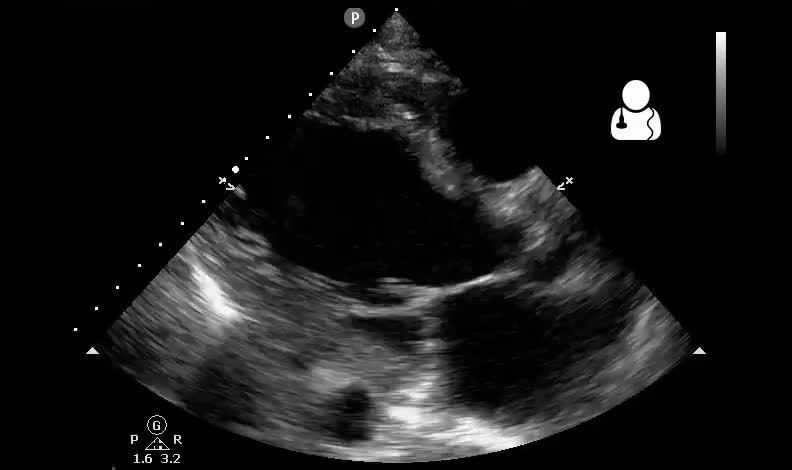
L’ecocardiografia colordoppler è lo strumento principe per definire la frazione di eiezione e le alterazioni valvolari e cardiache.
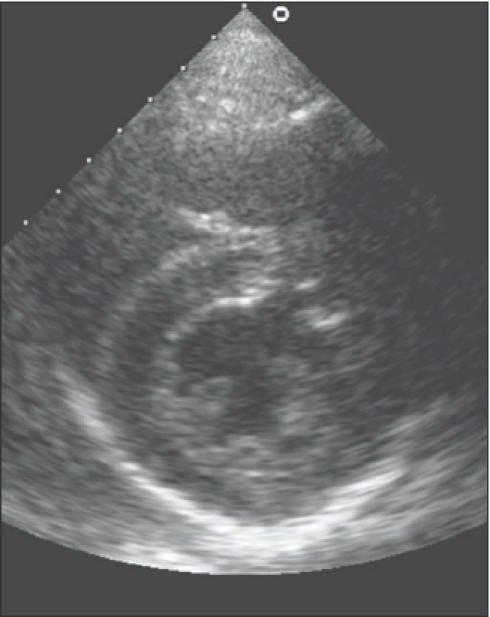
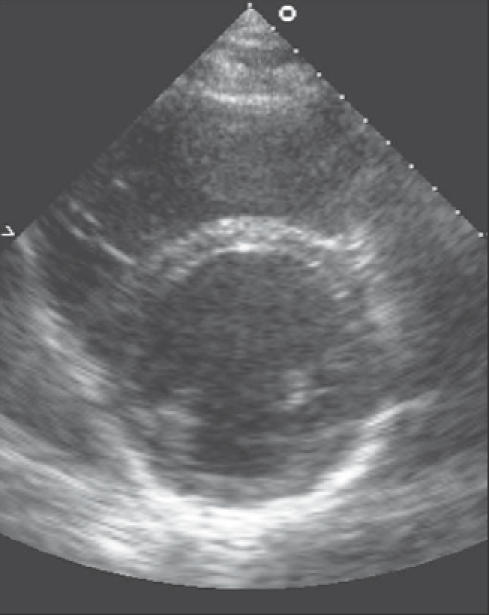
L’elettrocardiogramma (ECG) è utile per identificare cause scatenanti come fibrillazione atriale o pregresso infarto.
Terapia dello scompenso cardiaco cronico
Il trattamento si è evoluto verso una quadrupla terapia fondamentale per i pazienti HFrEF.
Trattamento farmacologico della HFrEF
Le linee guida ESC 2021 e l’aggiornamento 2023 pongono i seguenti farmaci come Classe I:
- ARNI (Sacubitril/Valsartan): raccomandato come sostituto di ACE-inibitori o sartani per ridurre ulteriormente mortalità e ospedalizzazioni;
- beta-bloccanti: fondamentali per bloccare l’iperattività simpatica. Devono essere iniziati a dosi basse e titolati lentamente;
- antagonisti dei mineralocorticoidi (MRA): spironolattone o eplerenone, essenziali per contrastare la fibrosi;
- gliflozine (SGLT2i): dapagliflozin o empagliflozin. Hanno rivoluzionato la terapia riducendo il rischio di morte cardiovascolare indipendentemente dalla presenza di diabete.
Altri farmaci includono l’ivabradina (per frequenza >70 bpm), la digossina (per controllo della fibrillazione atriale o sintomi refrattari) e i diuretici per la gestione dei liquidi.
Terapia per HFmrEF e HFpEF
Recentemente, gli SGLT2i hanno ricevuto una raccomandazione di Classe I anche per HFmrEF e HFpEF, diventando la prima terapia a dimostrare un beneficio chiaro in queste popolazioni. Per le altre classi di farmaci, i dati sono meno robusti (Classe IIb).
Prevenzione della morte improvvisa e CRT
L’impianto di un defibrillatore automatico (ICD) è indicato in prevenzione primaria se LVEF ≤35% nonostante terapia medica ottimale.
La terapia di resincronizzazione cardiaca (CRT) è invece indicata in pazienti con LVEF ridotta e blocco di branca sinistra (QRS largo) per migliorare la coordinazione della contrazione ventricolare.
Gestione dell’insufficienza cardiaca acuta grave
In fase acuta, l’obiettivo è la stabilizzazione emodinamica e il sollievo dei sintomi.
Trattamento dell’edema polmonare acuto e dello Shock Cardiogeno
Si basa sull’uso di ossigeno (anche tramite ventilazione non invasiva), furosemide endovena e vasodilatatori (nitroglicerina) se la pressione arteriosa è preservata18. Nello shock cardiogeno, sono necessari farmaci inotropi:
- dobutamina: agonista beta-1, aumenta la portata ma anche il consumo di ossigeno;
- milrinone: inibitore della fosfodiesterasi, utile in pazienti già trattati con beta-bloccanti;
- levosimendan: sensibilizzante al calcio, migliora la gittata senza aumentare il calcio intracellulare, riducendo il rischio di aritmie rispetto alle amine.19
Supporto meccanico: IABP e VAD
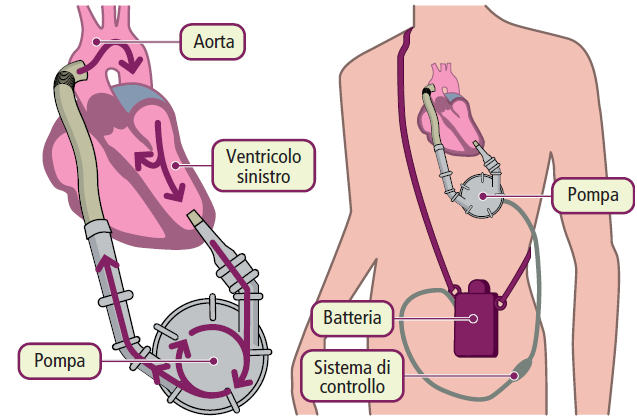
Il contropulsatore aortico (IABP) è un supporto temporaneo che riduce il postcarico e aumenta la perfusione coronarica. I dispositivi di assistenza ventricolare (VAD) sono invece pompe meccaniche a lungo termine utilizzate come20:
- bridge to transplant (BTT): ponte al trapianto;
- bridge to decision (BTD): ponte alla decisione terapeutica;
- destination therapy (DT): terapia definitiva per chi non può ricevere un trapianto.21
Trapianto cardiaco
Il trapianto rimane l’opzione definitiva per l’insufficienza terminale (Stadio D).
Le indicazioni principali sono lo shock cardiogeno refrattario, la dipendenza da inotropi e un VO2 max <12 ml/kg/min.
Le controindicazioni assolute includono l’ipertensione polmonare fissa, neoplasie attive e infezioni sistemiche non controllate.22
Le principali sfide includono il rigetto acuto e cronico, le infezioni (specialmente CMV) e la vasculopatia del graft (CAV).23
La CAV è una forma accelerata di aterosclerosi che colpisce le coronarie del cuore trapiantato, rappresentando la principale causa di fallimento dell’organo a lungo termine.
Fonte: Manuale di cardiologia, chirurgia vascolare e cardiochirurgia. Concorso Nazionale SSM.
Caricamento…
Altre fonti:
- ACC/AHA/HFSA 2022 and ESC 2021 guidelines on heart failure comparison – PMC ↩︎
- The 2023 ESC heart failure guideline update and its implications for clinical practice – PMC ↩︎
- History of Heart Failure Definition – Cardiac Failure Review ↩︎
- Heart Failure – Cardiovascular Pathophysiology for Pre-Clinical Students ↩︎
- Edema formation in congestive heart failure and the underlying mechanisms – PMC – NIH ↩︎
- Cardiac remodelling: concentric versus eccentric hypertrophy in strength and endurance athletes – PMC ↩︎
- Alcohol and Heart Failure | ECR Journal – European Cardiology Review ↩︎
- Heart failure – Wikipedia ↩︎
- Ventricular Assist Devices for Bridge-to-Transplant and Destination Therapy (CAG-00432R) – Decision Memo – CMS ↩︎
- Strategies for risk stratification and cardiovascular toxicity prevention in patients with cancer ↩︎
- Physiology, Starling Relationships – StatPearls – NCBI Bookshelf ↩︎
- Pathophysiology of Congestion in Heart Failure: A Contemporary Review ↩︎
- Oliguria – StatPearls – NCBI Bookshelf – NIH ↩︎
- Cheyne–Stokes respiration – Wikipedia ↩︎
- Fourth heart sound – Wikipedia ↩︎
- Cardiorenal Syndrome – StatPearls – NCBI Bookshelf ↩︎
- The epidemiology of congestive heart failure: the Framingham Heart Study perspective – PMC ↩︎
- Use of levosimendan in acute heart failure – PMC – NIH ↩︎
- Comparative safety and efficacy of levosimendan versus dobutamine in acute heart failure: a systematic review, meta-analysis, and meta-regression – PMC ↩︎
- Intra-Aortic Balloon Pump – StatPearls – NCBI Bookshelf – NIH ↩︎
- Implantable ventricular assistance systems (VAD) as a bridge to transplant or as ‘destination therapy’ – PMC ↩︎
- Guidelines for heart transplantation – PMC – NIH ↩︎
- Risk factors of cardiac allograft vasculopathy – PMC – NIH ↩︎