L’elettroforesi è un tipo di metodica analitica che permette l’analisi di molecole proteiche, amminoacidi e DNA. Essa consiste nella migrazione di particelle in sospensione, dotate di carica elettrica q, sotto l’azione di un campo elettrico E applicato esternamente.
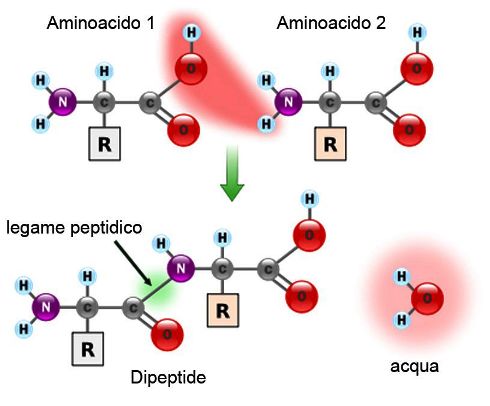
Le molecole di aminoacidi o di proteine contengono sia gruppi acidi che gruppi basici che si dissociano parzialmente quando si trovano in soluzione formando grossi ioni, sia carichi positivi che negativi. La grandezza e il segno di queste cariche elettriche dipendono dal pH della soluzione.
Inserendo due elettrodi, tra i quali si stabilisce una certa differenza di potenziale ΔV, si genera un campo elettrico E uniforme:
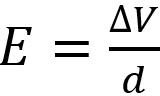
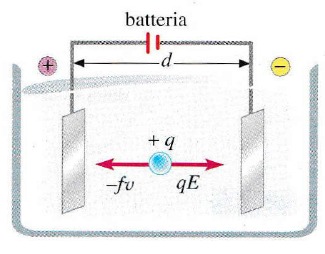
dove d è la distanza tra i due elettrodi. Il campo elettrico è diretto dall’elettrodo positivo (anodo) a quello negativo (catodo). La presenza del campo elettrico porta alla formazione di una forza che agisce sulla carica q di valore: Fe= q E.
Gli ioni si muovono con una certa velocità v in un mezzo viscoso e sono frenati perciò da una forza di attrito viscoso (FR) che ha la stessa direzione di v ma verso opposto: FR= -f v. Dove f è il coefficiente di attrito viscoso e v è la velocità degli ioni.
Considerando che gli ioni sono di forma sferica la FR può essere scritta applicando la legge di Stokes: FR= -6πηrv, dove r è il raggio dello ione in movimento mentre η è il coefficiente di viscosità della soluzione.
La FR frenante cresce con la v fino ad eguagliare in modulo la Fe elettrica e la velocità limite di trascinamento v=vs sapendo che Fe=-FR per cui q E = –6πηrvs allora sarà:
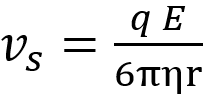
La forza peso e la spinta di Archimede non si considerano all’equilibrio delle forze, perché perpendicolari alla direzione della velocità.
In luogo del coefficiente di sedimentazione, si definisce nel caso dell’elettroforesi la mobilità elettroforetica μe che risulta essere una proprietà della particella e del solvente:
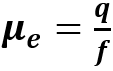
La μe rappresenta la velocità elettroforetica per unità di campo elettrico E applicato. Sostituendo f con 6πηr per particelle sferiche si ha:
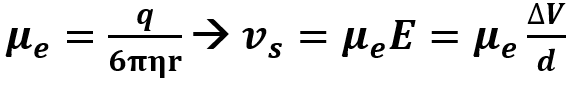
Poiché la mobilità dipende dalle dimensioni delle particelle (in quanto f=6πηr), particelle di dimensioni diverse hanno mobilità e velocità di trascinamento diverse, in particolare la velocità delle particelle è inversamente proporzionale alle loro dimensioni. Inoltre la mobilità dipende dalla carica elettrica q che nel caso degli amminoacidi varia a seconda del pH della soluzione. Infatti esiste un valore di pH per cui la carica netta è nulla (punto isoelettrico). Particelle che hanno carica nulla non si muoveranno.
Sfruttando le diverse velocità di migrazione elettroforetica si possono separare e analizzare quantitativamente le diverse componenti di una miscela di proteine o di amminoacidi.
Fonte: Fisica biomedica.