Anche detto carcinoma papillifero, è il più frequente tumore della tiroide rappresentando circa l’80% di tutti i tumori maligni della tiroide, ma è anche il meno aggressivo, specialmente se diagnosticato prima che dà metastasi.
In genere insorge in aree dove non vi è carenza di iodio e una condizione clinica che può portare alla predisposizione dell’insorgenza di carcinoma papillare è la tiroidite di Hashimoto. Con la questa tiroidite i tireociti diventano ossifili ed in alcuni casi hanno dei nuclei attivati che somigliano a quelli del carcinoma. La flogosi provocata dal quadro di tiroidite provoca uno stimolo cronico che dà irritazione, favorendo la predisposizione alla neoplasia e portando quindi maggiore incidenza di carcinoma papillare nei soggetti con tiroidite.
Oltre alla tiroidite, l’esposizione a radiazioni ionizzanti costituisce un fattore di rischio primario nello sviluppo del carcinoma papillare.
Le alterazioni molecolari associate con tale neoplasia sono in genere mutazioni puntiforme in BRAF, ma vi possono essere anche mutazioni in RAS e alterazioni con riarrangiamento RET/PTC.
Circa l’80% dei casi all’esame macroscopico appare solido con margini irregolari, il 10% come nodulo ben circoscritto, il 10% ha invece un aspetto cistico. E’ spesso privo di capsula e multifocale (ovvero interessa contemporaneamente punti diversi della tiroide).
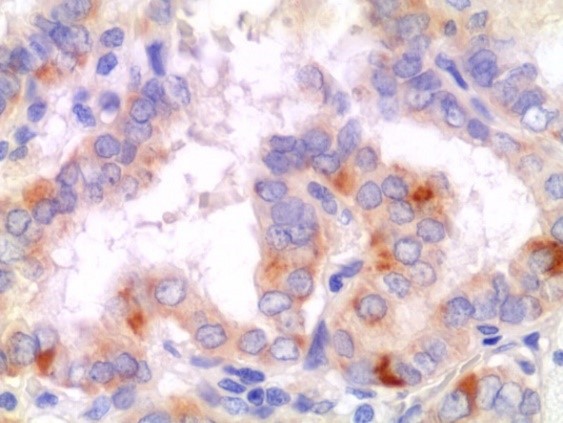
Molto importante è invece il quadro istologico che è utile ai fini diagnostici. Questo carcinoma presenta un’architettura papillare con papille ramificate costituite da un peduncolo fibrovascolare centrale rivestito da epitelio cubico monostratificato.
I nuclei delle cellule contengono cromatina dispersa che assume un aspetto otticamente chiaro o vuoto, detti nuclei a vetro smerigliato o ad occhi dell’orfanella Annie, aspetto dovuto all’azione della fissazione in formalina su queste peculiari cellule neoplastiche.
È caratteristica anche la presenza di invaginazioni del citoplasma, in sezione, che hanno l’aspetto di pseudoinclusioni. Sono presenti incisioni nucleari; all’interno delle lesioni sono presenti calcificazioni concentriche di materiale calcareo dette corpi psammomatosi e focolai di metaplasia squamosa.
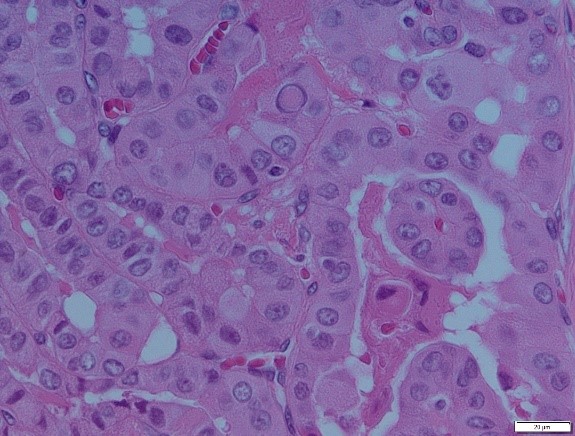
Nelle forme multifocali si evidenzia la presenza di microfocolai neoplastici che possono essere dovuti a:
- Insorgenza indipendente di più neoplasie;
- Disseminazione metastatica intratiroidea per via linfatica.
Per quanto riguarda il quadro clinico, non dà sintomi rilevanti. I noduli sono asintomatici, mobili alla deglutizione, freddi. Negli stadi avanzati della neoplasia si possono tuttavia avere sintomi clinici da compressione e infiltrazione quali disfagia, disfonia, tosse o dispnea e tumefazioni dei linfonodi cervicali (in seguito a metastatizzazione).
La prognosi è eccellente in oltre il 95% dei casi, infatti il tasso di sopravvivenza a 20 anni è del 98-99%. Ci sono poche possibilità di metastasi a distanza, mentre più comuni sono le metastasi linfonodali ai linfonodi cervicali satelliti (circa 50% dei pazienti).
All’esame immunoistochimico si possono avere positività a diversi marcatori:
- Il tumore primitivo è positivo per HBME-1, galectina 3 e citocheratina 19;
- Le metastasi sono positive per la tireoglobulina (nel citoplasma) e il fattore di trascrizione TTF-1 (nel nucleo).
Un altro marcatore molto utilizzato è il CD56, un marcatore neuroendocrino che viene espresso normalmente dalle cellule tiroidee, tuttavia la sua perdita è indicativa di neoplasia.
Fatti insieme questi marcatori aumentano la specificità della diagnostica che rimane comunque citologica sulla base delle alterazioni nucleari.
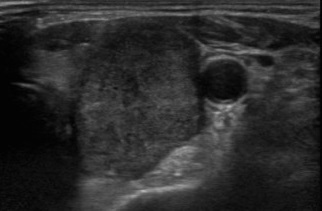
Come per tutti i tumori tiroidei non è assolutamente possibile effettuare la diagnosi di tumore papillare della tiroide solo con gli esami del sangue (ormoni tiroidei, TSH, tireoglobulina) in quanto questi risultano quasi sempre nella norma, pertanto gli esami più importanti nella diagnosi del tumore papillare sono l’ecografia e l’agoaspirato tiroideo.
L’ecografia tiroidea permette di valutare le dimensioni e le principali caratteristiche del nodulo tiroideo (ipoecogenicità, margini del tumore, vascolarizzazione, cacilficicazioni). Alcune di queste caratteristiche, soprattutto se associate, possono orientare decisamente verso la diagnosi di tumore papillare della tiroide soprattutto in presenza di franche metastasi linfonodali. Per una diagnosi certa è comunque necessario l’agoaspirato del nodulo sospetto.
L’agoaspirato tiroideo (Fine Needle Aspiration, FNA) è una metodica minimamente invasiva che consente una diagnosi certa e sicura del tumore tiroideo. Consiste nel prelevare alcune cellule tiroidee contenute nel nodulo per studiarne le caratteristiche e capire se presentano le caratteristiche tipiche del carcinoma papillare (papille, corpi psammomatosi, pseudoinclusi, nuclei con incisione).
Varianti istologiche
In base al WHO 2017 sono riconosciute 14 forme di varianti istologiche di cui le più conosciute sono: follicolare (più comune), oncocitaria (cellule Askenazi o di Hurtle o cellule ossifile), a cellule chiare, sclerosante diffusa, a cellule alte, a cellule colonnari (nucleo allungato e ipercromico). Identificare le varianti è importante perché sono collegate ad un comportamento clinico diverso (diversa aggressività, capacità di metastasi, associazione con alterazioni genetiche particolari).
- VARIANTE FOLLICOLARE
Cellule neoplastiche con morfologia classica del papillare che si aggregano a formare un pattern follicolare (per poter essere considerato tale vi devono essere più del 75% di follicoli). È una forma a capsula ed ha meno incidenza di metastasi. Si distingue in due sottotipi: infiltrativa e incapsulata con invasione.
Alterazioni genetiche: mutazioni RAS, mutazioni BRAF (con riduzione attività BRAFK), riarrangiamento RET/PTC. - VARIANTE SCLEROSANTE DIFFUSA
È tipica nei soggetti giovani ed insorge su tiroidite di Hashimoto. È caratterizzata da una crescita papillare mescolata ad aree solide contenenti nidi di metaplasia squamosa. Si evidenzia una fibrosi estesa con infiltrato linfocitario; sono presenti metastasi linfonodali anche quando il tumore è piccolo e nel 50% dei casi il tumore è associato a traslocazione RET/PTC. - VARIANTE A CELLULE ALTE
Presenta un pattern “a binario” con cellule alte, con citoplasma eosinofilo, che rivestono le papille. Questa variante insorge negli anziani. Si evidenzia una maggior incidenza di invasioni vascolari che portano a metastasi cervicali.
Alterazioni genetiche: 55-100% associato a mutazioni BRAF oppure traslocazioni RET/PTC. Se sono presenti entrambe le mutazioni avremo un tumore aggressivo. - MICROCARCINOMA PAPILLARE
È un tumore di piccole dimensioni, < 1cm, confinato alla tiroide possono essere TUMORI OCCULTI O SCLEROSANTI OCCULTI in quanto il riscontro è occasionale ed avviene solo in tiroide asportata per patologie non neoplastiche come il gozzo multinodulare oppure in corso di autopsia.
Terapia e follow-up
La terapia del carcinoma papillare della tiroide consiste nell’asportazione di tutta la tiroide (tiroidectomia totale).
L’asportazione di un solo lobo tiroideo o del solo nodulo tumorale è da sconsigliare in quanto la presenza di tessuto tiroideo normale residuo impedisce la visualizzazione di eventuali metastasi con la scintigrafia post-operatoria, impedisce l’impiego della tireoglobulina come marker di malattia e favorisce l’espressione di eventuali foci di carcinoma occulto presente nel tessuto tiroideo residuo provocando recidive.
Subito dopo l’intervento chirurgico può essere somministrato dello iodio radioattivo (radioiodio) a dosi ablative (terapia radiometabolica) al fine di distruggere l’eventuale tessuto tiroideo residuo o le eventuali metastasi. In alcuni casi a basso rischio, o in caso di microcarcinomi individuati in seguito a tiroidectomia, la terapia radiometabolica può anche non essere effettuata.
In tutti gli altri casi, dopo la terapia radiometabolica va instaurata una terapia soppressiva con levotiroxina finalizzata ad abbassare i livelli di TSH e quindi a ridurre lo stimolo proliferativo su eventuali foci neoplastici residui.
A distanza di 3 mesi dall’intervento è consigliato un controllo ecografico, il dosaggio della funzione tiroidea, del TSH, della tireoglobulina e degli anticorpi anti tireoglobulina.
A distanza di 6-12 mesi è consigliabile ripetere l’ecografia del collo ed un controllo della tireoglobulina dopo stimolo con TSH ricombinante (Thyrogen).
In base agli esiti di tali accertamenti potranno rendersi necessari ulteriori trattamenti di tipo radiometabolico o chirurgico.
Il tumore papillare della tiroide presenta un tasso di recidiva abbastanza basso e solitamente un terzo delle recidive si verifica entro 10 anni dall’intervento e solitamente solo a livello locale.
Tuttavia sono segnalati casi di recidiva di tumore della tiroide anche dopo 40 anni dall’intervento. Pertanto, anche se il tasso di mortalità per carcinoma papillare della tiroide è più basso rispetto ad altri tumori, è necessario che il follow up del carcinoma tiroideo dopo l’intervento, duri per molti anni se non tutta la vita.
Fonte: Endocrinologia oggi
Fonte: Anatomia patologica e correlazioni anatomo-cliniche (Mariuzzi).