L’emogasanalisi (EGA) è un esame fondamentale che consente di misurare in modo quantitativo i livelli di ossigeno (O₂), anidride carbonica (CO₂) e idrogenioni (H⁺) nel sangue. Da questi parametri primari vengono poi calcolati altri valori importanti, come i bicarbonati (HCO₃⁻), la CO₂ totale, la saturazione di ossigeno (SatO₂) e l’eccesso di basi. I risultati di un’EGA arteriosa forniscono informazioni preziose su tre aspetti principali: l’ossigenazione, la ventilazione e l’equilibrio acido-base.
| Parametro | Valore Normale |
|---|---|
| pH | 7,35 – 7,45 |
| PaCO₂ | 35 – 45 |
| HCO₃⁻ | 24 – 26 |
| Na⁺ | 135 – 150 |
| K⁺ | 3,5 – 5,0 |
| Cl⁻ | 98 – 106 |
| Lattato | < 1,5 |
Valutazione dello stato di ossigenazione
Uno dei parametri fondamentali nell’interpretazione dell’EGA è la pressione parziale di ossigeno nel sangue arterioso (PaO₂), che riflette l’efficienza degli scambi gassosi a livello polmonare. La PaO₂ dipende dalla frazione inspirata di ossigeno (FiO₂) e dalla pressione atmosferica (legge di Dalton: pO2 = FIO2 x Patm).
Ad esempio, a livello del mare, dove la pressione atmosferica è di 760 mmHg, la pressione parziale di O₂ nell’aria inspirata è circa 160 mmHg (0,21 × 760).
Tuttavia, a livello alveolare, la presenza di altri gas (come CO₂, vapore acqueo e azoto) riduce la pressione alveolare di ossigeno (PAO₂) a circa 100 mmHg.
La PaO₂ arteriosa è generalmente 5 mmHg inferiore alla PAO₂ a causa di un lieve shunt fisiologico.
Caricamento….
Un valore di PaO₂ inferiore a 80 mmHg è indicativo di ipossiemia, una condizione che può derivare da alterazioni della ventilazione, della perfusione o della diffusione alveolo-capillare.
La sola valutazione della PaO₂ può essere fuorviante, poiché questo valore è influenzato dalla concentrazione di ossigeno inspirato. Per ovviare a questo limite, si utilizza l’indice di Horowitz (P/F), calcolato come il rapporto tra PaO₂ (pressione arteriosa di O2) e FiO₂ (frazione inspiratoria di ossigeno). In condizioni normali, questo indice è superiore a 450, mentre valori inferiori a 300 suggeriscono un’alterazione degli scambi gassosi.
Un P/F ridotto può essere causato da:
- difetto di ventilazione (es. coma, depressione del centro respiratorio);
- difetto di perfusione (es. embolia polmonare);
- difetto di diffusione (es. polmonite, malattie interstiziali).
Un altro parametro cruciale è il gradiente alveolo-arterioso di ossigeno, che rappresenta la differenza tra la pressione di O₂ a livello alveolare (pAO₂) e quella arteriosa (paO₂). Un aumento di questo gradiente può indicare problemi di perfusione (es. embolia polmonare) o di diffusione (es. polmonite interstiziale).
Il calcolo del gradiente PA-PaO₂ in aria ambiente si ottiene con la formula:
ΔAaO2=[150−(PaCO2/0,8)]−PaO2
I valori normali variano con l’età: ΔAaO2 normale = età/4 ± 4
Ad esempio:
- in un giovane di 20 anni, il range fisiologico è 1–9 mmHg.
- in un soggetto di 60 anni, il valore atteso è 11–19 mmHg.
Un gradiente superiore a 20 mmHg suggerisce un deficit moderato degli scambi gassosi, mentre valori oltre i 50 mmHg indicano un’alterazione severa, come nell’ARDS (Acute Respiratory Distress Syndrome).
Caso clinico esemplificativo
Una donna di 35 anni si presenta con dispnea acuta. L’EGA mostra:
- pH = 7,46;
- PaO₂ = 75 mmHg;
- PaCO₂ = 20 mmHg;
- HCO₃⁻ = 23 mEq/L;
- SatO₂ = 97%.
Il primo passo è calcolare il P/F. Ovvero: P/F=75/0,21 ≈ 357.
Il valore è lievemente ridotto (normale >450).
Il secondo passo è calcolare il gradiente ΔAaO2. ΔAaO2=[150−(20/0,8)]−75= 50 mmHg.
In una paziente giovane, ci si aspetta un valore tra 0 e 8 mmHg. Un gradiente di 50 mmHg è fortemente patologico, suggerendo un’importante alterazione degli scambi respiratori, come un’embolia polmonare.
Analisi del pH
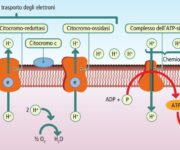
Il pH ematico è un parametro cruciale che riflette l’equilibrio acido-base dell’organismo. Il suo valore è mantenuto entro un range fisiologico (7,35–7,45) grazie a diversi sistemi tampone, sia intracellulari (proteine, emoglobina) che extracellulari (bicarbonati, fosfati). Tra questi, il sistema bicarbonato-acido carbonico (HCO₃⁻/CO₂) è particolarmente importante perché è l’unico “aperto” all’esterno, ovvero può essere rapidamente modificato attraverso la regolazione respiratoria della CO₂ e, più lentamente, attraverso l’aggiustamento renale dei bicarbonati.
- regolazione respiratoria (rapida, entro minuti-ore): l’aumento della ventilazione elimina più CO₂, riducendo l’acidità, mentre una diminuzione della ventilazione trattiene CO₂, aumentandola;
- regolazione renale (lenta, entro ore-giorni): i reni modulano l’escrezione o il riassorbimento di HCO₃⁻ e ioni idrogeno (H⁺), influenzando il pH in modo più duraturo.
Caricamento…
Un’alterazione primaria del pH può essere causata da:
- variazioni della PCO₂ (disturbi respiratori):
- acidosi respiratoria (↑PCO₂, pH <7,35);
- alcalosi respiratoria (↓PCO₂, pH >7,45);
- variazioni di HCO₃⁻ (disturbi metabolici):
- acidosi metabolica (↓HCO₃⁻, pH <7,35);
- alcalosi metabolica (↑HCO₃⁻, pH >7,45).
Attenzione ai casi complessi:
- disturbi compensati: un pH normale con alterazioni marcate di PCO₂ e HCO₃⁻ può indicare un disturbo primario ben compensato (es. acidosi respiratoria cronica con aumento renale di bicarbonati).
- disturbi misti: la contemporanea presenza di due alterazioni primarie (es. acidosi respiratoria + alcalosi metabolica) può mascherare il pH, rendendo necessaria un’analisi più approfondita.
Caso clinico: paziente con BPCO e Squilibrio Acido-Base
Un uomo di 55 anni, affetto da BPCO e cuore polmonare cronico, in terapia con diuretici tiazidici, giunge in PS per peggioramento di tosse e dispnea ed espettorato senza addensamenti all’RX torace. Il medico del Pronto Soccorso lo ricovera con diagnosi di riacutizzazione di BPCO. L’EGA mostra:
- pH = 7,42 (normale);
- PaO₂ = 63 mmHg (ipossiemia);
- PaCO₂ = 87 mmHg (ipercapnia marcata);
- HCO₃⁻ = 55 mEq/L (bicarbonati elevati).
La prima cosa da notare è che il pH è normale, anche se la CO2 e gli ioni HCO3 sono fortemente alterati.
Interpretazione:
- acidosi respiratoria primaria: l’elevata PaCO₂ (87 mmHg) suggerisce un’ipoventilazione da riacutizzazione di BPCO;
- alcalosi metabolica compensatoria: l’aumento dei bicarbonati (55 mEq/L) è dovuto a:
- compenso renale cronico (tipico della BPCO avanzata, dove i reni trattengono HCO₃⁻ per contrastare l’acidosi).
- effetto dei diuretici tiazidici, che possono ulteriormente aumentare i bicarbonati attraverso la deplezione di cloro.
Conclusioni:
Si tratta di un disturbo misto:
- acidosi respiratoria (da riacutizzazione di BPCO).
- alcalosi metabolica (da compenso renale e terapia diuretica).
Nonostante il pH sia normale, le alterazioni estreme di PaCO₂ e HCO₃⁻ richiedono un trattamento mirato:
- correzione dell’ipossiemia (ossigenoterapia controllata);
- monitoraggio della ventilazione (eventuale supporto ventilatorio se necessario);
- bilancio idroelettrolitico (correzione di eventuali squilibri da diuretici).
Analisi del PCO2 e dei bicarbonati
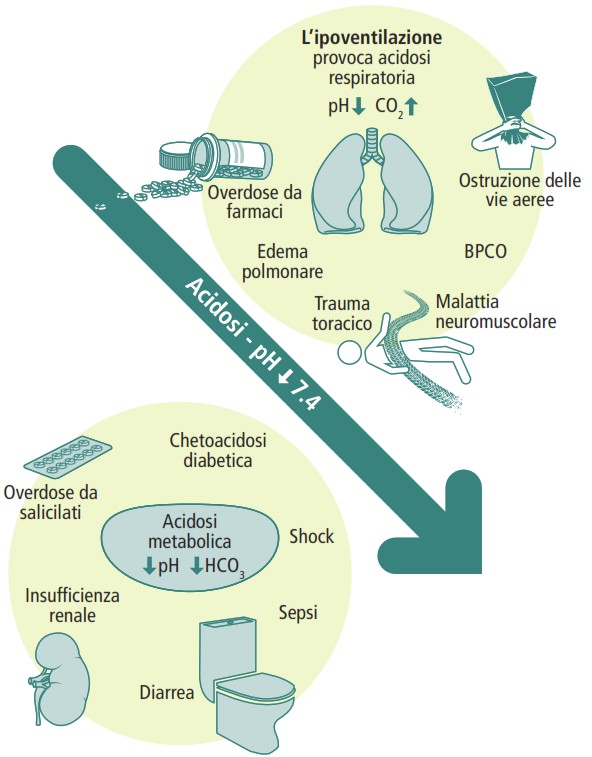
La pressione parziale di anidride carbonica (PCO₂) rappresenta la componente respiratoria dell’equilibrio acido-base. Come già detto, quando la ventilazione polmonare è insufficiente, la PCO₂ aumenta, portando a una condizione di acidosi respiratoria. Al contrario, un’eccessiva eliminazione di CO₂ attraverso l’iperventilazione determina alcalosi respiratoria. Queste alterazioni si manifestano con cambiamenti opposti del pH rispetto alla PCO₂.
I bicarbonati (HCO₃⁻) costituiscono invece la componente metabolica. Il loro aumento o diminuzione riflette rispettivamente condizioni di alcalosi o acidosi metabolica. A differenza della PCO₂, le variazioni dei bicarbonati si muovono nella stessa direzione del pH nei disturbi metabolici primari. Questo comportamento opposto rispetto ai disturbi respiratori aiuta nella diagnosi differenziale.
L’organismo mette in atto sofisticati meccanismi compensatori:
- per i disturbi respiratori, i reni rispondono modificando l’escrezione di bicarbonati;
- nei disturbi metabolici, la compensazione avviene principalmente attraverso variazioni della ventilazione polmonare.
Per distinguere tra disturbi respiratori e metabolici, è utile seguire un approccio sistematico.
Regola mnemonica: “ROME” (Respiratory Opposite, Metabolic Equal):
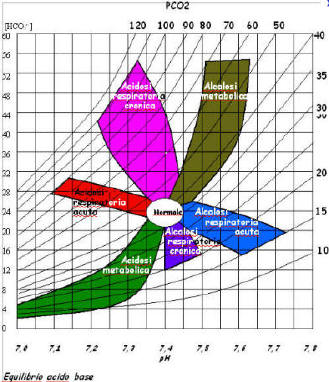
- disturbi respiratori: PCO₂ e pH si muovono in direzioni opposte.
- acidosi respiratoria: ↓pH (<7,35) + ↑PCO₂ (>45 mmHg) → ipoventilazione (es. BPCO, overdose da oppioidi);
- alcalosi respiratoria: ↑pH (>7,45) + ↓PCO₂ (<35 mmHg) → iperventilazione (es. ansia, polmonite);
- disturbi metabolici: PCO₂ e pH si muovono nella stessa direzione (compenso respiratorio):
- acidosi metabolica: ↓pH + ↓HCO₃⁻ (<22 mEq/L) + ↓PCO₂ compensatoria (es. chetoacidosi).
- alcalosi metabolica: ↑pH + ↑HCO₃⁻ (>26 mEq/L) + ↑PCO₂ compensatoria (es. vomito prolungato).
Compenso atteso nei disturbi acido-base
| Disturbo | Variazione iniziale | Compenso atteso |
|---|---|---|
| Acidosi respiratoria | Ogni ↑ 10 CO₂ | In acuto → ↑ 1 HCO₃⁻ In cronico → ↑ 3,5 HCO₃⁻ |
| Alcalosi respiratoria | Ogni ↓ 10 CO₂ | In acuto → ↓ 2 HCO₃⁻ In cronico → ↓ 4 HCO₃⁻ |
| Acidosi metabolica | Ogni ↓ 1 HCO₃⁻ | ↓ 1,2 CO₂ |
| Alcalosi metabolica | Ogni ↑ 1 HCO₃⁻ | ↑ 0,5 CO₂ |
Caso clinico 1
Consideriamo il caso di un paziente di 60 anni, affetto da ipertensione arteriosa e in trattamento cronico con diuretici dell’ansa e ACE-inibitori, si presenta con i seguenti valori all’emogasanalisi arteriosa (EGA):
- pH: 7,58;
- pO₂: 91,6 mmHg;
- pCO₂: 50,8 mmHg;
- HCO₃⁻: 47,0 mEq/L.
Di fronte a questi risultati, il primo passo è l’analisi del pH: essendo 7,58, ci troviamo chiaramente in una condizione di alcalosi. A questo punto, è necessario valutare la direzione delle altre componenti per capire se il disturbo sia di origine metabolica o respiratoria. In questo caso, osserviamo che anche la pCO₂ è aumentata (50,8 mmHg), quindi si muove nello stesso verso del pH, il che indica che il disturbo primario è metabolico. Siamo dunque di fronte a un quadro di alcalosi metabolica.
La domanda successiva è: questa alcalosi è compensata? Per rispondere, possiamo fare riferimento ai criteri di compenso atteso. In caso di alcalosi metabolica, il compenso respiratorio si traduce in un aumento della pCO₂ pari a circa 0,5 mmHg per ogni aumento di 1 mEq/L di HCO₃⁻. Considerando che il valore normale di HCO₃⁻ è di circa 24 mEq/L, e che nel nostro caso il paziente ha un HCO₃⁻ pari a 47 mEq/L, l’incremento totale è di 23 mEq/L.
Moltiplicando questo incremento per 0,5 otteniamo un valore atteso di aumento della pCO₂ pari a 11,5 mmHg. Sommando questo incremento al valore normale di partenza della pCO₂ (circa 40 mmHg), ci aspetteremmo quindi un valore intorno a 51,5 mmHg.
Il valore misurato della pCO₂ è di 50,8 mmHg, molto vicino a quello previsto. Possiamo quindi concludere che il compenso respiratorio è presente e adeguato.
In sintesi, ci troviamo di fronte a un caso di alcalosi metabolica con compenso respiratorio appropriato, verosimilmente secondaria all’uso cronico di diuretici dell’ansa, noti per indurre perdite di potassio e idrogenioni con conseguente alcalosi.
Caso clinico 2
Un giovane di 20 anni arriva in PS lamentando vertigini. Non presenta segni di distress respiratorio né patologie polmonari note. All’esame obiettivo, si evidenzia un respiro rapido e superficiale, ma i parametri vitali sono stabili. Viene eseguita un’emogasanalisi arteriosa che mostra:
- pH 7,63;
- pCO₂ 20 mmHg;
- pO₂ 132 mmHg;
- HCO₃⁻ 21 mEq/L.
Il rapporto P/F (PaO₂/FiO₂) è di 628, indicativo di un’ossigenazione perfettamente conservata.
L’analisi parte dal pH: essendo 7,63, siamo chiaramente in una condizione di alcalosi. La pCO₂ è marcatamente ridotta (20 mmHg), quindi si muove in direzione opposta rispetto al pH: questo indica che il disturbo primario è respiratorio. Si tratta di una alcalosi respiratoria.
A questo punto, è utile determinare se il disturbo sia acuto o cronico, valutando il compenso metabolico. Secondo la fisiologia del compenso, in un’alcalosi respiratoria acuta, per ogni riduzione di 10 mmHg della pCO₂, i bicarbonati si riducono di circa 2 mEq/L. In caso di disturbo cronico, invece, la riduzione è di circa 4 mEq/L per ogni 10 mmHg di calo della pCO₂.
Nel nostro caso, il valore normale atteso di pCO₂ è 40 mmHg, e il valore misurato è 20 mmHg: quindi si è verificata una riduzione di 20 mmHg. Applicando le formule del compenso:
- In caso di alcalosi respiratoria acuta:
2 mEq × 2 = 4 mEq di riduzione → HCO₃⁻ atteso = 24 – 4 = 20 mEq/L - In caso di alcalosi respiratoria cronica:
4 mEq × 2 = 8 mEq di riduzione → HCO₃⁻ atteso = 24 – 8 = 16 mEq/L
Nel paziente in esame, l’HCO₃⁻ misurato è 21 mEq/L, valore che si avvicina molto al compenso atteso per un disturbo acuto. Possiamo quindi concludere che si tratta di una alcalosi respiratoria acuta, con compenso metabolico coerente.
L’ossigenazione arteriosa (pO₂ = 132 mmHg) è normale, e il rapporto P/F è molto elevato, escludendo quindi una causa ipossica dell’iperventilazione. Non siamo nemmeno di fronte a un disturbo dello scambio gassoso.
Alla luce di tutti questi dati, la causa più probabile dell’iperventilazione è uno stato d’ansia acuto, che ha determinato un’iperventilazione marcata con sviluppo di alcalosi respiratoria.
Acidosi metabolica: calcolo dell’anion gap
Quando ci troviamo di fronte a un’acidosi metabolica, è fondamentale calcolare l’anion gap per meglio comprendere la causa sottostante del disturbo. L’organismo tende a mantenere l’elettroneutralità, ovvero un equilibrio tra le cariche elettriche positive e negative. Tuttavia, non tutti gli ioni presenti nel sangue sono facilmente misurabili in laboratorio: alcune cariche, come quelle associate alle proteine plasmatiche, non vengono rilevate.
Per ovviare a questo limite, si utilizza il gap anionico, che rappresenta la differenza tra le cariche positive e negative misurabili. La formula classica per il calcolo è:
AG=(Na++K+)−(Cl−+HCO3−)
Tuttavia, poiché la concentrazione di potassio è generalmente bassa e incide poco sul risultato, spesso si usa la formula semplificata:
AG= Na+−(Cl−+HCO3−)
Il valore normale dell’anion gap, considerando solo sodio, cloro e bicarbonato, è di circa 12 ± 4 mEq/L. Se si include anche il potassio, l’intervallo si alza leggermente, arrivando a 15 ± 4 mEq/L.
Un anion gap aumentato indica che l’acidosi è causata da un accumulo di acidi organici nel sangue. In queste situazioni, il bicarbonato viene “consumato” per tamponare l’eccesso di H⁺, lasciando spazio a anioni non misurabili che fanno salire il gap. Le principali cause di acidosi metabolica con anion gap elevato includono:
- acidosi lattica (es. nello shock settico);
- chetoacidosi diabetica;
- acidosi alcolica;
- uremia.
Al contrario, un anion gap normale è tipico delle cosiddette acidosi metaboliche ipercloremiche, in cui la perdita di bicarbonato (es. per via intestinale o renale) è bilanciata da un aumento di cloro. In questi casi il gap non varia, ma si osserva un’inversione tra HCO₃⁻ e Cl⁻. Le cause principali sono:
- diarrea (perdita extrarenale di bicarbonati);
- acidosi tubulare renale;
- infusione di soluzione fisiologica (che contiene un’elevata concentrazione di cloro, circa 154 mEq/L);
- insufficienza renale acuta prerenale.
Disturbi acido-base: principali cause
- acidosi respiratoria: dovuta a ipoventilazione, come in caso di coma, malattie neuromuscolari o intossicazione da oppiacei;
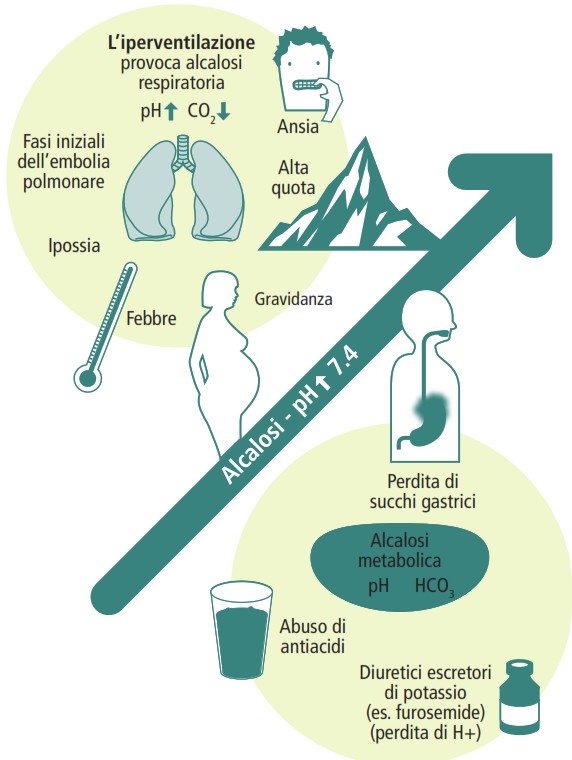
- alcalosi respiratoria: secondaria a iperventilazione, che può avvenire in caso di embolia polmonare, esposizione ad alta quota o attacchi di panico;
- alcalosi metabolica: tipicamente legata a disidratazione, uso di diuretici dell’ansa, vomito prolungato o abuso di antiacidi;
- acidosi metabolica (vedi paragrafo precedente).
Valutazione di K⁺, emoglobina e glucosio
Nella valutazione di un paziente con squilibrio acido-base è altrettanto importante controllare il potassio (K⁺), l’emoglobina (Hb) e la glicemia. Questi parametri possono indicare condizioni sottostanti gravi, che richiedono un intervento tempestivo. L’emogasanalisi può offrire un primo allarme in caso di:
- iperkaliemia o ipokaliemia, entrambe potenzialmente pericolose per l’attività elettrica cardiaca;
- anemia grave, attraverso un valore di Hb ridotto;
- iperglicemia marcata, indicativa di uno stato iperosmolare o di una chetoacidosi diabetica.
La valutazione integrata dei dati dell’EGA con questi parametri permette una diagnosi più completa e un intervento clinico più mirato.
Fonte: Manuale di anestesia e rianimazione. Concorso Nazionale SSM.