L’acqua è una molecola che ha un ruolo importantissimo per la sopravvivenza degli organismi viventi. Sul pianeta Terra essa copre il 71,11% della superficie ed è il principale costituente del corpo umano. E’ proprio dall’acqua che si è generata la vita sulla Terra e le funzioni vitali degli esseri viventi giocano quasi tutte sulle proprietà di questo composto.
La formula chimica dell’acqua è H2O, una molecola polare in quanto gli atomi legati da legame covalente non condividono gli elettroni equamente. Infatti l’ossigeno, essendo più elettronegativo, attira mediamente di più gli elettroni verso di sé. La polarità dell’acqua consente la formazione del legame idrogeno. Ogni molecola d’acqua può legare a sé mediante legame idrogeno altre quattro molecole d’acqua.
Una caratteristica dell’acqua è quella di essere meno densa allo stato solido, questa condizione è dovuta al fatto che il ghiaccio è formato da una struttura reticolare più ordinata, rigida e stabile rispetto all’acqua liquida. Grazie a questa caratteristica è possibile la vita delle specie marine anche nelle zone polari caratterizzate dalla presenza di ghiacciai che galleggiano ed impediscono il congelamento degli oceani.
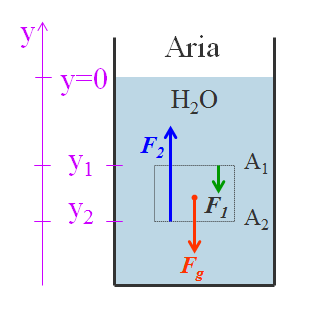
I legami idrogeno dell’acqua garantiscono un’altra proprietà importante, quella dell’elevata coesione. Le molecole d’acqua tendono ad unirsi tra loro consentendo, per esempio, il trasporto di liquidi dalle radici alle foglie degli alberi anche sfidando la forza di gravità.
Un’altra proprietà è la tensione superficiale elevata, quella che garantisce agli insetti di camminare sull’acqua. (Guarda questo video per vedere alcuni semplici esperimenti che sfruttano la tensione superficiale).
Importante è anche l’elevata capacità termica dell’acqua, di gran lunga superiore rispetto a qualsiasi liquido comune. L’acqua immagazzina e rilascia elevate quantità di calore con minime variazioni di temperatura perché è necessaria una grossa quantità di energia (sotto forma di calore) per rompere i legami idrogeno. Questa proprietà è molto importante per la vita perché permette di stabilizzare la temperatura ambientale e quella corporea. In particolare il nostro organismo, essendo composto prevalentemente da acqua, sfrutta questa proprietà per poter regolare la temperatura del corpo attraverso il meccanismo della sudorazione.
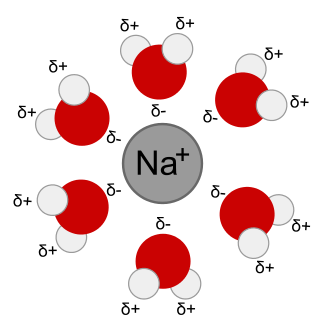
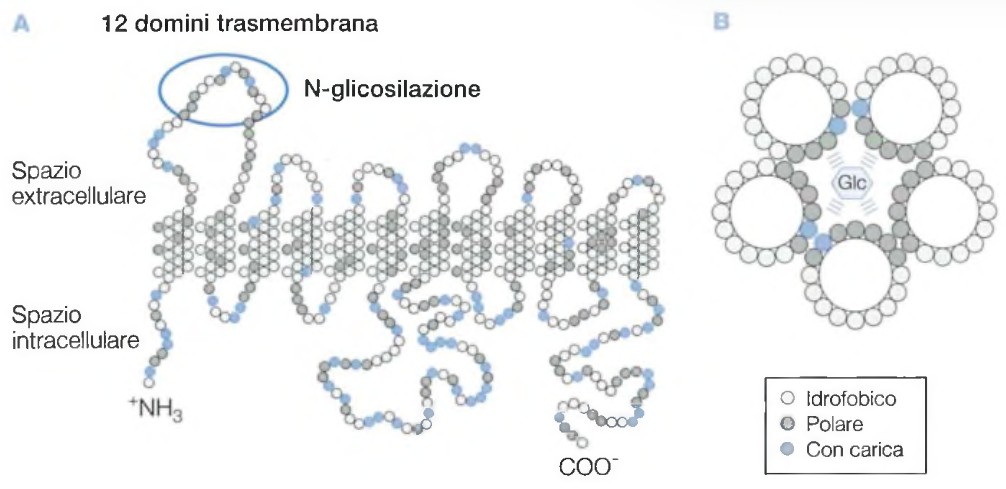
Oltre a queste caratteristiche, l’acqua è un ottimo solvente di ioni e molecole polari o cariche. La capacità di solubilizzare le sostanze è dovuta alla rottura dei legami tra le molecole sia nel soluto che nel solvente e al loro intimo mescolamento. Le molecole d’acqua tendono a circondare i soluti polari o carichi sciogliendoli e formando soluzioni acquose. Ogni ione che viene circondato dalle molecole d’acqua viene detto idratato o solvatato e le sue dimensioni sono maggiori rispetto a quelle degli ioni non idratati.
I composti apolari, invece, sono insolubili in acqua e possono essere semplicemente dispersi nel mezzo acquoso formando delle emulsioni instabili. Questa insolubilità è dovuta al fatto che tra il soluto e l’acqua non possono formarsi legami sufficientemente forti da compensare l’energia richiesta per la rottura dei legami idrogeno tra le molecole di acqua.
Infine esistono i composti anfipatici, come i saponi, che hanno sia una parte polare che una apolare. Questa caratteristica consente loro di interagire con l’acqua tendendo ad andare in soluzione, ma anche da essere espulsi e formare particolari strutture organizzate: micelle, strati monomolecolari e membrane.
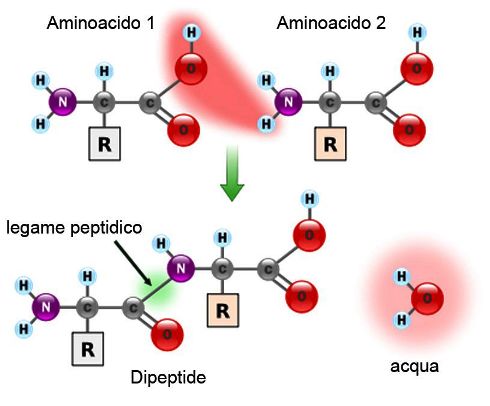
L’acqua è una componente fondamentale di tutti gli organismi viventi presenti sul nostro pianeta. Si trova in elevate percentuali nelle cellule, dove rappresenta il composto predominante, e agisce come solvente per tutte le biomolecole dando loro la possibilità di reagire nelle varie reazioni biochimiche. Oltre che come solvente, l’acqua partecipa attivamente come reagente in diverse reazioni metaboliche, soprattutto quelle di idrolisi, ed è, assieme all’anidride carbonica, uno dei principali reagenti della fotosintesi clorofilliana; è inoltre, sempre assieme alla CO2, il prodotto conclusivo del processo di respirazione cellulare.
Fonte: Wikipedia.