I virus influenzali di tipo A, B e C sono i tre generi della famiglia Orthomyxoviridae. Il primo isolamento risale al 1933. Nel 1940 venne isolato un virus influenzale antigenicamente differente che fu denominato B per distinguerlo dal primo genere (virus influenzale A). Il terzo genere, C, ha un ruolo epidemiologico e un’importanza clinica molto più modesti.
Il virus influenzale A è l’agente eziologico dell’influenza epidemica. Il virus B causa forme sporadiche e più limitate epidemie. Il virus C provoca infezioni inapparenti o sindromi respiratorie minori tra i bambini.
Morfologia
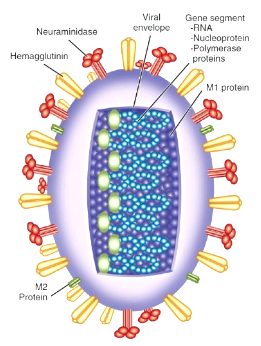
Tutti i virus influenzali hanno simmetria elicoidale, forma sferica, talora filamentosa, diametro da 80 a 120 nm. Contengono un singolo filamento RNA. La struttura appare complessa. il nucleocapside è contenuto in un involucro pericapsidico la cui componente lipidica origina dalla membrana della cellula infetta durante il processo di maturazione del virione.
L’involucro è ricoperto all’interno dalle proteine M1 e M2, che probabilmente intervengono nel processo di assemblaggio del virus e stabilizzano la componente lipidica; all’esterno si proiettano alcune proteine glicosilate virus-specifiche, che formano due distinti “peplomeri”:
- il primo, di forma bastoncellare, è un trimero di polipeptidi, e corrisponde all’attività dell’emoagglutinina. L’emoagglutinina (antigene H) consente ai virus influenzali di aderire alle cellule epiteliali delle vie respiratorie e di penetrare al loro interno durante la fase iniziale dell’infezione. L’emoagglutinina si fissa ai recettori mucoproteici cellulari; a tale fenomeno fa seguito la fusione della membrana virale con quella della cellula ospite. Deve il suo nome alla capacità di agglutinare gli eritrociti, poiché si fissa anche ai recettori mucoproteici di questi ultimi.
- il secondo, di forma allargata all’estremo terminale (a fungo), è un tetramero di polipeptidi e corrisponde all’attività della neuraminidasi.
La neuraminidasi scinde l’acido sialico dalle mucine presenti nelle vie respiratorie, eliminando così un importante fattore in grado di interferire con l’adesione del virus alla superficie delle cellule epiteliali. Secondo un’altra ipotesi, essa avrebbe invece un ruolo nella liberazione dei virioni maturi dalla cellula infettata e nel prevenire la loro aggregazione.
Il nucleocapside consiste in una doppia elica formata dalla nucleoproteina (NP) e dal genoma a RNA. Sono presenti poi tre polimerasi (PB1, PB2 e PA), proteine essenziali per il processo di trascrizione e sintesi dell’RNA virale, e due proteine non strutturali (NS1 e NS2) di funzione ignota. Il genoma del virus influenzale A è frammentato in 8 segmenti, il che facilita i fenomeni di ricombinazione.
I fenomeni di ricombinazione avvengono per:
- drift antigenico ovvero mutazioni puntiformi nel gene dell’emoagglutinina con formazione di una variante che in parte è già conosciuta dal nostro sistema immunitario (immunità limitata ma presente), causando epidemie stagionali. Ciò ci obbliga ad aggiornare costantemente i vaccini.
- shift antigenico ovvero un riassortimento genetico (virus animale e umano) oppure una trasmissione diretta da animali all’uomo (salto di specie), cambia completamente l’emoagglutinina e quindi il virus è completamente sconosciuto al sistema immunitario e tutti sono suscettibili. Tutto ciò causa le pandemie.
I virus influenzali si coltivano agevolmente in uova embrionate di pollo e in colture cellulari (rene di scimmia, tessuto embrionale umano), ove l’emoagglutinina può essere messa in evidenza addizionando eritrociti umani o di cavia che aderiscono alle cellule infettate dando luogo a immagini a “rosette”.
Nei virus influenzali sono riconoscibili 3 antigeni:
- la nucleoproteina (antigene S) generespecifica, stabile, identica in tutti i ceppi del medesimo genere, ma differente per i virus influenzali A, B e C; l’antigene S, quindi, permette di differenziare i virus influenzali nei generi A, B e C.
- l’emoagglutinina (antigene H).
- la neuraminidasi (antigene N), sottotipospecifiche. Insieme agli antigeni H consentono la suddivisione in sottotipi e ceppi dei virus A e B (non sono noti sottotipi del virus C).
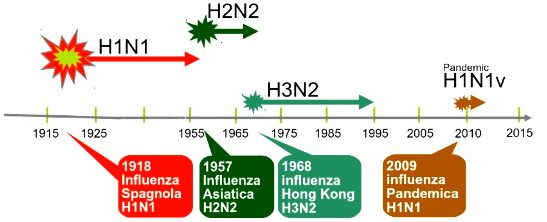
Per quanto concerne il virus influenzale di genere A, sono note 3 varianti antigeniche maggiori dell’antigene H (H1, H2, H3) e 2 dell’antigene N (N1, N2) che, variamente associate, danno origine ai diversi sottotipi.
Le variazioni maggiori degli antigeni N e H, che hanno determinato la comparsa di vari sottotipi, si sono approssimativamente verificate ogni 11 anni. Alla diffusione di ogni nuovo sottotipo è seguita una pandemia influenzale, in quanto il patrimonio anticorpale precedente era inefficace.
Modificazioni minori avvengono ogni 2-5 anni e producono nuovi ceppi nell’ambito del medesimo sottotipo. Ogni nuovo ceppo causa epidemie più o meno limitate, in quanto il patrimonio anticorpale preesistente risulta parzialmente valido.
Alcune osservazioni inducono a prospettare che le modificazioni maggiori del virus influenzale A avvengano in serbatoi animali. La grande pandemia del 1918-19 (influenza spagnola) era infatti associata a un’epidemia di influenza suina negli USA; numerosi animali (volatili da cortile, cavalli, e altri) albergano virus influenzali specifici, ma assai vicini ai virus umani; un virus isolato dal maiale è risultato identico a un ceppo umano. È ipotizzabile, pertanto, che le variazioni antigeniche del virus influenzale umano di genere A siano la risultante di interazioni genetiche tra ceppi umani e animali.
Attualmente i vari virus influenzali sono definiti in base al genere/sede o fonte del ceppo/data/variante degli antigeni H ed N, per esempio: A/Hong Kong/1/68 (H3, N2); A/Taiwan/1/86 (H1, N1). Questa nomenclatura ha sostituito la suddivisione del genere A in A0, A1, A2 sulla scorta delle variazioni della sola emoagglutinina (antigene H).
INFLUENZA
È una malattia infettiva virale causata dai virus influenzali A, B, C. Il virus A causa prevalentemente la forma ad andamento epidemico e talora pandemico; il tipo B le forme sporadiche e le piccole epidemie, mentre il virus C provoca infezioni inapparenti e piccoli focolai tra i bambini.
È altamente contagiosa in quanto viene facilmente trasmessa per via aerea da un soggetto all’altro ed il quadro clinico è tipico, con brusca comparsa di febbre, malessere generale, astenia, dolori muscolari e articolari e flogosi delle vie aeree e delle congiuntive.
Eziologia e trasmissione
Da un punto di vista eziologico il virus A, in base alle variazioni degli antigeni emoagglutinina (H) e neuraminidasi (N), dà origine periodicamente a vari sottotipi e ceppi, responsabili delle ondate epidemiche e pandemiche. Il virus B è antigenicamente più stabile, il virus C è di modestissima rilevanza in patologia umana.
L’influenza si trasmette per inalazione di aerosol prodotti dalla tosse o dagli starnuti di pazienti infetti a stretto contatto (1 metro di distanza), ma in alcuni casi anche per contatto interumano diretto, o tramite veicoli inanimati (superfici e oggetti contaminati). Ai fini del contagio hanno maggiore importanza gli aerosol costituiti da particelle di piccole dimensioni (diametro inferiore a 10 μm). Meno frequentemente si trasmette per via aerea.
Patogenesi
Per quanto riguarda la patogenesi, l’epitelio ciliato delle prime vie aeree, in particolare della mucosa dei turbinati, rappresenta la primitiva sede di impianto e replicazione virale. Le cellule recettive presentano in superficie strutture mucoproteiche il cui gruppo prostetico è il recettore per l’enzima neuraminidasi del virus influenzale. Avvenuta la fissazione alla membrana, il virus penetra, compie il suo ciclo replicativi in 4-6 ore e viene successivamente liberato nel lume dell’albero respiratorio a seguito della lisi della cellula ospite. Così potrà penetrare in altre cellule e diffondersi a macchia d’olio. Per effetto della replicazione virale, ampie zone di epitelio ciliato cadono in necrosi lasciando aree di mucosa disepitelializzate su una base iperemia ed edematosa, facili sedi di sovrinfezioni batteriche.
L’infezione si autolimita e si arresta spontaneamente in 2-5 giorni, mentre prontamente subentrano i processi di rigenerazione che portano a restitutio ad integrum della mucosa respiratoria.
Clinica
Dopo un periodo d’incubazione di 2-3 fino ad un massimo di 7 giorni, la sintomatologia si manifesta con esordio brusco, con febbre che si eleva rapidamente sino a 38-39°C e oltre, preceduta da intensa sensazione di freddo e accompagnata da cefalea, malessere generale, astenia intensa, inappetenza, mioartralgie (sensazione di “ossa rotte” o di “bastonatura”). Precocemente si manifestano segni e sintomi che richiamano l’attenzione sull’apparato respiratorio: compaiono rinite, sensazione di secchezza delle fauci o faringodinia, dolore retrosternale da irritazione tracheale, tosse per lo più secca e stizzosa con espettorato scarso e tenace, fotofobia.
L’obiettività è modesta, limitata ad iperemia congiuntivale e orofaringea e congestione della mucosa nasale.
Il quadro clinico descritto persiste per 3-5 giorni e recede abbastanza bruscamente, mentre la guarigione si completa in una settimana. Una persona adulta può trasmettere in modo efficiente il virus da un giorno prima dell’inizio dei sintomi.
Complicanze
I soggetti a maggior rischio di complicanze sono i bambini al di sotto di 4 anni o bambini con malattie metaboliche, respiratorie, cardiovascolari, renali, epatiche ed ematologiche, immunosoppressi, che fanno uso di aspirina.
Anche gli adulti maggiori di 65 anni, con malattie croniche concomitanti quali l’obesità e donne in gravidanza, sono categorie a rischio di complicanze che possono ancora oggi essere causa di morte.
Tra le complicanze respiratorie, prevale la broncopolmonite batterica secondaria all’infezione virale, mentre assai rara è la broncopolmonite da virus influenzale.
Le broncopolmoniti batteriche secondarie sono dovute alla compromissione del meccanismo di difesa dell’apparato mucociliare e alla disponibilità di pabulum (materiale nutritizio e condizioni ambientali ottimali) offerto dalla mucosa necrotizzata. Ciò permette la moltiplicazione di batteri occasionalmente presenti nel cavo orofaringeo che, con frequenza maggiore in ospiti cardiopatici, anziani, defecati, immunocompromessi, portatori di BPCO, possono raggiungere il parenchima polmonare. Tra i batteri Staphylococcus aureus è frequentemente chiamato in causa, seguito da Streptococcus pneumoniae, Haemophilus influenzae, e altri streptococchi.
La complicanza è contraddistinta dalla ricomparsa della febbre, la tosse diviene produttiva e l’espettorato è abbondante e mucopurulento. L’obiettività toracica e l’Rx documentano presenza di addensamento polmonare. La VES si eleva e compare leucocitosi neutrofila.
La polmonite primitivamente virale segue alla diffusione dell’infezione dalle vie aeree al parenchima. Quando si presenta nelle forme diffuse è particolarmente grave.
Un’altra complicanza è la miocardite influenzale ed è più comune di quanto ritenuto, poiché frequentemente misconosciuta.
L’encefalite postinfluenzale è rara; più frequenti, ma mal documentate, sono invece le nevriti e le radicoliti.
Diagnosi
La diagnosi è basata sulla clinica (febbre maggiore uguale di 38 °C accompagnata dalla sintomatologia: cefalea, malessere generalizzato, brividi, astenia, tosse faringodinia, congestione nasale). Il quadro clinico ha aspetti molto indicativi, ma non risulta patognomico. La diagnosi è clinica dunque solo in fase epidemica. Il metodo più sicuro è l’isolamento del virus e successiva PCR dal tampone o dal liquido di lavaggio nasale, dal tampone faringeo o dal gargarizzato oppure dall’escreato entro i primi 4-5 giorni dall’inizio dei sintomi (quando è maggiormente probabile che la persona elimini i virus). Lievemente meno sensibili, ma di grande utilità pratica, sono i metodi rapidi, quali immunofluorescenza, test immunoenzimatico, che permettono di dimostrare la presenza dei virus influenzali A e B nei campioni biologici in poche ore. I metodi sierologici sono impiegati soprattutto per studi epidemiologici.
Terapia e profilassi
Nell’infezione non complicata la terapia è sintomatica. Deve essere allettato il paziente e gli si assicurerà un adeguato apporto di liquidi. Si somministrano antinfiammatori e analgesici come acido acetilsalicilico.
Utilizzati per trattare la malattia sono invece gli inibitori delle neuraminidasi (antivirali) tra cui Oseltamivir e Zanamivir (rispettivamente Tamiflu e Relenza). Essi vengono utilizzati in soggetti che hanno gravi forme di influenza o nei soggetti ad elevato rischio di sviluppare una complicanza. Vanno somministrati entro 48 ore e con durata di 5 giorni.
Per il trattamento della broncopolmonite batterica secondaria da Staphylococcus aureus si somministrano macrolidi oppure penicilline semisintetiche penicillinasi-resistenti come oxacillina o cloxacillina a pieno dosaggio.
Il principale mezzo di prevenzione è l’immunizzazione attiva mediante vaccini che conferisce protezione per 4-6 mesi nel 90% dei casi. Va effettuata ogni anno in autunno avanzato con inoculazione di una dose da 0,5 mL per gli adulti o due dosi nei bambini. La profilassi immunitaria va effettuata in: anziani, portatori di BPCO, pazienti con diabete mellito, HIV e immunodeficienze, donne al III trimestre di gestazione, personale sanitario o chi lavora a contatto con gli animali.
In caso profilattico, nelle categorie a rischio per lo sviluppo di complicanze, possono essere utilizzati anche gli antivirali quando si è stati in contatto stretto con dei casi confermati, oppure negli operatori sanitari che sono stati esposti al virus senza aver utilizzato DPI.
La prevenzione dal virus avviene lavando spesso le mani con acqua e sapone o con soluzioni detergenti a base di alcol, evitando di toccare occhi, naso e bocca con mani non pulite, evitando contatti ravvicinati (<1.5 metri di distanza) con persone malate. Se non si possono evitare contatti con persone malate indossare mascherine chirurgiche e chiedere alla persona malata di seguire igiene respiratoria e delle mani e di indossare una mascherina.
Fonte: Manuale di malattie infettive.