La tomografia computerizzata (TC) è nata per superare i limiti della sovrapposizione delle immagini legati alla radiologia tradizionale. Questo tipo di imaging utilizza i raggi X per ottenere immagini dettagliate e tridimensionali del corpo.
Gli elementi costitutivi fondamentali di una TC sono:
- tubo radiogeno: si alta qualità, produce un fascio di raggi X omogeneo per diversi secondi;
- sistema di detettori: variabile nelle diverse generazioni di TC, è il sistema di rilevatori di radiazioni;
- workstation dedicata: un software che riceve il segnale dai detettori e lo trasforma in immagini basate sul gradiente di grigi.
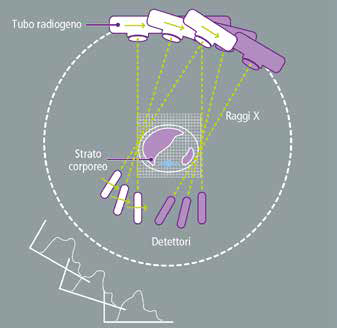
Durante una TC, il paziente è sdraiato su un lettino che si muove all’interno del gantry, un anello che contiene il tubo radiogeno e il sistema di detettori. Il tubo radiogeno ruota continuamente attorno al paziente, emettendo raggi X che attraversano il corpo. I detettori rilevano le radiazioni dopo che hanno attraversato il corpo e trasformano questo segnale in immagini sulla workstation.
Ogni elemento di volume della sezione corporea esplorata è suddiviso in voxel, ciascuno attraversato più volte dai raggi X durante la rotazione del tubo radiogeno. Ogni voxel ha un valore di densità, espresso in unità di Hounsfield (HU), che varia da +1000 (osso compatto) a -1000 (aria), con lo 0 che rappresenta la densità dell’acqua e +60/+90 UH per la densità del sangue. Un ematoma/emorragia sarà tendenzialmente dunque iperintenso nella TC basale senza mezzo di contrasto.
I dati grezzi dell’algoritmo matematico che elabora le letture dei detettori sono valori assoluti di radiodensità per tutti i voxel, su una scala densitometrica chiamata scala Hounsfield (HU). Questi valori vengono quindi tradotti in tonalità di grigio per l’immagine visualizzata sul monitor. Ogni voxel corrisponde a un pixel nell’immagine, con un livello di grigio corrispondente alla densità in HU.
Le moderne TC utilizzano profondità di grigio corrispondenti a 12 bit, quindi 212 = 4.096 possibili tonalità di grigio. Tuttavia, l’occhio umano può percepire distintamente solo 16-20 tonalità di grigio. Per permettere una visualizzazione ottimale, viene selezionato un intervallo di densità (chiamato finestra) che può essere rappresentato dalle tonalità di grigio differenziabili dall’occhio umano. Questo intervallo varia in base alle strutture che si vogliono studiare, come il mediastino, il polmone o l’addome.
Analisi Complesse e Ricostruzioni
La tomografia computerizzata ha attraversato diverse generazioni che hanno portato a uno sviluppo tecnologico sempre più avanzato, semplificando il processo di acquisizione delle immagini e consentendo analisi più dettagliate e ricostruzioni tridimensionali.
- I Generazione: tubo radiogeno con un unico detettore;
- II Generazione: riga lineare di detettori;
- III Generazione: riga circolare incompleta di detettori;
- IV Generazione: corona circolare completa di detettori;
- TC Spirale Volumetrica: ultimo passo, con traslazione del lettino porta-paziente all’interno del gantry, acquisendo immagini in modo spiraliforme. Non più singole fette parallele, ma interi volumi;
- TC Spirale Volumetrica Multistrato: serie di corone circolari di detettori, permettendo la ricostruzione ad alta risoluzione. Esistono macchine TC con 128 e 256 strati.
Una volta acquisito il volume campione e ottenute le immagini sulla workstation, è possibile effettuare delle analisi planimetriche e analisi volumetriche.
Analisi planimetriche
- MPR (Multi Planar Reconstruction): ricostruzione delle immagini in 3 piani dello spazio (trasversale, coronale, sagittale), piani obliqui e curvilinei. Utile per la ricostruzione di strutture tridimensionali e per seguire il decorso di vasi sanguigni.
Analisi Volumetriche
- MIP (Maximum Intensity Projection): evidenzia i voxel con valori densitometrici più alti, utile per la valutazione vascolare e dello scheletro.
- MinIP (Minimum Intensity Projection): evidenzia i voxel a densità minore, usato per la valutazione delle vie aeree.
- Surface Rendering o SSD (Shaded Surface Display): fornisce informazioni sulla relazione tra vasi sovrapposti, utile nella pianificazione preoperatoria e terapeutica.
- Volume Rendering: utilizza l’algoritmo VR per visualizzare in 3D i vasi sanguigni e altre strutture.
- VE (Virtual Endoscopy): Visualizza strutture canalicolari o cavità da una prospettiva intraluminale, simile a un’endoscopia virtuale.
Queste analisi complesse e tecniche di ricostruzione tridimensionale consentono agli operatori sanitari di ottenere una visione dettagliata e completa delle strutture anatomiche, facilitando la diagnosi e la pianificazione del trattamento.
Mezzo di Contrasto
La TC può essere eseguita con o senza l’uso di un mezzo di contrasto iodato, a seconda delle indicazioni diagnostiche. Vi sono scenari clinici in cui lo studio senza mezzo di contrasto è sufficiente, come nel caso di calcolosi ureterale o patologia infettiva polmonare. Tuttavia, ci sono situazioni in cui è indicato l’utilizzo del contrasto, ad esempio:
- Lesioni vascolari (ad esempio, emorragia occulta addominale);
- Traumi (ad esempio, rottura di un aneurisma aortico);
- Valutazione di lesioni focali;
- Valutazione del decorso ed escrezione del mezzo di contrasto attraverso le vie urinarie.
La somministrazione di mezzo di contrasto iodato per via endovenosa permette di evidenziare e valutare con maggior dettaglio il sistema vascolare e le strutture vascolarizzate, sia in studi urgenti che elettivi. La quantità, la velocità e la durata della somministrazione possono essere regolate per documentare al meglio la radiodensità delle strutture in esame all’arrivo del mezzo di contrasto (contrast enhancement). Successivamente, il mezzo di contrasto viene eliminato per via renale.
In base al tempo trascorso tra la somministrazione del contrasto e l’acquisizione delle immagini, si definiscono delle fasi standardizzate per realizzare i principali studi:
- Fase Arteriosa: eseguita a 30-35 secondi dalla somministrazione del contrasto. In questa fase si ottiene un enhancement massimo nei distretti vascolari arteriosi, permettendo una valutazione dettagliata delle lesioni vascolari e delle arterie;
- Fase Venosa: eseguita a 65-70 secondi dalla somministrazione del contrasto. In questa fase si ottiene un enhancement massimo nei distretti vascolari venosi e portali epatici. È utile per la valutazione delle vene e delle strutture vascolari venose;
- Fase Tardiva: eseguita a 5-10 minuti dalla somministrazione del contrasto. In questa fase si ottiene un enhancement localizzato a livello di strutture che mantengono l’impregnazione a causa di un lento wash-out. È utile per la valutazione di lesioni con caratteristiche particolari.
Per riconoscere una TC in fase arteriosa bisogna osservare che l’aorta sia ipertensa per la presenza di contrasto, la milza marezzata e la corticale dei reni iperdensa contrastata.
Le reazioni avverse ai mezzi di contrasto iodati (MDC) possono essere divise in due categorie principali:
- Effetti chemiotossici (Tipo A): questi effetti dipendono dalla dose di contrasto somministrata. Presentano un’alta incidenza, ma tendono a essere raramente gravi. Sono influenzati dalle caratteristiche del paziente, come la presenza di una nefropatia. Gli organi più colpiti da questi effetti sono:
- rene: è l’organo più suscettibile, soprattutto in caso di nefropatia preesistente. L’uso di MDC è sconsigliato in pazienti con alterazione della funzione renale, con valori di creatinina >1.5 mg/dL o filtrato glomerulare <60 mL/min;
- cuore: può essere danneggiato dall’osmolarità del MDC, che può richiamare liquidi all’interno dei vasi, aumentando la volemia e potenzialmente causando sovraccarico del sistema cardiovascolare;
- Sistema Nervoso Centrale (SNC): può subire la tossicità diretta del MDC, soprattutto se la barriera emato-encefalica è alterata;
- Effetti anafilattoidi (Tipo B): questi effetti sono imprevedibili e possono derivare da reazioni allergiche o pseudo-allergiche a specifici costituenti del MDC. Possono variare da lievi, come una sensazione di calore o dermatite cutanea, a potenzialmente letali, come edema della glottide o reazioni anafilattiche sistemiche.
Comuni controindicazioni all’utilizzo di MDC iodati includono lo stato di insufficienza renale e una storia anamnestica di reazioni gravi pregresse.
Se l’esame con MDC è indispensabile per la prognosi del paziente e dopo aver escluso altre opzioni diagnostiche che non richiedono l’uso di MDC (come ecografia o RM), si possono prendere in considerazione le seguenti misure:
- In caso di insufficienza renale, si può considerare l’esecuzione di dialisi immediatamente dopo l’acquisizione dell’esame TC per rimuovere il MDC;
- Per pazienti con diatesi allergica, può essere considerata un’opportuna premedicazione con steroidi e antistaminici per ridurre il rischio di reazioni anafilattoidi.
È fondamentale che il medico valuti attentamente la situazione clinica del paziente, inclusi i rischi e i benefici dell’utilizzo del MDC, prima di procedere con l’esame TC con mezzo di contrasto iodato. La sicurezza del paziente deve sempre essere una priorità durante la pianificazione e l’esecuzione di tali procedure.




