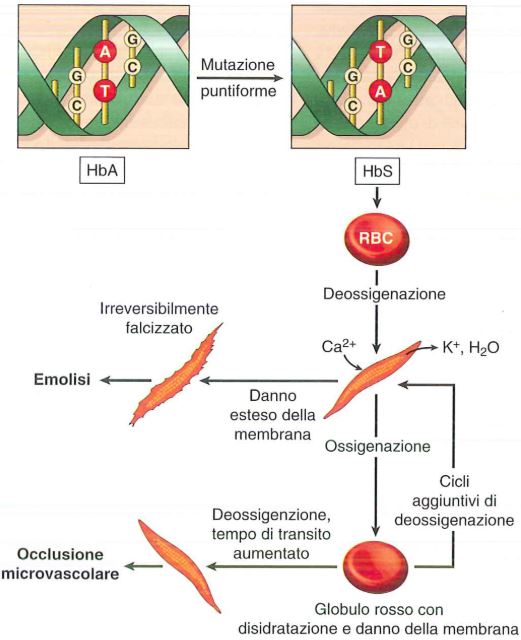
La drepanocitosi (anemia drepanocitica) o anemia falciforme, è un’anemia emolitica causata da una mutazione puntiforme in posizione 6 della catena β dell’emoglobina in cui un acido glutammico viene sostituito con valina, mutazione che trasforma una adenina in timina (e quindi uracile a livello di RNA: GAG->GUG). Quindi l’amminoacido codificato dal nuovo codone, la valina, ha caratteristiche biochimiche diverse, e fa sì che l’emoglobina HbS tende a formare dei veri e propri aggregati (a causa della valina, residuo idrofobico che interagisce con la tasca idrofobica delle catene β vicine) specialmente in condizioni di ipossia.
Nel momento in cui questi aggregati aumentano di numero sono anche in grado di distorcere quella che è la struttura normale del globulo rosso fino a fargli assumere una forma a falce, questo perché nel momento in cui l’HbS polimerizza, trasforma il citosol da liquido a gel viscoso portando alla formazione di fibre HbS. La nuova emoglobina si chiama HbS (S sta per sickle= falce). La falcizzazione inizialmente è reversibile in seguito all’ossigenazione, ma nel momento in cui vi è un danno di membrana, a causa della perdita di ioni, si ha perdita di acqua, quindi l’HbS si concentra in citosol e così la falcizzazione diventa irreversibile. L’entità della polimerizzazione dell’HbS dipende dalla concentrazione cellulare di emoglobina (aumenta dopo rottura membrana per fuoriuscita di acqua).
La malattia è autosomica recessiva, tuttavia la condizione di eterozigote è un vantaggio per impedire l’insorgenza della malaria: questi globuli rossi falcemici impediscono la replicazione al plasmodio (Plasmodium Falciparum) veicolato dalla zanzara Anopheles. Ciò è legato sia al fatto che i globuli rossi falcemici hanno una vita media minore, circa 20 giorni, e sia i bassi livelli di potassio (a causa della sua fuoriuscita dalla cellula), fattori che portano alla morte del parassita (è stato dimostrato che il potassio serve per la sua crescita). In particolare il potassio esce perché a basse concentrazioni di ossigeno questi globuli rossi, in seguito al danno di membrana (a sua volta causato dalle fibre HbS) si caricano di calcio (quindi entra calcio) che attiva un canale del potassio.
Le talassemie sono endemiche nelle stesse aree dell’anemia falciforme e anche in questo caso i globuli rossi hanno vita media inferiore e fanno “da protezione” dall’infezione di questi parassiti.
Circa l’8% degli americani di colore è eterozigote per HbS. Nei paesi dove la malaria è endemica, fino al 30% dei neri africani è eterozigote perché l’eterozigosi dà il cosiddetto vantaggio del portatore.
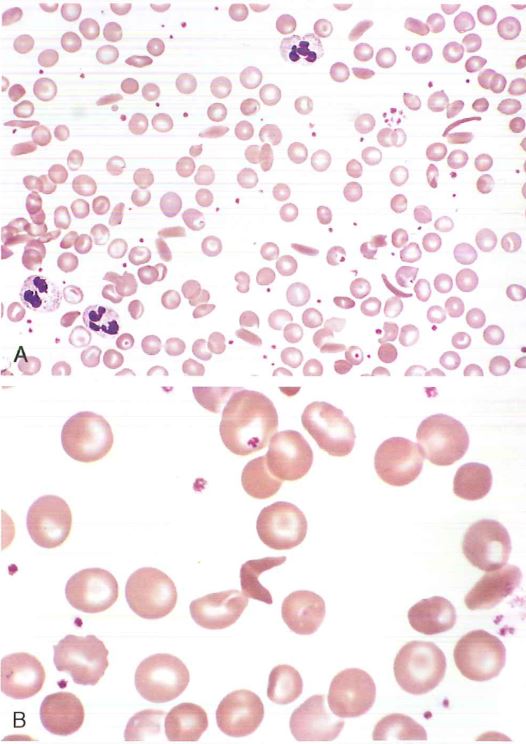
A: A un basso ingrandimento si notano cellule falciformi, anisocitosi e poichilocitosi.
B: A elevato ingrandimento si evidenzia una cellula che ha acquisito irreversibilmente la forma a falce.
(Per gentile concessione del Dr, Robert W. McKenna, Department oi Pathology, University of Texas Southwestern Medical School, Dallas, TX);
Fonte: Le basi patologiche delle malattie.
Una caratteristica dell’anemia falciforme è che non compare subito dopo la nascita perché per i primi 6 mesi di vita è presente emoglobina fetale che impedisce la polimerizzazione di HbS. Quindi la malattia si manifesta dopo il 5°/6° mese di vita, cioè quando l’emoglobina fetale viene sostituita dall’emoglobina adulta.
Oltre alla classica mutazione glutammato/valina, ci può essere un altro tipo di mutazione sempre in posizione 6 in cui glutammato è sostituito con lisina. In questo caso l’emoglobina è chiamata HbC. Le HbC non formano aggregati come le HbS.
Ci sono anche individui eterozigoti in cui su un allele hanno mutazione HbS e sull’altro HbC. Paradossalmente questi individui hanno effetti minori rispetto agli omozigoti di HbS, questo è dovuto al fatto che HbC polimerizza con HbS impedendo che HbS polimerizzi con altre HbS. Questi aggregati HbC/HbS non sono importanti (soprattutto per quanto riguarda le dimensioni) come quelli HbS/HbS e quindi la patologia è meno grave. Gli individui eterozigoti per HbS e HbC hanno una patologia falcizzante sintomatica (malattia HbSC) più lieve rispetto alla anemia falciforme.
L’anemia falciforme è recessiva, tuttavia gli individui eterozigoti portatori comunque presentano globuli rossi anomali (in questo caso non sono del tutto falcemici e non ci son danni alla membrana) pur non avendo nessun sintomo di malattia, quindi per il clinico la patologia è recessiva invece per l’ematologo è dominante perché basta una sola mutazione per poter osservare al microscopio globuli rossi anomali.
HbA interagisce debolmente con HbS: i globuli rossi in soggetti eterozigoti non falcizzano se non in condizioni di grave ipossia. La condizione di eterozigosi per HbS è nota come tratto falcemico. Il tratto falcemico non presenta né emolisi né anemia. Gli eterozigoti HbC/HbA sono asintomatici. Chiaramente, in condizioni di ipossia, anche i portatori comunque avranno degli effetti come la falcizzazione dei globuli rossi.
Manifestazioni cliniche
Anemia emolitica cronica: i globuli rossi irreversibilmente falcizzati si trasformano in cellule rigide e vengono subito sequestrati e rimossi dai fagociti mononucleati (in milza si ha emolisi extravascolare, ma anche intravascolare perché i globuli rossi a falce sono anche più fragili ed hanno un’emivita di circa 20 giorni).
Laddove vi è un’occlusione ischemica si può avere un danno ischemico. A seguito del processo infiammatorio che ne consegue, l’endotelio esprime più molecole di adesione e quindi aumenta l’adesività favorendo le occlusioni. Inoltre, poiché i globuli rossi hanno un transito più lento proprio a causa della loro maggiore adesività, sono esposti ad una tensione di ossigeno più bassa e questo favorisce un aumento della falcizzazione e un aggravamento dell’occlusione (la falcizzazione avviene dove il flusso sanguigno è lento).
A seguito dell’emolisi cronica si ha catabolismo di eme in bilirubina e quindi iperbilirubinemia con manifestazione di ittero.
Vi è inoltre un’iperplasia del midollo osseo poiché tende a compensare l’anemia (quindi si ha una sintesi notevole di EPO proprio per favorire la sintesi di nuovi globuli rossi). Questa iperplasia tuttavia è tale che il midollo osseo invade poi la corticale dell’osso con comparsa di neoformazioni e anomalie a livello osseo (comparsa di cranio a spazzola e zigomi prominenti facilmente visibile ai Raggi X).
I globuli rossi sono maggiormente suscettibili a infezioni da organismi capsulati come Haemophilus influenzae (coccobacillo gram negativo).
Si può avere inoltre occlusione vascolare (cervello, rene, ossa, polmoni, fegato e retina) e autosplenectomia, ovvero la necrosi della milza dovuta ad una congestione della polpa rossa causata dall’intrappolamento dei globuli rossi falciformi nei cordoni e nei seni splenici. Col tempo, questa eritrostasi cronica, provoca infarto splenico, fibrosi e progressiva riduzione del volume della milza.