Il ferro organico, presente nei prodotti alimentari di origine animale come l’eme della carne rossa, è rapidamente assorbito dall’organismo. D’altra parte, il ferro non organico, che è più abbondante, può essere assorbito in forma ridotta (come ione ferroso o Fe++) ma il processo è più lento.
L’assorbimento intestinale del ferro avviene principalmente nel duodeno e nel digiuno prossimale e medio. Fattori come il pH acido gastrico, la presenza di vitamina C e citrato favoriscono l’assorbimento del ferro, mentre cereali, tannati e fitati (presenti nelle verdure) ne limitano l’assorbimento. Una persona sana dovrebbe assorbire almeno 1 mg di ferro elementare al giorno, ma in situazioni di aumento della produzione di globuli rossi (eritropoiesi), la richiesta di ferro è maggiore.
Nel corpo umano, il ferro si trova principalmente legato all’emoglobina, alla mioglobina e ai citocromi (noto come ferro “emico”), oppure legato a diverse proteine come ferritina, emosiderina, transferrina, ecc. (ferro “non emico”).
Gli enterociti assorbono il ferro attraverso un trasportatore che lega l’eme, o in forma atomica tramite il trasportatore dei metalli DMT1. All’interno dell’enterocita, parte del ferro viene immagazzinata nella ferritina intracellulare, mentre il resto viene trasferito al lato basale verso il flusso sanguigno, dove il complesso efestina-ferroportina rilascia il ferro per renderlo disponibile alla trasferrina, la principale proteina di trasporto.
La trasferrina trasporta il ferro assorbito sotto forma di ione ferrico (Fe+++) al sistema fagocitico mononucleare e al midollo osseo, dove si lega al recettore della trasferrina e penetra nella cellula. All’interno della cellula, il ferro si lega alla protoporfirina IX nei mitocondri per formare il gruppo eme, che a sua volta si lega alle catene di globina sintetizzate nel nucleo, formando l’emoglobina. Il ferro non utilizzato per la sintesi dell’emoglobina viene immagazzinato nei macrofagi (nella milza e nel fegato) e negli eritroblasti del midollo osseo sotto forma di ferritina ed emosiderina. Nei casi di infiammazione cronica, c’è un rilascio ridotto di ferro dai depositi, un meccanismo modulato dall’epcidina, una proteina epatica di fase acuta.
L’agoaspirato midollare con la reazione di Perls e, in secondo luogo, la misurazione della ferritina sono i migliori parametri per identificare una carenza di ferro (sideropenia). Tuttavia, l’agoaspirato midollare non viene comunemente eseguito per diagnosticare la sideropenia a causa della sua natura invasiva.
Eziologia
La carenza di ferro è la causa più comune di anemia, con diverse ragioni sottostanti:
- Perdita eccessiva. Nei Paesi sviluppati, la perdita di piccole quantità di sangue è la causa principale dell’anemia sideropenica. Le perdite più comuni sono dovute alle mestruazioni nelle donne. Negli uomini e nelle donne non mestruate, le perdite intestinali possono essere significative e includono:
- Emorroidi;
- Esofagite;
- Ulcera peptica;
- Neoplasie;
- Parassiti intestinali (più comune nei Paesi in via di sviluppo);
- Altri fattori come l’uso di FANS, presenza di diverticoli, donazione eccessiva di sangue, analisi frequenti durante ricoveri ospedalieri, e autolesioni (come nella sindrome di Lasthénie de Ferjol);
- Apporto insufficiente. Questa causa è meno comune nei Paesi sviluppati, ma può essere osservata nei bambini fino ai 2 anni di età;
- Diminuzione dell’assorbimento:
- Gastrectomia;
- Acloridria (tipicamente associata all’anemia perniciosa);
- Sindromi da malassorbimento, inclusa la malattia celiaca che può essere sospettata nei pazienti che non rispondono al trattamento con ferro orale. Per diagnosticare la malattia celiaca, vengono generalmente eseguiti test per gli anticorpi antiendomisio e antigliadina di classe IgG e IgA;
- Infezione da Helicobacter pylori senza erosione, che può portare a una diminuzione dell’acidità gastrica e influenzare l’assorbimento del ferro;
- Aumento del fabbisogno. Questo è tipico nei bambini fino ai 2 anni, durante l’adolescenza e durante la gravidanza, quando il fabbisogno di ferro è significativamente aumentato.
Segni clinici
La carenza di ferro può manifestarsi con diversi segni e sintomi:
- Sindrome anemica: la sintomatologia tipica di un’anemia da carenza di ferro include pallore cutaneo-mucoso, dispnea (difficoltà respiratoria), cefalea, nausea, acufeni (fischi alle orecchie), oligoanuria (ridotta produzione di urina), e anoressia (riduzione dell’appetito);
- Sintomi specifici della sideropenia. Oltre alla sindrome anemica, la sideropenia può causare sintomi specifici, tra cui:
- Caduta di capelli;
- Fragilità ungueale (unghie fragili e che si sfaldano facilmente);
- Glossite con atrofia linguale (infiammazione della lingua con perdita di papille e lingua liscia e dolorante);
- Stomatite angolare (ragadi ai lati della bocca);
- Ozena (atrofia della mucosa nasale, causando un odore sgradevole);
- Gastrite atrofica (infiammazione dello stomaco con atrofia dei suoi tessuti);
- Sindrome di Plummer-Vinson (caratterizzata da sideropenia, glossite e disfagia da presenza di membrane ipofaringee ed esofagee);
- Sclere blu (causata da un’alterazione del collagene);
- Epatomegalia (ingrossamento del fegato);
- Sindrome depressiva;
- Infezioni: sono meno comuni, ma possono verificarsi a causa dell’alterazione della capacità battericida dei granulociti dovuta alla carenza di lattoferrina, una proteina coinvolta nella difesa immunitaria.
Diagnosi
Per diagnosticare la carenza di ferro, sono necessari diversi esami:
- Emocromo:
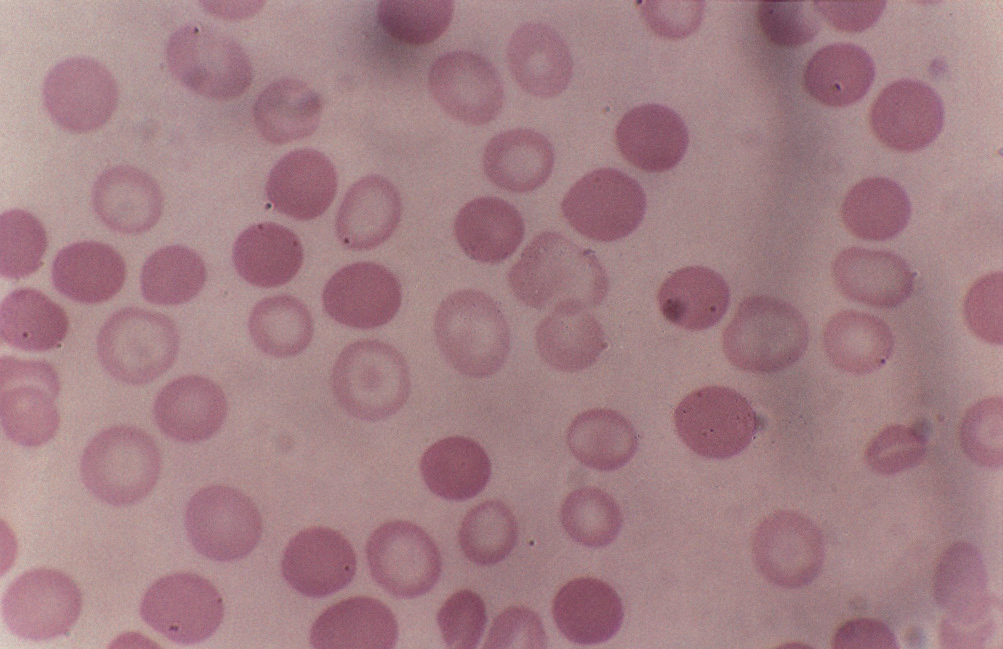
- Numero di globuli rossi generalmente ridotto, con microcitosi (volume corpuscolare medio, MCV, basso) e ipocromia (palloramento dei globuli rossi);
- L’ampiezza della distribuzione eritrocitaria (RDW) è aumentata, indicando anisocitosi (variazione delle dimensioni dei globuli rossi);
- Morfologia del sangue periferico: possono essere presenti emazie pallide, “a bersaglio”, con centro molto chiaro. Poichilocitosi (globuli rossi in forme irregolari) e cellule bersaglio possono essere osservati in caso di anemia significativa;
- Reticolociti generalmente normali o ridotti, ma aumentano rapidamente con il trattamento;
- Possibile presenza di trombocitosi reattiva (aumento delle piastrine) e/o leucopenia/leucocitosi (diminuzione o aumento dei globuli bianchi);
- Metabolismo del ferro:
- Ferritina diminuita: è la prima alterazione di laboratorio osservabile;
- Sideremia (o ferro sierico) bassa;
- Transferrina aumentata;
- Capacità totale di saturazione della transferrina (TIBC) aumentata;
- Indice di saturazione della transferrina (IST) diminuito (<16%);
- Recettore solubile della transferrina (sTfR) molto elevato;
- Protoporfirina libera aumentata: non può legarsi al ferro, quindi si osserva un aumento relativo della protoporfirina libera;
- Emoglobina A2 diminuita;
- Bilirubina diminuita: dovuta alla diminuzione del catabolismo dell’emoglobina;
- Midollo osseo: può mostrare assenza o diminuzione dei depositi di ferro nei macrofagi e nei sideroblasti, confermando la carenza di ferro.
| Ferro sierico: Transferrina: TIBC: IST: Ferritina: | 50-150 μg/dL 170-290 mg/dL 212-362 mg/dL 20-50% 20-300 ng/mL |
Diagnosi eziologica
Dopo aver confermato la diagnosi di anemia ferropriva, è fondamentale individuare le cause sottostanti alla carenza di ferro. Questo processo è noto come diagnosi eziologica e varia a seconda del sesso e dell’età del paziente:
- Donne in età fertile:
- Si inizia con un’accurata anamnesi di sanguinamento ginecologico e una visita ginecologica;
- Nel caso in cui l’anamnesi ginecologica non fornisca chiarimenti, si procede con il controllo del sangue occulto nelle feci in almeno due occasioni;
- Uomini di età inferiore ai 40 anni:
- È consigliato eseguire test del sangue occulto nelle feci in almeno tre occasioni, a meno che non siano presenti segni di sanguinamento intestinale.
Se i risultati indicano sanguinamento intestinale, sono necessari ulteriori esami mirati come l’endoscopia, il transito esofago-gastroduodenale o il clisma opaco.
Prima di sottoporsi a una colonscopia, la terapia sostitutiva con ferro deve essere sospesa per almeno 10 giorni per garantire una valutazione corretta;
- È consigliato eseguire test del sangue occulto nelle feci in almeno tre occasioni, a meno che non siano presenti segni di sanguinamento intestinale.
- Uomini di età superiore ai 40 anni o donne non mestruate:
- È importante escludere la presenza di sanguinamento intestinale attraverso il test del sangue occulto nelle feci;
- Si devono escludere anche lesioni neoplastiche, in particolare nel colon, mediante esami specifici come la colonscopia.
Questi approcci diagnostici sono essenziali per individuare le cause sottostanti dell’anemia ferropriva e determinare il trattamento più appropriato.
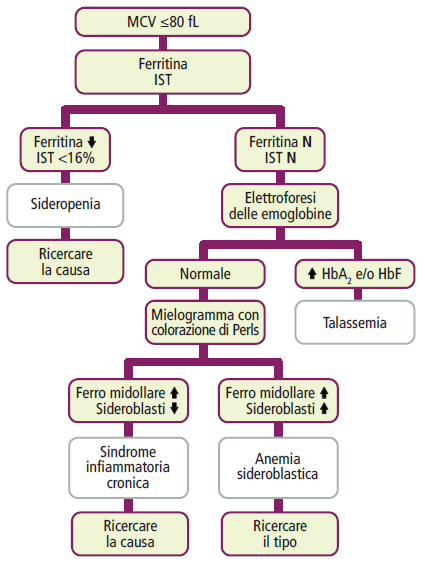
Diagnosi Differenziale
Nel valutare un quadro di microcitosi, è importante considerare anche altre condizioni che possono causare questo tipo di anemia. Le principali condizioni da prendere in considerazione includono:
- Talassemia Minor: una forma ereditaria di anemia che comporta una produzione ridotta di globuli rossi. La talassemia minor è caratterizzata da microcitosi e ipocromia simili a quelle dell’anemia ferropriva. Test specifici per la talassemia, come l’elettroforesi dell’emoglobina o l’analisi del DNA, possono essere necessari per la diagnosi differenziale;
- Anemia da Malattie Croniche, come le patologie infiammatorie (es. artrite reumatoide, lupus eritematoso sistemico), le malattie renali croniche e il cancro possono causare un’alterazione nella produzione di globuli rossi, portando a un quadro di microcitosi. In questi casi, l’anemia è spesso associata a livelli di ferritina normali o elevati, a differenza dell’anemia ferropriva;
- Anemia da carenza di vitamine, come l’acido folico e la vitamina B12 possono causare anemia megaloblastica, caratterizzata da globuli rossi grandi (macrociti) e ipocromici. Questo tipo di anemia è differente dalla microcitosi dell’anemia ferropriva;
- Sindrome da perdita di ferro, come in caso di emorragie croniche (es. ulcera peptica, neoplasie) possono causare perdite eccessive di ferro e quindi un’eventuale microcitosi. La diagnosi di queste condizioni richiede spesso esami specifici per identificare la causa sottostante della perdita di ferro.
| ANEMIA SIDEROPENICA | TALASSEMIA MINOR | ANEMIA INFIAMMATORIA | ANEMIA SIDEROBLASTICA | |
|---|---|---|---|---|
| MCV | ↓ | ↓↓ | N | ↓/N/↑ |
| RDW | ↑↑ | N | ↑ | ↑↑ |
| IPOCROMIA | +++ | + | No | Doppia popolazione |
| SIDEREMIA | ↓↓ | N/↑ | ↓ | ↑↑ |
| IST | <16% | N | N | N |
| FERRITINEMIA | ↓↓ | N/↑ | ↑↑ | N/↑ |
Trattamento
Il trattamento dell’anemia sideropenica si basa sull’eliminazione della causa sottostante e sulla correzione della carenza di ferro. Ecco le principali modalità di trattamento:
- Trattamento Eziologico: è di fondamentale importanza trattare la causa sottostante dell’anemia sideropenica per garantire una risoluzione a lungo termine. Senza eliminare la causa, l’anemia potrebbe persistere nonostante il trattamento con il ferro;
- Ferro Orale: è il trattamento di prima linea. Viene somministrato sotto forma di sale ferroso (Fe++), con una dose tipica di 100-200 mg al giorno fino alla normalizzazione dei depositi di ferro (misurata dalla ferritina), il che può richiedere da 3 a 6 mesi di trattamento. Dopo 7-10 giorni di trattamento, di solito si osserva un aumento dei reticolociti, un segno di produzione aumentata di globuli rossi, che raggiunge il picco massimo dopo circa 10 giorni. È preferibile assumerlo a digiuno per evitare interferenze alimentari con l’assorbimento del ferro. L’associazione con la vitamina C (ad esempio, succo d’arancia) è raccomandata in quanto favorisce l’assorbimento del ferro;
- Ferro Parenterale (Endovenoso): è utilizzato quando vi è intolleranza o inefficacia del ferro orale, malassorbimento (come nelle malattie infiammatorie dell’apparato digerente come il Morbo di Crohn o la colite ulcerosa, gastrite acuta, ulcere), perdite di ferro superiori all’assorbimento, o mancanza di collaborazione del paziente con il trattamento orale. In questi casi, il ferro viene somministrato direttamente in vena per garantire un assorbimento efficace.
Il trattamento dell’anemia sideropenica dovrebbe essere personalizzato in base alla gravità della carenza, alla causa sottostante e alla risposta del paziente alla terapia. È importante monitorare i livelli di ferro e la risposta ematologica durante il trattamento per garantire un recupero ottimale. La durata del trattamento può variare da paziente a paziente e dovrebbe essere stabilita dal medico curante.